Clear Sky Science · sv
Exceptionellt selektiv fångst av spänningssensor hos NaV1.5-kanaler av Mg-protoporfyrin försämrar cancercellsrörelse
Växtpigment pekar på en ny cancerstrategi
Våra hjärtan och våra tumörer kan dela en oväntad sårbarhet: en särskild typ av elektriskt dörrblad i cellmembranet kallad NaV1.5. Denna studie visar att en naturlig släkting till klorofyllens byggstenar i växter, magnesium‑protoporfyrin IX (MgPpIX), kan stänga detta dörrblad med extraordinär precision. Genom att göra det bromsar det kraftigt förflyttningen av vissa cancerceller — vilket antyder att en molekyl inspirerad av fotosyntesens kemi skulle kunna bidra till att tygla metastaser utan att starkt störa hjärna eller muskler.
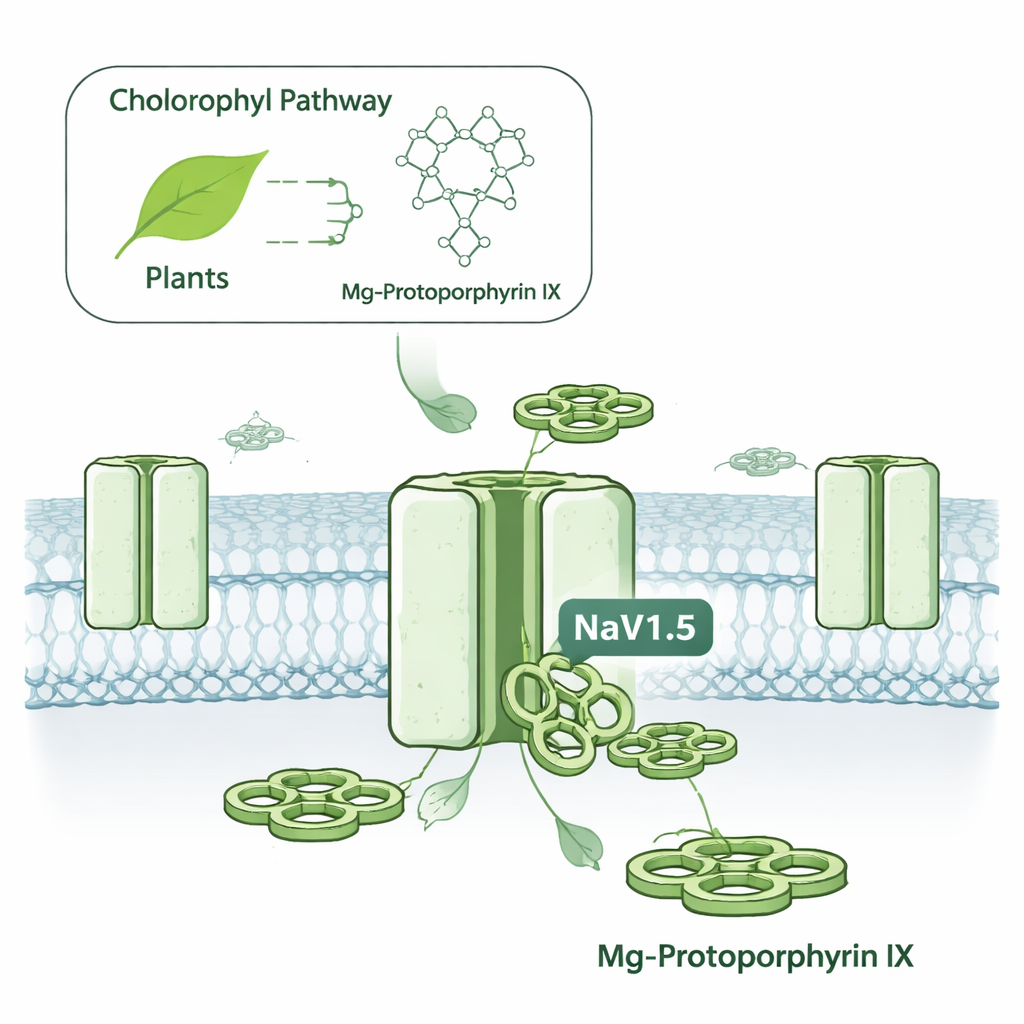
En dold elektrisk strömbrytare i cancerceller
Celler använder spänningsstyrda natriumkanaler som små dörrar som öppnas och stängs för att låta laddade partiklar passera och därigenom skapa elektriska signaler. NaV1.5 är mest känd för sin roll i hjärtrytmen, där den hjälper till att utlösa varje sammandragning. Men samma kanal finns också i flera cancerformer, inklusive bröst‑ och tarmtumörer, där dess aktivitet har kopplats till ökad cellrölighet och invasivitet. Att rikta in sig på NaV1.5 har varit svårt eftersom de flesta natriumkanalsläkemedel även påverkar närbesläktade kanaler i nerver och skelettmuskulatur, vilket riskerar biverkningar som anfall, domningar eller muskelsvaghet. Författarna gav sig därför i kast med att ta reda på om några små molekyler kan särskilja NaV1.5 från dess släktingar med mycket högre selektivitet.
En växtinspirerad blockerare med rekordprecision
Forskargruppen undersökte en familj ringformade molekyler kallade metallprotoporfyriner, som liknar kärnstrukturerna i hem i blod och klorofyll i växter men innehåller olika centrala metallatomer. När de applicerade olika varianter på mänskliga NaV1.5‑kanaler framställda i cellodling framträdde en förening: MgPpIX. Den minskade den elektriska strömmen genom NaV1.5 med ungefär 99 % vid nanomolära koncentrationer, cirka 100 gånger mer potent än en järnbaserad motsvarighet (hemin). Andra metallvarianter, till exempel med nickel eller koppar, var i princip inaktiva. Anmärkningsvärt nog lämnade MgPpIX flera andra mänskliga natriumkanaltyper (som används i hjärnan, perifera nerver och skelettmuskulatur) helt orörda vid samma doser, vilket gör dess selektivitet till en av de skarpaste som någonsin rapporterats för denna kanalfamilj.
Hur molekylen låser en liten spänningsspak
För att förstå denna ovanliga precision kombinerade forskarna genetisk manipulation med datorsimuleringar. Natriumkanaler har fyra upprepade delar, var och en innehållande en "spänningssensor" som skiftar position när membranpotentialen ändras. Genom att byta ut enstaka aminosyror mellan NaV1.5 och dess okänsliga släktingar spårade teamet MgPpIX:s verkan till spänningssensorn i det andra domenet, särskilt två rester som är exponerade mot utsidan av cellen. Molekylär dynamics‑simulationer i en realistisk membranomgivning föreslog att MgPpIX lägger sig intill denna sensor när den befinner sig i sin vilande, "nedre" position. MgPpIX:s positivt laddade metallcenter attraheras av en negativt laddad sidokedja på kanalen, medan den plana ringen interagerar med omgivande lipider. Denna bindning verkar låsa spänningssensorn på plats, vilket hindrar den från att röra sig till den aktiva "övre" staten och därmed hålla kanalen stängd. Intressant nog kan starka depolarisationer — som de under en hjärtslag — tillfälligt fälla loss molekylen, ett beteende författarna beskriver som "reverse use‑dependence."
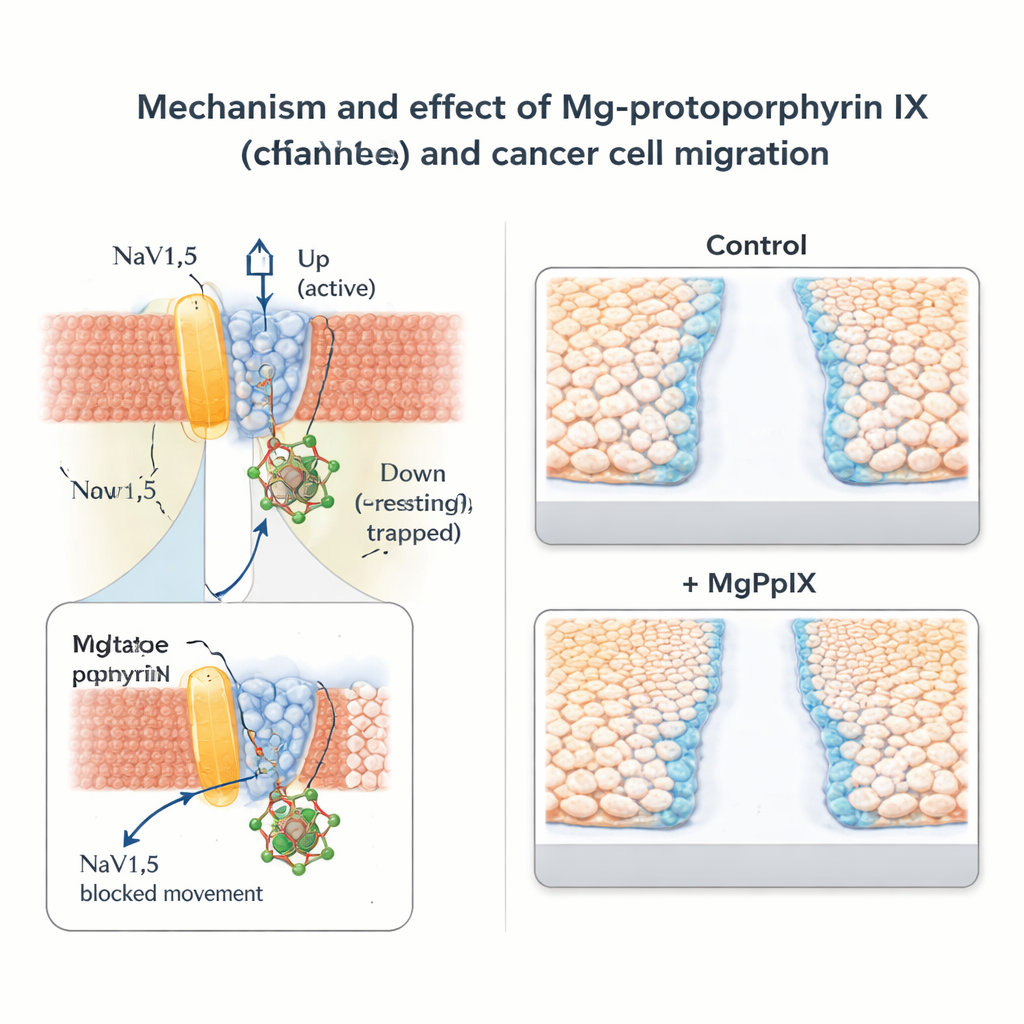
Bromsar cancercellernas rörelse utan bred nervblockad
Forskarteamet undersökte därefter vad denna molekylära broms innebär för cancerbeteende. I bröstcancercellinjen MDA‑MB‑231 och koloncancercellinjen SW‑480, som naturligt uttrycker NaV1.5, minskade MgPpIX dramatiskt natriumströmmarna och saktade ner cellmigration i standardiserade "scratch"‑ och transwell‑tester. Ju mer en given metallprotoporfyrin blockerade NaV1.5, desto mer hindrade den cellrörelsen, vilket stärkte kopplingen mellan kanalaktivitet och motilitet. Däremot visade cancer‑cellinjer som saknar NaV1.5 inget svar på MgPpIX varken elektriskt eller i migrationstester, vilket stöder idén att effekten är högspecifik snarare än allmänt toxisk. Jämfört med den klassiska natriumkanalstoxinen tetrodotoxin uppnådde MgPpIX starkare undertryckande av migration vid betydligt lägre koncentrationer.
Hopp och försiktighet för framtida anti‑metastatiska läkemedel
För en icke‑specialist är huvudbudskapet att forskarna funnit en växtrelaterad molekyl som fungerar som en precis klämma på ett hjärttypiskt elektriskt dörrblad som kapats av vissa cancerformer. Genom att fånga dörrbladets lilla spänningsspak i dess viloposition kan MgPpIX kraftigt dämpa cancercellers rörlighet i laboratoriet samtidigt som andra natriumkanaler som är avgörande för känsel och rörelse skonas. Eftersom hjärtats snabba elektriska aktivitet delvis kan lätta denna blockad kan det till och med finnas ett säkerhetsfönster där tumörceller hämmas mer än hjärtceller. Medan MgPpIX i sig kanske inte är redo som läkemedel, ger dess unika bindningsställe och verkningsmekanism en kraftfull ritning för att designa framtida läkemedel som syftar till att stoppa cancerspridning genom att rikta in sig på NaV1.5 med enastående selektivitet.
Citering: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
Nyckelord: natriumkanaler, Nav1.5, cancercellsrörelse, klorofyll‑besläktade molekyler, riktade jonkanal‑läkemedel