Clear Sky Science · sv
MiniPromoters Ple384 (TH) och Ple388 (PITX3) för riktning mot midbrain-dopaminerga neuroner hos möss och apor
Varför denna forskning är viktig för hjärnhälsa
Hjärnans dopaminproducerande celler hjälper oss att röra oss, lära av belöningar och behålla motivation. Det är också dessa celler som dör vid Parkinsons sjukdom. Forskare och läkare vill leverera nyttiga gener eller molekylära verktyg specifikt till dessa utsatta neuroner, både i försöksdjur och så småningom hos människor. Men att styra genterapi så att den aktiveras endast i rätt celler, och inte i hela hjärnan, har varit ett stort hinder. Denna studie beskriver två nya, kompakta DNA‑”strömbrytare” som pålitligt kan slå på gener nästan uteslutande i midbrain-dopaminneuron hos möss och apor, och öppnar en väg mot mer precisa och potentiellt säkrare behandlingar.
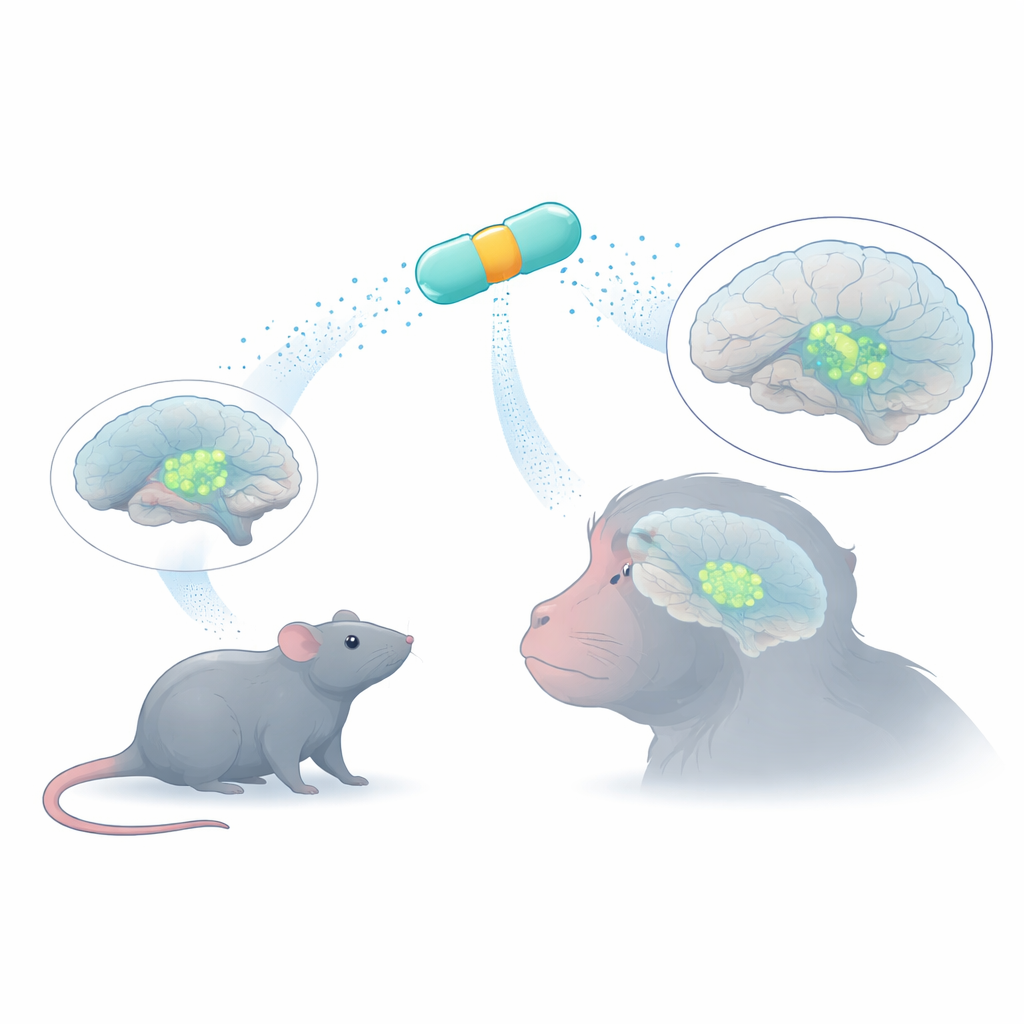
Små genetiska strömbrytare med ett stort uppdrag
För att få ett terapeutiskt geninnehåll in i hjärnceller använder forskare ofta adenoassocierade virus (AAV), ofarliga leveransfordon som bara kan bära en begränsad mängd DNA. Inuti varje virus fungerar en kort promotorsekvens som en på‑/av‑knapp och bestämmer var genen blir aktiv. Många naturliga promotorer är för stora eller för ospecifika och slår på gener i för många celltyper. Teamet använde bioinformatik för att designa åtta mycket kompakta ”MiniPromoters” från mänskligt DNA—korta kombinationer av reglerande element hämtade från gener som är kända markörer för dopaminproducerande neuroner. Målet var en uppsättning strömbrytare som ryms i AAV men ändå driver stark, cellspecifik uttryckning.
Att hitta rätt mål i musens hjärna
De åtta kandidat‑MiniPromotors testades först i möss. Varje promotor placerades i en AAV som bar ett grönt fluorescerande protein, vilket gjorde det möjligt för forskarna att se var strömbrytaren var aktiv. De levererade virusen antingen i blodomloppet eller direkt i hjärnans vätskefyllda utrymmen. De flesta MiniPromoters misslyckades med att vara selektiva: vissa tändes i många icke‑dopaminceller, andra fungerade knappt alls. Två stod ut. En, kallad Ple384, byggdes från regleringsregioner i genen för tyrosinhydroxylas, det avgörande enzymet som används av alla katekolaminproducerande neuroner. Den andra, Ple388, kom från PITX3, en gen som är kritisk för en delmängd av midbrain-dopaminneuroner. Både Ple384 och Ple388 gav starka, tätt begränsade signaler i substantia nigra compacta och ventral tegmental area—midbrain‑knutpunkterna för dopaminneuroner—med över 90 % av märkta celler som också bar dopaminets karakteristiska molekyl.
Från möss till apor utan att borra djupt i hjärnan
Någon genterapi riktad mot mänsklig sjukdom måste så småningom fungera i primater, vars hjärnor är större och mer komplexa. Direkt injektion i substantia nigra är tekniskt krävande och kan skada denna lilla, djupa struktur. I stället testade forskarna om samma MiniPromoters kunde levereras i cerebrospinalvätskan hos rhesusmakaker via en enda injektion i en lateral ventrikel. Med hjälp av en AAV‑kapsidvariant som sprider sig väl från vätskerymderna fann de att både Ple384 och Ple388 drev robust uttryck i midbrain‑dopaminneuron i substantia nigra och ventral tegmental area, samtidigt som andra dopaminrika regioner som hypotalamus och locus coeruleus i stor utsträckning undveks. De flesta märkta celler i målregionen var dopaminneuroner, vilket bekräftar att strömbrytarna behöll sin selektivitet över arter.
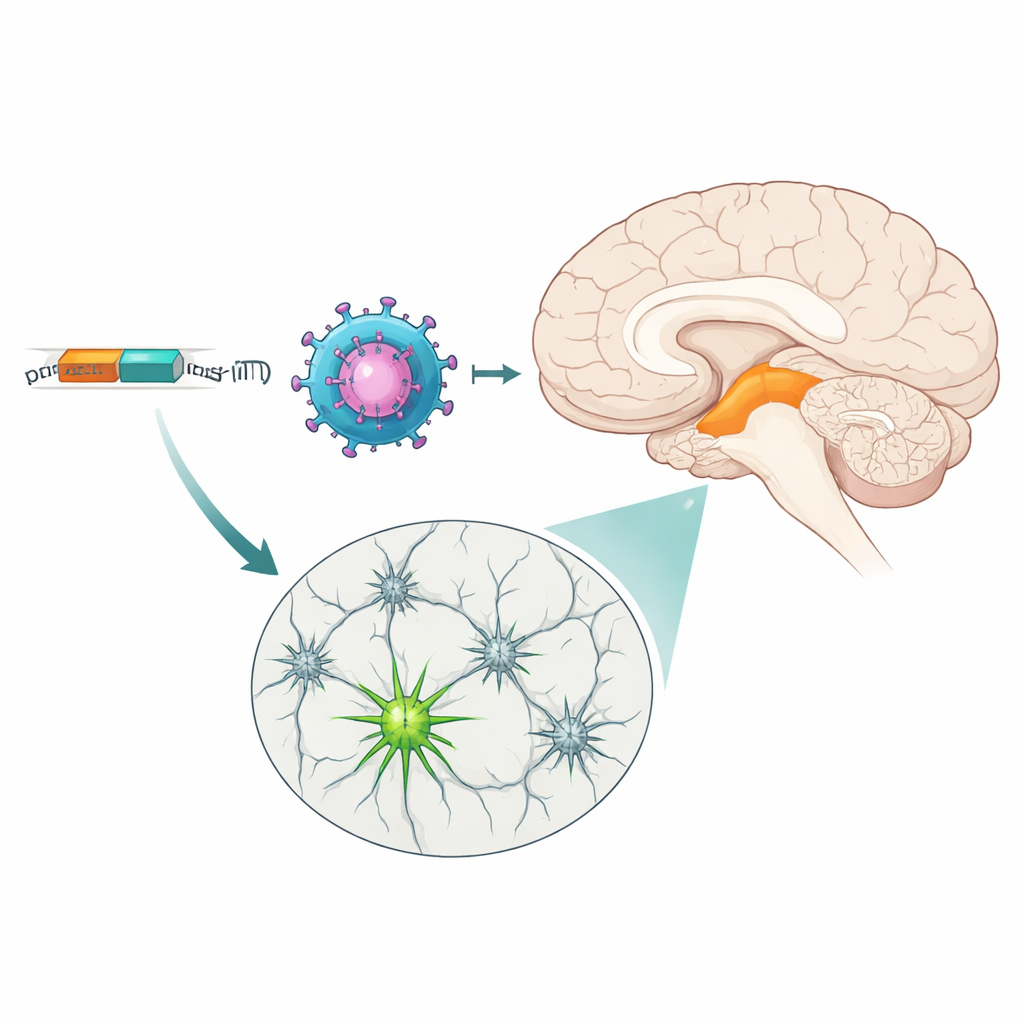
Två verktyg med olika styrkor
Även om båda MiniPromoters nådde sina mål gjorde de det med olika mönster. Ple384, baserad på den bredare tyrosinhydroxylasgenen, tände fler neuroner totalt och täckte både ventrala och dorsala skikten av substantia nigra samt en större del av ventral tegmental area. Ple388, som speglar den mer begränsade PITX3‑genen, etiketterade främst en delmängd av ventrala tier‑neuroner och gav svagare fluorescens. Off‑target‑uttryck sågs främst nära injektionsställen och i vissa perifera organ efter administrering via blodomloppet, men noggranna kontroller visade att de virala vektorerna kunde nå många hjärnregioner; det var MiniPromoters själva som begränsade uttrycket mestadels till midbrain‑dopaminneuroner. Denna justerbara styrka—en mer kraftfull och bred, en mer selektiv och måttlig—innebär att forskare kan välja den strömbrytare som bäst passar deras behov, från försiktig modulering till storskalig intervention.
Vad detta betyder för framtida terapier
För en icke‑specialist är huvudbudskapet att författarna har skapat två kompakta genetiska strömbrytare som fungerar som precisa, programmerbara ljusbrytare för dopaminneuroner hos både möss och apor. Ple384 erbjuder stark, omfattande åtkomst till dessa celler, medan Ple388 fokuserar på en snävare, särskilt sårbar delmängd. Eftersom strömbrytarna är tillräckligt små för att bekvämt rymmas i vanligen använda virala vektorer lämnar de plats för terapeutiska gener och kan hjälpa till att minska biverkningar genom att undvika oönskade hjärnregioner. När genterapi för Parkinsons sjukdom och närliggande tillstånd utvecklas kommer sådana riktade kontroll‑element att vara viktiga ingredienser för behandlingar som är både kraftfulla och precisa.
Citering: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
Nyckelord: dopaminneuroner, genterapi, Parkinsons sjukdom, AAV-vektorer, cellspecifika promotorer