Clear Sky Science · sv
Terapeutiska effekter av IGF-2 vid NMOSD genom hämning av astrocyt-apoptos via modulering av IGF-1R/PI3K/AKT-signalvägen
Skydda hjärnan vid en lite känd autoimmun sjukdom
Neuromyelit optica spektrumstörning, eller NMOSD, är en sällsynt men förödande autoimmun sjukdom som angriper synnerverna och ryggmärgen och ofta lämnar patienter blinda, förlamade eller med allvarliga kognitiva problem. Nuvarande läkemedel dämpar i huvudsak immunsystemet, är kostsamma och skyddar inte direkt hjärnans celler från skada. Denna studie undersöker om en naturlig tillväxtrelaterad molekyl i blodet, kallad IGF‑2, kan hjälpa till att skydda hjärnceller från skada vid NMOSD och erbjuda ett nytt behandlingssätt.
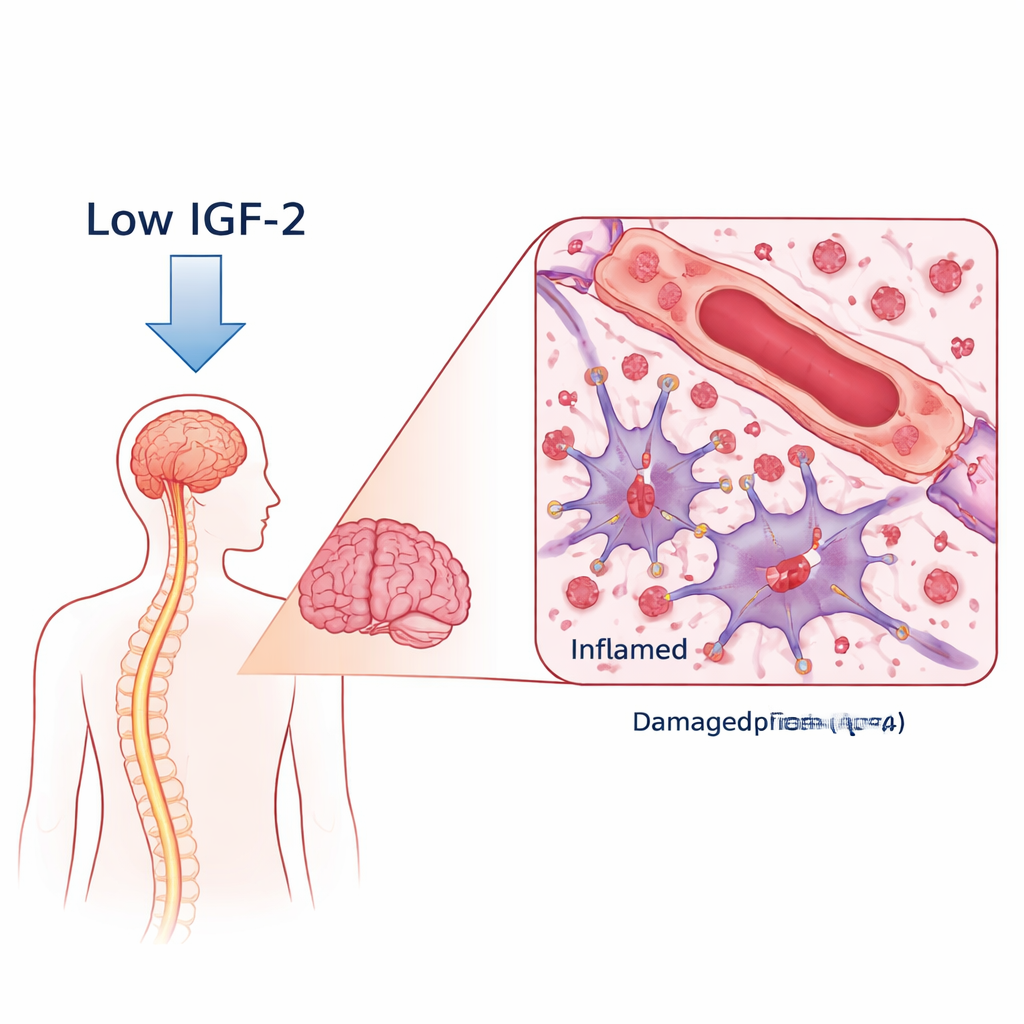
En skadlig antikropp och en saknad skyddare
Vid NMOSD producerar kroppen antikroppar mot ett vattenkanalprotein kallat AQP4, som finns på stjärnformade stödjande celler i hjärnan kallade astrocyter. När dessa antikroppar binder utlöser de immunsvar som skadar astrocyterna, avleder myelin (nervernas isolerande hölje) och kan skada neuroner. Forskarna jämförde blod från kvinnor med AQP4-antikroppspositiv NMOSD med friska frivilliga. Genom en bred proteinscreening fann de att IGF‑2-nivåerna var markant lägre hos NMOSD-patienter, medan två IGF-bindande proteiner som kan fånga upp IGF‑2 var högre. Viktigt är att patienter med lägst IGF‑2 tenderade att ha större funktionsnedsättning och sämre resultat på tester av tänkande och minne, vilket kopplar denna molekyl till sjukdomens svårighetsgrad och kognitiv hälsa.
Standardbehandling hjälper IGF-2 att återhämta sig
Många NMOSD-patienter får rituximab, ett läkemedel som tar bort antikroppsproducerande B‑celler. Teamet mätte blodproteiner före och efter rituximabbehandling. Efter terapin steg IGF‑2-nivåerna och de bindande proteinerna föll, i riktning mot mönstret som ses hos friska personer. Detta tyder på att dämpning av immunsystemet kan göra det möjligt för kroppen att återställa vissa av sina egna skyddsfaktorer. Även om rituximab inte är avsett att verka på IGF‑2, antyder förändringen i denna molekyl att den kan vara en del av kroppens återhämtningssvar, och att övervakning av IGF‑2 skulle kunna hjälpa till att följa patienternas tillstånd över tid.
Test av IGF-2 i en musmodell av sjukdomen
För att se om IGF‑2 kan göra mer än att signalera sjukdomsallvar vände sig forskarna till en musmodell. De injicerade mänskliga AQP4-antikroppar och mänskligt komplementsystem i hjärnorna på möss, vilket återupprepade nyckelfunktioner hos NMOSD: förlust av AQP4 på astrocyter, inflammation, myelinskada och extremitetssvaghet. En annan grupp möss fick först ett ofarligt virus som fick deras hjärnceller att producera extra IGF‑2. Dessa möss med förhöjt IGF‑2 tappade mindre vikt, hade mildare rörelseproblem och visade mindre myelinförlust och inflammation i hjärn- och ryggmärgsvävnad. Standardbehandling med rituximab hjälpte också, men överuttryck av IGF‑2 verkade skydda hjärnvävnaden mer direkt, vilket tyder på en neuroprotektiv roll snarare än enbart en immunhämmande effekt.
Hur IGF-2 dämpar celldöd och inflammation
Teamet undersökte sedan astrocyter i laboratorieförsök som exponerats för NMOSD-antikroppar. Vanligtvis sänkte dessa antikroppar nivåerna av en viktig receptor kallad IGF‑1R och dämpade en nedströms skyddsväg känd som PI3K/AKT, samtidigt som de aktiverade ”själv-destruktion”-proteiner och inflammatoriska signaler. När forskarna tvingade astrocyter att producera mer IGF‑2 återaktiverades denna skyddsväg, markörer för celldöd minskade och cellerna frigjorde färre inflammatoriska molekyler såsom IL‑1β, IL‑6 och TNF‑α. Blockering av IGF‑1R-receptorn raderade delvis dessa fördelar, vilket visar att IGF‑2 främst verkar genom att aktivera IGF‑1R/PI3K/AKT-kedjan inne i astrocyterna. I levande möss minskade också IGF‑2-ökning aktiveringen av mikroglia, hjärnans immunsentinel, och sänkte inflammatoriska signaler i blodet.
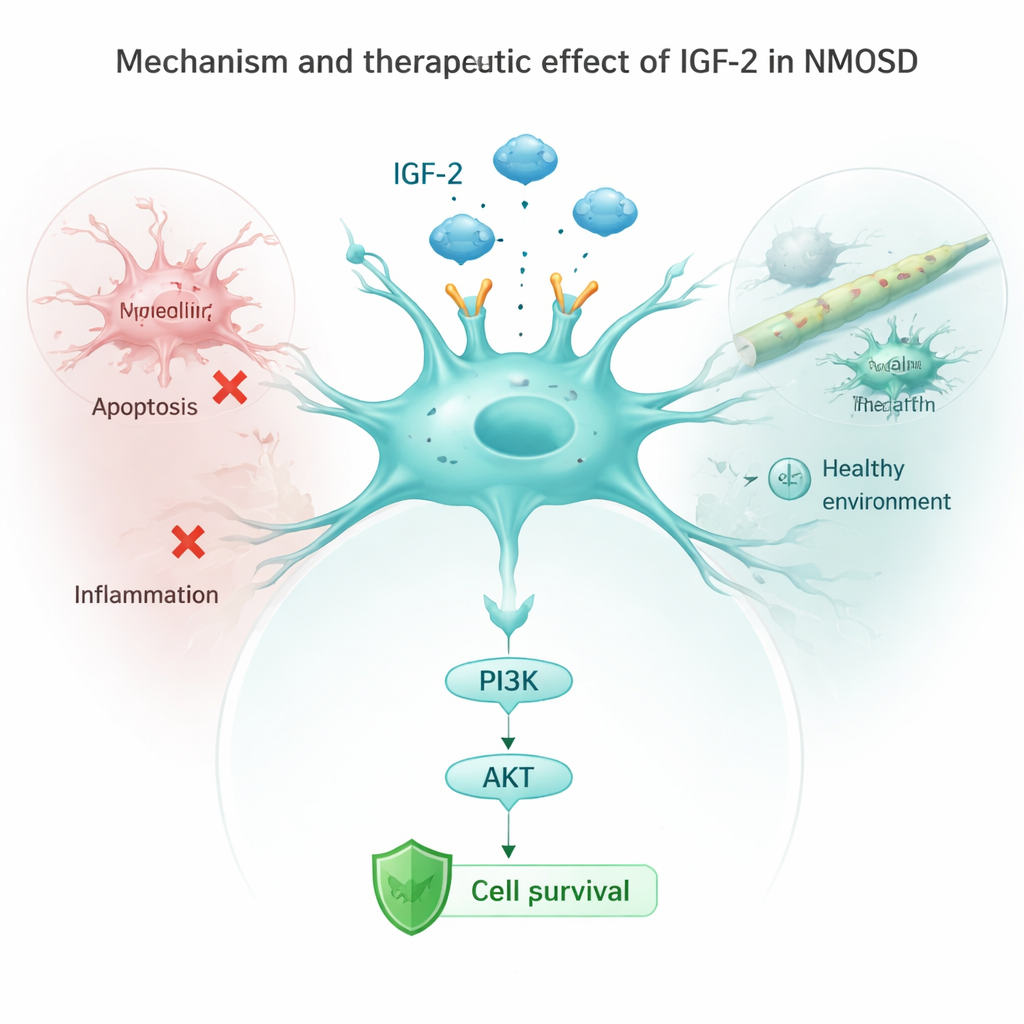
Vad detta kan innebära för patienter
Tillsammans tyder dessa fynd på att låg IGF‑2 både är en varningssignal och en missad möjlighet vid NMOSD. Patienter med mindre IGF‑2 tenderar att vara mer funktionsnedsatta och ha sämre kognitiv funktion, medan återställande eller förstärkning av IGF‑2 i experimentella modeller hjälper astrocyter att överleva, minskar hjärninflammation och minskar nervskador. Även om detta arbete är tidigt och baserat på små patientgrupper och djurstudier, pekar det mot IGF‑2 som ett lovande mål för framtida behandlingar som inte bara dämpar det immunologiska anfallet utan också direkt skyddar sårbara hjärnceller.
Citering: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
Nyckelord: neuromyelit optica, astrocyter, IGF-2, neuroinflammation, neuroprotection