Clear Sky Science · sv
Integrera nätverkstoxikologi, maskininlärning och molekylära dynamiksimuleringar för att avslöja tanshinon IIA:s dubbla mekanismer i trippelnegativ bröstcancer och doksorubicinförorsakad kardiotoxicitet
Varför denna forskning är viktig för patienter
Doksorubicin är ett standardläkemedel mot bröstcancer, men det har en allvarlig nackdel: det kan skada hjärtat, ibland år efter avslutad behandling. Samtidigt behöver trippelnegativ bröstcancer — en svårbehandlad form som saknar vanliga hormon- och tillväxtfaktormål — bättre terapier. Denna studie undersöker om tanshinon IIA, en förening utvunnen från den traditionella kinesiska örten Salvia miltiorrhiza, både kan skydda hjärtat från doksorubicins toxicitet och hjälpa till att angripa aggressiva brösttumörer, vilket potentiellt skulle göra kemoterapi säkrare och mer effektiv.
En förening, två stora problem
Doksorubicin har räddat otaliga liv, men dess nytta begränsas av dosberoende kardiotoxicitet: över en viss livstidsdos stiger risken för hjärtsvikt kraftigt. Kliniker ställs ofta inför ett smärtsamt avvägande mellan att kontrollera cancern och skydda hjärtat. Tidigare laboratoriestudier föreslog att tanshinon IIA kan stärka antioxidativa försvar i hjärtceller och direkt döda cancerceller, men de molekylära mekanismerna var oklara. Författarna gav sig i kast med att systematiskt kartlägga hur denna enda förening kan dämpa hjärtskada samtidigt som den angriper trippelnegativ bröstcancer, och därigenom bygga en bro mellan traditionell medicin och modern precisionsonkologi. 
Utvinning av stora biologiska data för hjärtskydd
För att förstå hjärtskyddet samlade teamet först tusentals gener kopplade till kardiotoxicitet från flera stora databaser och kombinerade dem med kända proteintargets för doksorubicin och tanshinon IIA. Tretton ”överlappande” targets framkom — proteiner som var förknippade med hjärtskada, interagerade med doksorubicin och också potentiellt kunde påverkas av tanshinon IIA. Genom protein–protein-interaktionskartor begränsade forskarna detta till sex kärnspelare, inklusive CCND1 (en cellcykelregulator), APAF1 (en utlösare av programmerad celldöd), AR (androgenreceptor), TERT (viktig för upprätthållandet av kromosomändar), MMP2 (ett vävnadsombyggnadsenzym) och NQO1 (ett antioxidativt enzym). Datorsimuleringar av dockning och molekylär dynamik antydde att både doksorubicin och tanshinon IIA kan binda hårt till dessa proteiner, men att komplexen med tanshinon IIA ofta är mer stabila och energetiskt fördelaktiga, vilket tyder på att den örtbaserade föreningen kan omdirigera eller mildra doksorubicins skadliga signaler i hjärtat.
Upptäcka hur det riktar sig mot aggressiva brösttumörer
På cancersidan fokuserade forskarna på genuttrycksdata för trippelnegativ bröstcancer. De jämförde tumörprover med normal bröstvävnad för att hitta hundratals gener som var onormalt på- eller avstängda. De använde sedan en teknik kallad viktad gen‑ko‑uttrycks‑nätverksanalys för att identifiera genkluster som var starkast kopplade till det trippelnegativa fenotypen. Genom att korsa dessa cancergener med förutsedda targets för tanshinon IIA destillerade de fram en kort lista kandidater och körde tre oberoende maskininlärningsmetoder för att se vilka gener som bäst skilde tumör från normal vävnad och mest sannolikt var kliniskt relevanta. Konvergerande bevis framhävde ett tydligt mål: EZH2, en gen som hjälper till att packa DNA och ofta är överaktiv i aggressiva cancerformer.
Koppla tumörbiologi och immunsystemet
För att förstå varför EZH2 är viktig i verkliga patienter undersökte teamet stora cancerregister. De fann att EZH2 är markant mer aktiv i invasiva brösttumörer än i normal bröstvävnad. Även om dess uttryck inte elegant följde total överlevnad för alla bröstcancerfall, var det starkt kopplat till egenskaper i tumörens immikromiljö. Högre EZH2‑nivåer korrelerade med större infiltration av flera immuncellstyper — såsom B‑celler och T‑celler — och med ökat uttryck av molekyler som både stimulerar och undertrycker immunsvar, inklusive välkända checkpoint‑proteiner som CTLA‑4 och LAG‑3. Dessa mönster tyder på att EZH2 befinner sig i ett vägskäl mellan tumörtillväxt och immun kontroll, och att ett läkemedel som tanshinon IIA, genom att påverka EZH2, kan bidra till att omforma hur immunsystemet känner igen och angriper trippelnegativ bröstcancer. 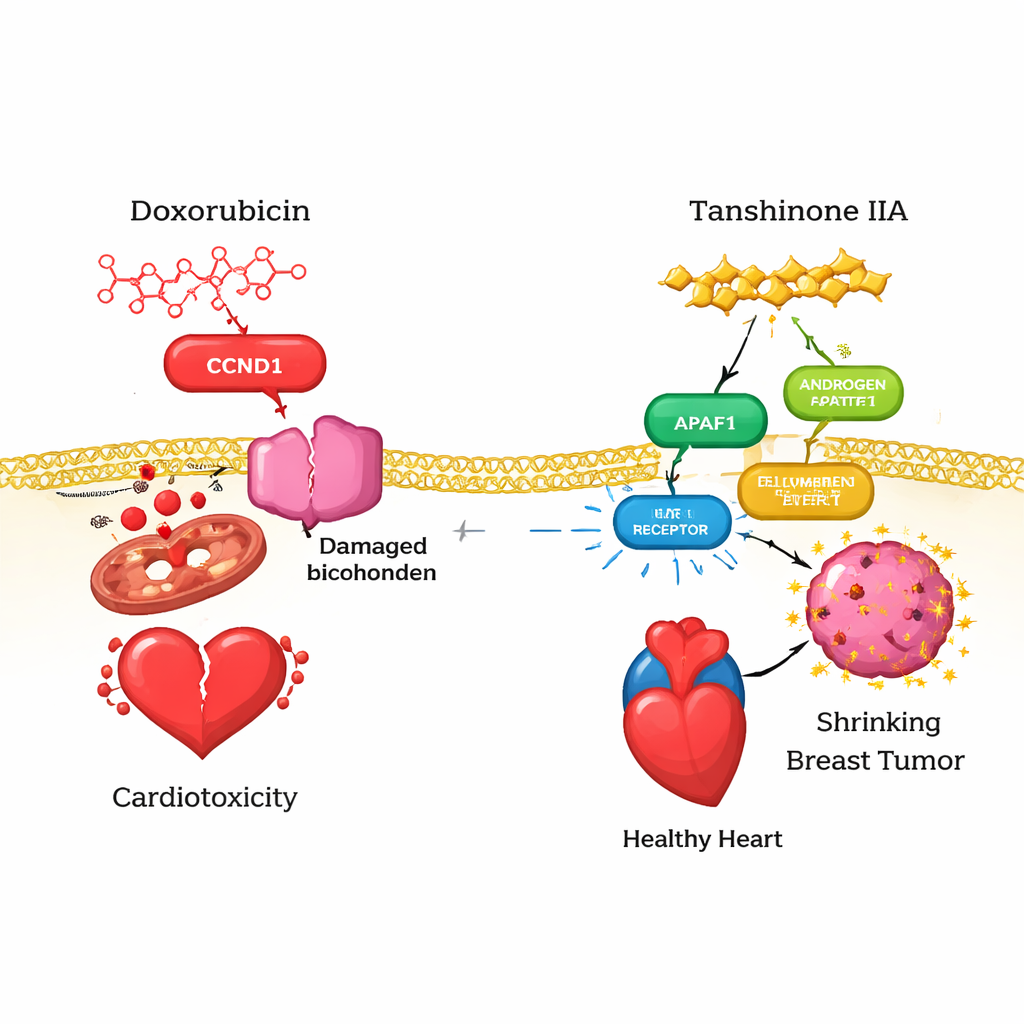
Vad detta kan innebära för framtida behandling
Enkelt uttryckt föreslår detta arbete att tanshinon IIA skulle kunna ha en dubbel roll i bröstcancerbehandling: fungera som en slags ”kemisk sköld” som minskar doksorubicinrelaterad hjärtskada genom att stabilisera nyckelproteiner som skyddar hjärtat, och samtidigt fungera som ett riktat vapen mot trippelnegativ bröstcancer via sin påverkan på EZH2 och relaterade immunsystemvägar. Resultaten bygger på beräknings‑ och statistiska analyser snarare än djur‑ eller kliniska studier, så de utgör en tidig ritning snarare än en färdig behandling. Ändå erbjuder de en detaljerad molekylär färdplan för att designa kombinationsbehandlingar som bevarar doksorubicins livräddande kapacitet samtidigt som dess långsiktiga risker minskas — och för att översätta en traditionell örtingrediens till ett modernt, mekanismstyrt cancerkomplement.
Citering: Wu, B., Lan, Xh., Chen, Xq. et al. Integrating network toxicology, machine learning, and molecular dynamics simulations to reveal tanshinone iia’s dual mechanisms in TNBC and doxorubicin-induced cardiotoxicity. Sci Rep 16, 6861 (2026). https://doi.org/10.1038/s41598-026-37428-8
Nyckelord: tanshinone IIA, doxorubicin kardiotoxicitet, trippelnegativ bröstcancer, EZH2, nätverksfarmakologi