Clear Sky Science · sv
GJB2 c.109G > A-mutation som aktiverar IFI27-medierad mitokondriell apoptosväg och leder till ärftlig icke-syndromisk hörselnedsättning
Varför mikroskopiska hörselceller betyder så mycket för barns framtid
Hörselnedsättning som är närvarande vid födseln drabbar miljontals barn världen över och påverkar ofta hur de lär sig tala, klarar skolan och knyter sociala kontakter. Ett av de vanligaste genetiska orsakerna är genen GJB2, men läkare har inte fullt ut förstått hur förändringar i denna gen faktiskt skadar innerörat. Denna studie använder zebrafisk och humana celler för att spåra händelsekedjan från en enda DNA-förändring i GJB2 till döden av känsliga ljudkännande celler, och pekar på en ny molekyl, IFI27, som en möjlig måltavla för framtida behandlingar.
En vanlig genförändring bakom tyst barndom
Forskarna började med att screena blodprover från 1 199 barn med misstänkt ärftlig hörselnedsättning i Fujianprovinsen, Kina. De fokuserade på flera välkända dövhetsgener och fann att förändringar i GJB2 dominerade bilden och stod för 85 % av alla upptäckta mutationer. Bland dessa var en specifik förändring kallad c.109G>A (även känd som p.Val37Ile) mest frekvent. Denna variant är relativt vanlig i allmänheten men starkt överrepresenterad hos personer med hörselnedsättning, vilket tyder på att den spelar en central roll i icke-syndromisk hörselnedsättning — hörselproblem som uppträder utan andra medicinska tecken.
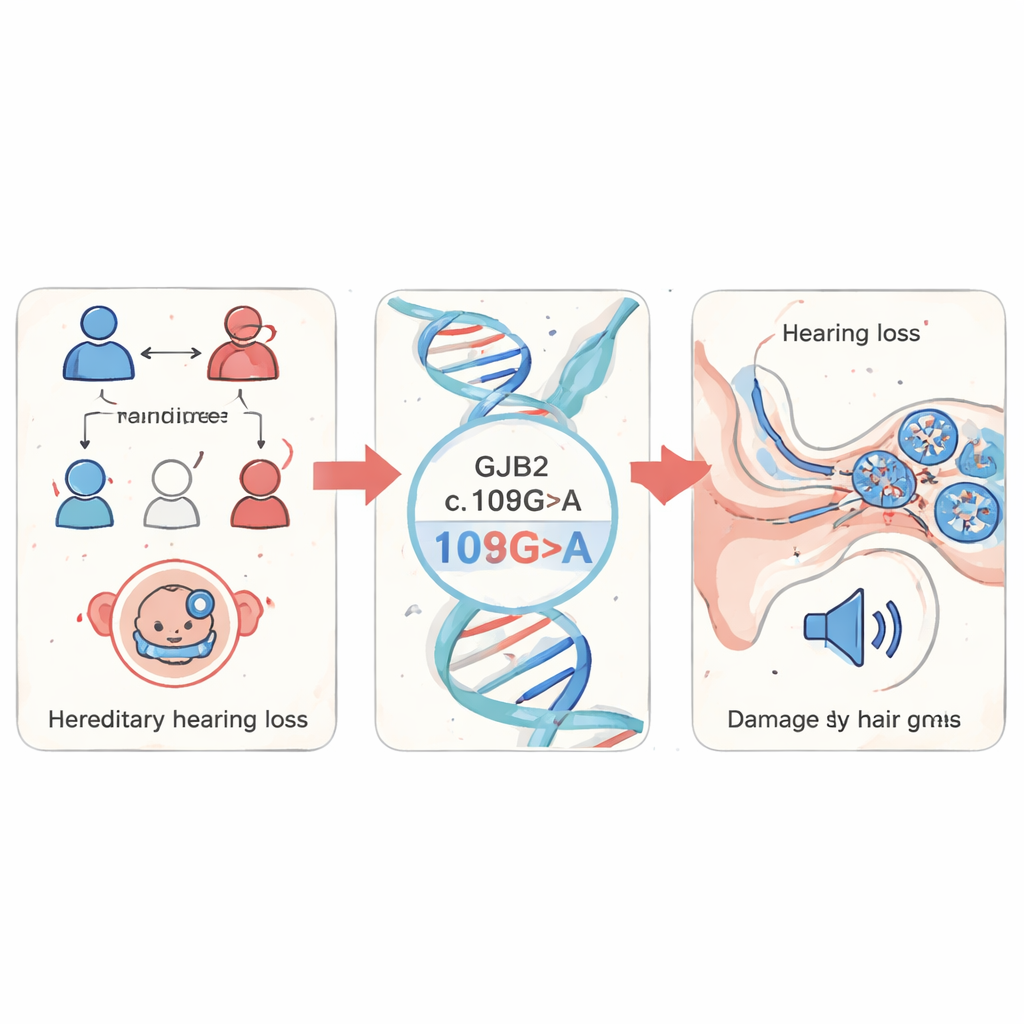
Följa skadorna i en genomskinlig fisk
För att se vad denna mutation gör i en levande organism vände teamet sig till zebrafisk, en liten sötvattensfisk vars embryon är genomskinliga och delar många gener och öronstrukturer med människor. De konstruerade zebrafiskembryon så att de producerade antingen normal mänsklig GJB2 eller den c.109G>A-mutanta versionen, och använde också en ”knockdown”-metod för att minska fiskens eget gjb2-genuttryck. Embryon med den mutanta eller reducerade genen visade fördröjd tillväxt, böjda svansar och svullnad runt hjärtat — tecken på att utvecklingen gick fel. Viktigast var att deras inneröron var tydligt avvikande: nyckelstrukturer kallade otoliter var mindre och längre ifrån varandra, och det vätskefyllda cochleära området var förminskat. När forskarna återinförde normal GJB2 tillsammans med mutanten förbättrades många av dessa strukturella problem, vilket visar att mutationen i sig driver defekterna.
Från trasiga öron till försämrat hörselbeteende
Eftersom hörseln beror på små ”hårceller” som omvandlar ljudvibrationer till nervsignaler färgade teamet dessa celler i zebrafisken. Fisk med GJB2-mutation eller knockdown hade betydligt färre hårceller både i innerörat och längs kroppens yta, där zebrafisk också känner vattenrörelser. Forskarna testade sedan hur bra fiskarna reagerade på ljud. Med ett automatiserat spårningssystem mätte de hur långt och hur snabbt 5 dagar gamla larver simmade när de utsattes för korta ljudpulser. Normal- och vildtyp-GJB2-fisk svarade genom att simma längre och snabbare, medan mutant- och knockdown-fisk knappt ändrade sitt beteende, vilket indikerar försämrad hörsel. Återigen återställde tillsats av normal GJB2 delvis både antalet hårceller och ljuddriven rörelse.
En dödande bana inne i cellens kraftverk
För att förstå vad som hände inne i cellerna användes RNA-sekvensering för att jämföra genaktivitet mellan normala zebrafiskar och de med minskat gjb2. En grupp gener kopplade till den ”mitokondriella apoptosvägen” — en självdestruktionsväg centrerad i cellens energifabriker — var starkt aktiverade. Särskilt flera medlemmar av IFI27-familjen framträdde, tillsammans med välkända celldödsaktörer såsom Bax, cytokrom c, Apaf1 och kaspaser. Uppföljande experiment i humana HEK293-celler bekräftade mönstret: celler med mutanta GJB2 producerade mer reaktiva syreföreningar (ROS, en form av oxidativ stress), frigjorde mer cytokrom c från mitokondrier och slog på apoptosproteiner, vilket ledde till ökad celldöd. När forskarna tystade IFI27 i celler som bar den mutanta genen sjönk ROS-nivåerna, dödssignalerna dämpades och färre celler genomgick apoptos.
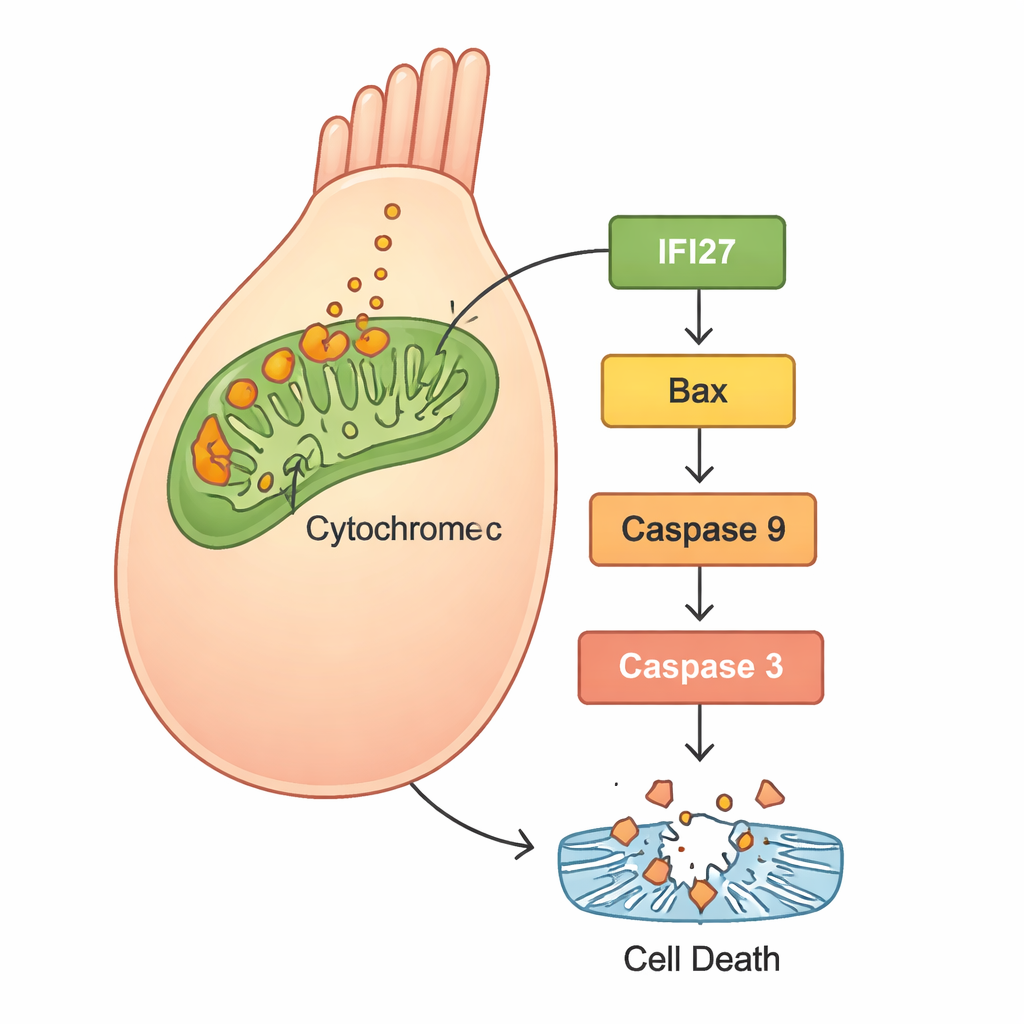
Vad detta betyder för framtida behandlingar
Sammantaget pekar fynden på en tydlig berättelse: GJB2 c.109G>A-mutationen stör normal utveckling och funktion i innerörat, inte bara genom att påverka cellkommunikation utan också genom att utlösa stress i mitokondrierna. Denna stress ökar uttrycket av IFI27 och relaterade gener, frigör cytokrom c och aktiverar en kaskad av proteiner som driver hårceller mot programmerad celldöd. Eftersom hårceller inte lätt återbildas hos människor leder deras förlust till permanenta hörselnedsättningar. Genom att visa att nedreglering av IFI27 kan dämpa denna destruktiva kaskad i humana celler framhäver studien IFI27 som en lovande måltavla för läkemedel eller genbaserade terapier. Medan sådana behandlingar fortfarande ligger långt fram i tiden — och troligen behöver ges mycket tidigt i livet — erbjuder detta arbete en konkret molekylär färdplan för att omvandla en tidigare gåtfull genmutation till en potentiellt förebyggbar orsak till barndomsdövhet.
Citering: Chen, Y., Zhao, P., Lin, Q. et al. GJB2 c.109G > A mutation activating IFI27-mediated mitochondrial apoptosis pathway leading to hereditary non-syndromic hearing loss. Sci Rep 16, 6240 (2026). https://doi.org/10.1038/s41598-026-37393-2
Nyckelord: genetisk hörselnedsättning, GJB2-mutation, zebrafiskmodell, mitokondriell apoptos, IFI27