Clear Sky Science · sv
Identifiering och karaktärisering av fibroblast-relaterade biomarkörer och proinflammatoriska subpopulationer i parodontit genom integrerad transkriptomisk och enkelcellsanalys
Varför dina tandkött spelar roll bortom leendet
Blödande tandkött och lösa tänder kan verka vara små problem, men kronisk tandköttssjukdom—kallad parodontit—kan skada käkbenet, leda till tandförlust och är kopplad till tillstånd som hjärtsjukdom och diabetes. Denna studie granskar en ofta förbisedd cellgrupp i tandköttet, kallade fibroblaster, för att förstå hur de driver eller dämpar inflammation. Genom att kombinera stora genetiska dataset med enkelcellsanalys avslöjar forskarna nya varningssignaler och celltyper som kan förbättra hur tandläkare diagnostiserar och behandlar tandköttssjukdom.
Gömda aktörer i ömma tandkött
Fibroblaster är arbetshästarna som bygger och upprätthåller bindväven som håller tänderna på plats. I åratal betraktades de främst som strukturellt ”stomme”. Denna forskning visar att de är mycket mer: fibroblaster kan fungera som små kontrollcenter för inflammation. När bakterier rubbar den normala mikrobiella balansen i munnen svarar fibroblaster genom att släppa ut kemiska budbärare som lockar immunceller och som antingen hjälper till att reparera vävnad eller förvärrar skadan. Författarna fokuserade på att hitta fibroblastrelaterade gen-signaler som skiljer friska tandkött från parodontit, och på att identifiera fibroblastsubgrupper som blir särskilt inflammatoriska i sjuk vävnad.
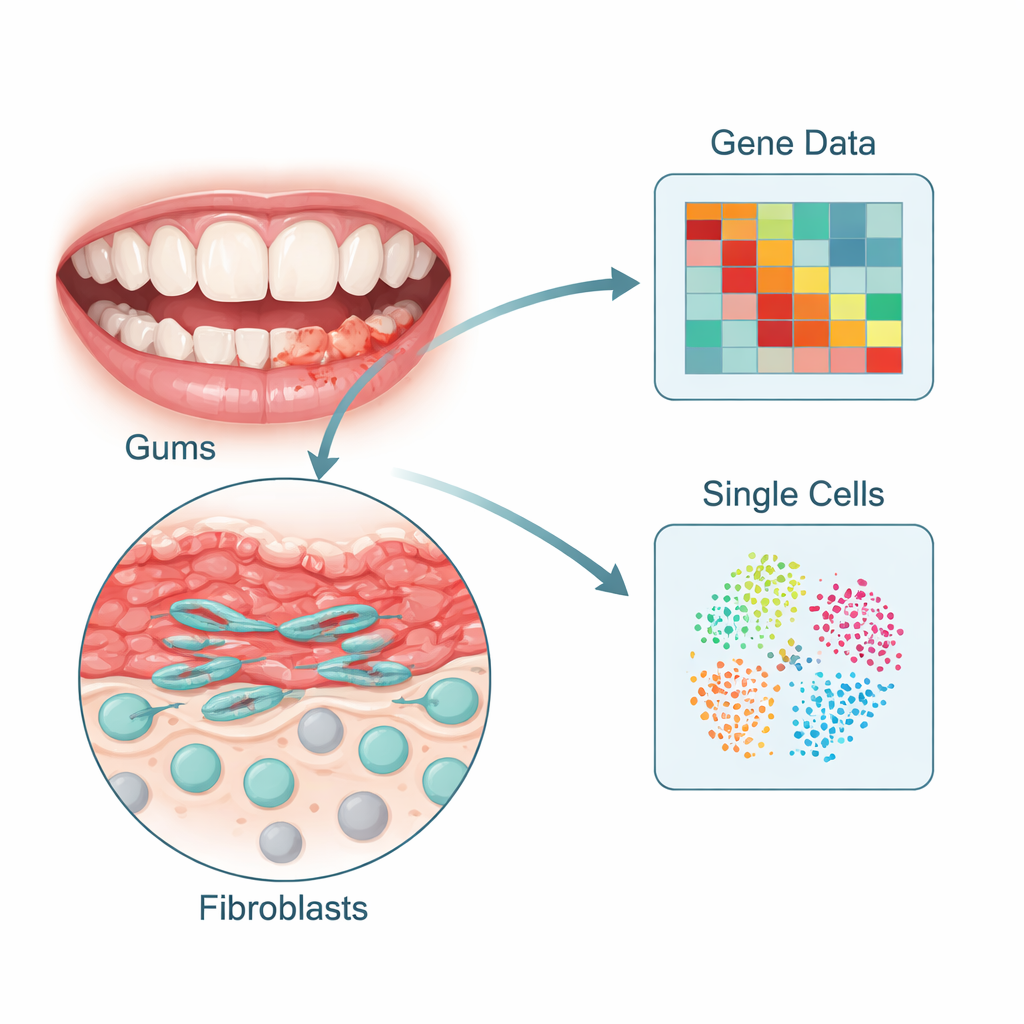
Skanning av tandköttsvävnad cell för cell
För att uppnå detta grävde teamet i flera stora genuttrycks-dataset från patienter med friska tandkött respektive parodontit, tillsammans med ett modernt enkelcellssekvenseringsdataset som profilerar tusentals enskilda celler. De kartlade först huvudcelltyperna i tandköttsvävnaden—såsom immunceller, blodkärlsceller och fibroblaster—och bekräftade att fibroblastantalet och dess aktivitet var högre i sjuk vävnad. Därefter sökte de efter gener som både förändrats vid parodontit och specifikt kopplats till fibroblaster. Med en statistisk metod som skärmar ner till de mest informativa dragen identifierade de sex viktiga fibroblastrelaterade gener vars kombinerade aktivitetsmönster med hög tillförlitlighet skiljde parodontit från frisk vävnad över flera patientgrupper.
Riskmönster och immunsystemets ”personligheter” vid tandköttssjukdom
Med dessa sex gener byggde forskarna en diagnostisk modell som presterade väl för att skilja sjuk från frisk vävnad, och de översatte den till ett enkelt poängschema—kallat en nomogram—som i princip skulle kunna uppskatta en individs risk. När de grupperade patienter efter hur starkt dessa fibroblastgener uttrycktes framträdde tre distinkta former av parodontit. En form visade ett höggradigt inflammatoriskt immunsammanhang, fyllt av aggressiva T‑celler och makrofager i ”attackläge”. En andra form dominerades av celler som dämpar immunsvar, vilket antyder en mer undertryckt miljö. En tredje form låg mitt emellan, med en mer balanserad eller vilande blandning av immunceller. Dessa mönster tyder på att inte all tandköttssjukdom är densamma—och att fibroblaster bidrar till att forma dessa olika inflammations‑”personligheter”.
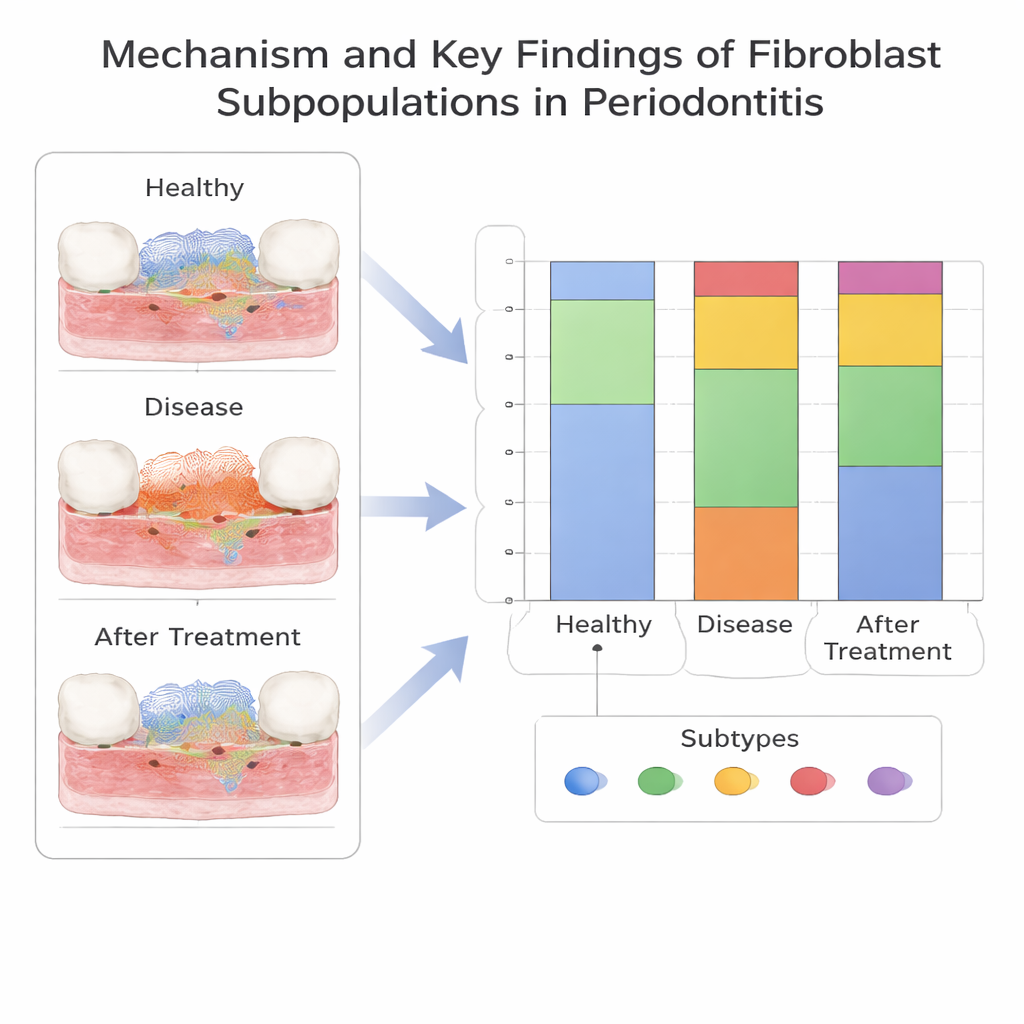
En ny proinflammatorisk fibroblastsubtyp
På enkelcellsnivå delade teamet in fibroblaster i fem subtyper baserat på deras gene uttryck. En subtyp, markerad av genen CXCL13, utmärkte sig genom att vara mycket vanligare vid parodontit än i friska tandkött. Denna CXCL13‑positiva fibroblastgrupp verkade uppträda tidigt längs en utvecklingsväg och kopplades till signaler som lockar immunceller och omformar vävnadsmatrisen—egenskaper förenliga med en stark proinflammatorisk roll. I kontrast var en annan fibroblastsubtyp rikligare i frisk vävnad och kan hjälpa till att hålla tandköttsmiljön stabil. Författarna bekräftade i patientprover att vissa fibroblastrelaterade gener, särskilt SELL, och de CXCL13‑positiva fibroblasterna själva, verkligen var högre i sjuk vävnad, vilket stärker de beräkningsmässiga fynden.
Vad detta innebär för framtida tandvård
Enkelt uttryckt visar studien att vissa fibroblaster i ditt tandkött beter sig som accelererande faktorer för inflammation, medan andra kan fungera mer som bromsar eller reparationslag. Genom att identifiera precisa genmarkörer och en distinkt proinflammatorisk fibroblastgrupp öppnar arbetet för mer träffsäkra tester som kan upptäcka parodontit tidigare och mer tillförlitligt. Det antyder också att framtida behandlingar kan rikta in sig på dessa specifika fibroblastdrivna vägar—att dämpa skadliga subgrupper som CXCL13‑positiva fibroblaster eller stärka skyddande sådana—för att bättre kontrollera guminflammation och möjligen minska dess påverkan på hela kroppen.
Citering: Huang, M., Lin, Y., Wu, Z. et al. Identification and characterization of fibroblast-related biomarkers and pro-inflammatory subpopulations in periodontitis by integrated transcriptomic and single-cell analysis. Sci Rep 16, 6223 (2026). https://doi.org/10.1038/s41598-026-37385-2
Nyckelord: parodontit, fibroblaster, guminflammation, single-cell RNA-sekvensering, biomarkörer