Clear Sky Science · sv
Effektiv apoptos via dubbelsträngsbrott i DNA hos humana epitelceller inducerat av icke-termisk effekt av högfälts bredbandiga terahertzvågor
Ny syn på att döda cancerceller
Cancerbehandlingar balanserar ofta på en knivsegg: de måste förstöra tumörceller utan att allvarligt skada frisk vävnad eller immunsystemet. Denna studie undersöker ett ovanligt verktyg för uppgiften — intensiva terahertz (THz)-vågor, en typ av osynligt ljus mellan mikrovågor och infrarött. Forskarna visar att noggrant stämda, högfälts THz-pulser kan få cancerceller att begå ”självmord” på ett kontrollerat sätt, utan att värma upp vävnaden eller orsaka den stökiga celldöd som leder till inflammation.
Därför spelar skonsam celldöd roll
Många vanliga cancerbehandlingar tvingar celler mot döden, men gör det ofta med oönskade följder. Läkemedel och biologiska medel kan förlora effekt när tumörer utvecklar resistens, och de kan försvaga immunsystemet. Fysiska metoder som röntgen, radioaktivitet eller värmebaserad ablation kan skada omgivande frisk vävnad och orsaka nekros — en våldsam form av celldöd som väcker inflammation och smärta. En metod som istället driver apoptos, en ordnad självdödsprocess där cellerna tyst demonterar sig själva, skulle kunna erbjuda ett mycket mindre traumatiskt sätt att krympa tumörer, särskilt de som ligger nära huden.
Terahertzvågor möter bröstcancerceller
Gruppen fokuserade på humana bröstcancerceller (MCF‑7), en typ av epitelcell som ofta används i laboratoriestudier. De exponerade dessa celler för mycket starka, bredbandiga pulserade THz-vågor i upp till fyra timmar samtidigt som de hölls vid normal kroppstemperatur. Fältstyrkorna nådde flera miljoner volt per centimeter, långt över vad som finns i vardagliga apparater. Under dessa förhållanden ökade andelen celler som genomgick apoptos stadigt med exponeringstiden. Vid den högsta testade THz-intensiteten gick nästan 99 % av cancercellerna in i apoptos, medan färre än 1 % dog genom nekros. Denna stora, rena våg av programmerad celldöd tyder på att THz-pulserna gör mer än att bara värma cellerna.
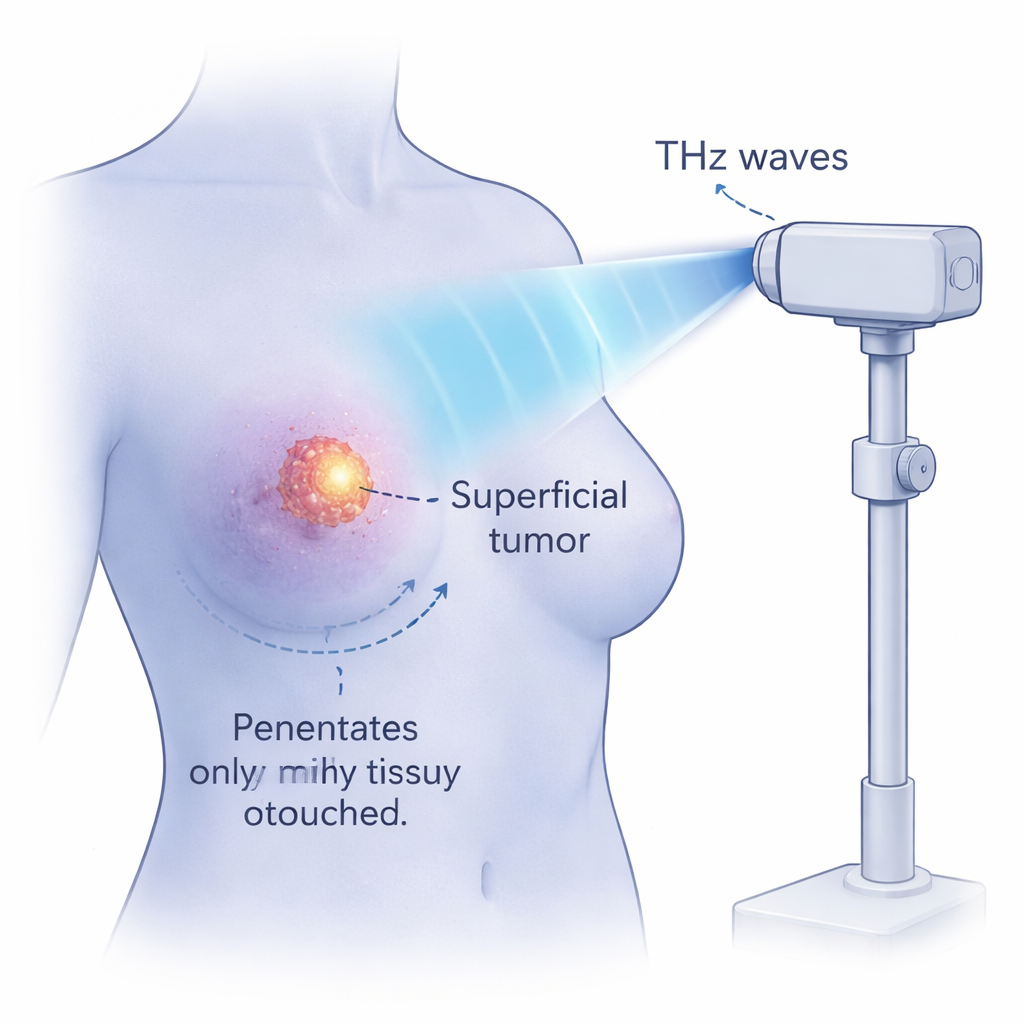
Icke-uppvärmnings‑effekter och säkra temperaturgränser
Eftersom vatten starkt absorberar THz-strålning är den uppenbara oron oavsiktlig uppvärmning. Forskarna använde termisk avbildning för att följa temperaturförändringar under bestrålning. Även efter fyra timmar vid måttlig intensitet värmdes cancercellerna endast med cirka 3 °C, och nekrosen hölls under 4 %. Separata kontrollförsök där celler enbart värmdes i fyra timmar visade att temperaturer under 41 °C gav nästan ingen död, medan en skarp ökning i nekros inträffade över 43 °C. Även vid sina mest intensiva THz-inställningar höll forskarna celltemperaturen vid eller under denna 43 °C-gräns och såg ändå nästan total apoptos med minimal nekros. Genom att sänka pulsernas repetitionsfrekvens visade de att temperaturen kan hållas i schack samtidigt som starka anti-tumöreffekter bevaras, vilket understryker att en icke-termisk mekanism är i spel.
Skakande DNA och aktivering av dödsgener
För att hitta den mekanismen tittade gruppen in i cellerna. I elektronmikroskop visade THz-behandlade celler klassiska tidiga tecken på apoptos: kondenserat genetiskt material, förändrade kärnor och intakta yttre membran. Med hjälp av en fluorescerande markör kallad γ‑H2AX upptäckte de omfattande dubbelsträngsbrott i DNA — skador mycket vanligare i bestrålade celler än i obehandlade eller lätt uppvärmda kontroller. Skademönstret följde intensitetsprofilen hos THz-strålen och blev starkare mot dess centrum. Gen- och proteinanalyser visade att en uppsättning stress- och skade‑responsiva molekyler, såsom GADD45B och c‑Jun, aktiverades kraftigt, medan välkända aktörer i traditionella celldödsrutiner, inklusive p53 och många kaspaser, inte förändrades mycket. Författarna föreslår att intensiva THz-fält kan driva våldsamma vibrerande ”resonanser” i DNA, fysiskt påfresta och bryta dubbelspiralen och därigenom utlösa en distinkt apoptosväg som är oberoende av p53 och kaspaser.
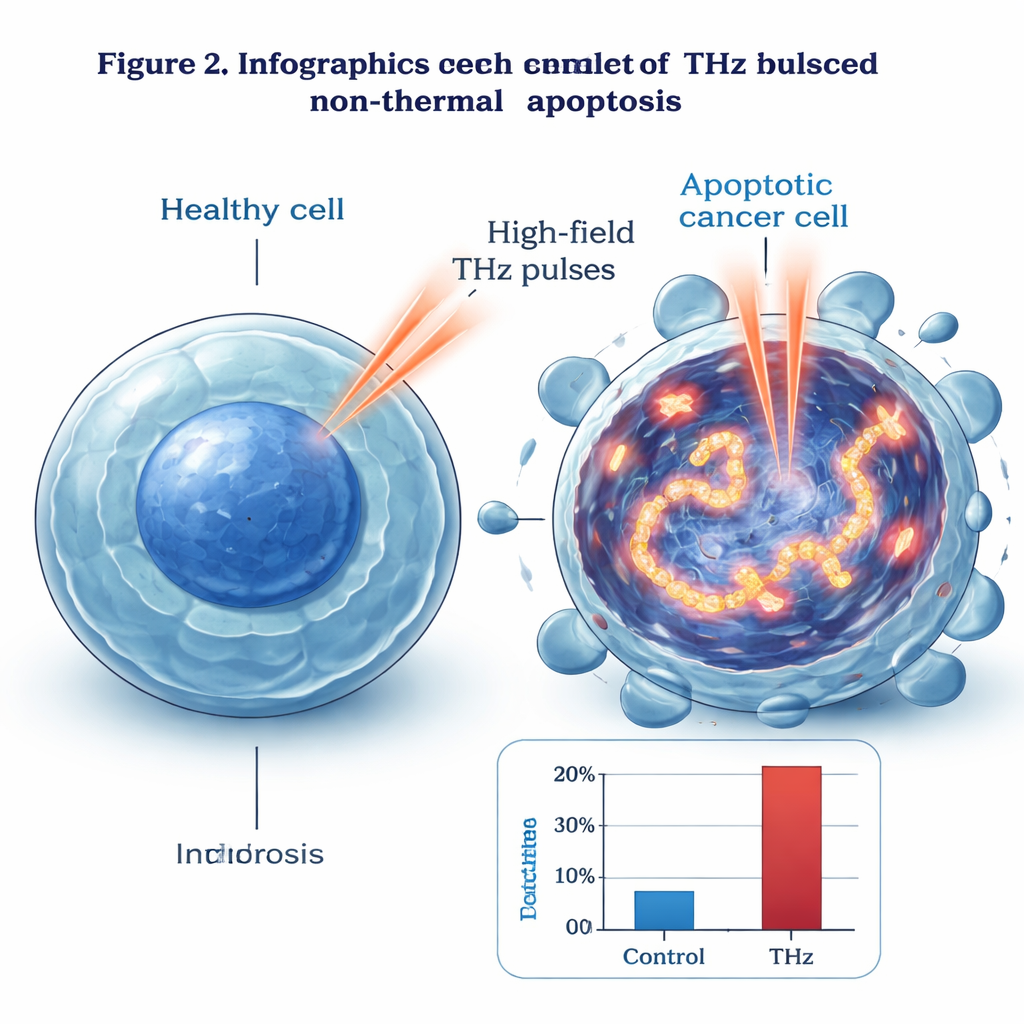
Från odlingsskål till framtida terapier
Även om dessa experiment utfördes i cellkulturer antyder de en ny typ av fysisk cancerterapi. Högfälts THz‑vågor verkar kunna penetrera flera millimeter in i fuktig vävnad — tillräckligt för att nå ytliga tumörer — men tappar snabbt i styrka, vilket potentiellt kan skona djupare organ. Eftersom effekten huvudsakligen är icke-termisk skulle den i princip kunna döda cancerceller lager för lager utan att bränna omgivande vävnad eller framkalla kraftig inflammation. Mycket arbete återstår: den föreslagna DNA‑"resonans"-mekanismen måste bekräftas, säkerheten för normala celler kräver noggrann testning, och djur- samt kliniska studier behövs. Ändå öppnar denna forskning dörren för idén att noggrant konstruerade ljuspulser, stämda till biomolekylernas naturliga rörelser, en dag kan erbjuda ett precist och relativt skonsamt sätt att ablatera vissa cancerformer.
Citering: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
Nyckelord: terahertz cancerterapi, icke-termisk apoptos, DNA dubbelsträngsbrott, bröstcancerceller, fysisk tumörablation