Clear Sky Science · sv
Generaliserade blodkärlsmodeller för magnetisk nanopartikelsstyrd onkologi: geometriska och mikrofluidiska egenskaper
Vägleda små magneter genom kroppen
Föreställ dig att kunna dra cancerläkemedel direkt in i en tumör med hjälp av en magnet och därigenom skona resten av kroppen från hårda biverkningar. Denna studie undersöker hur små magnetiska partiklar rör sig genom blodkärlsliknande nätverk och ställer en bedrägligt enkel fråga: under realistiska flödesförhållanden, kan magneter faktiskt styra dessa partiklar dit läkare vill ha dem?
Varför kärlgeometri och flöde spelar roll
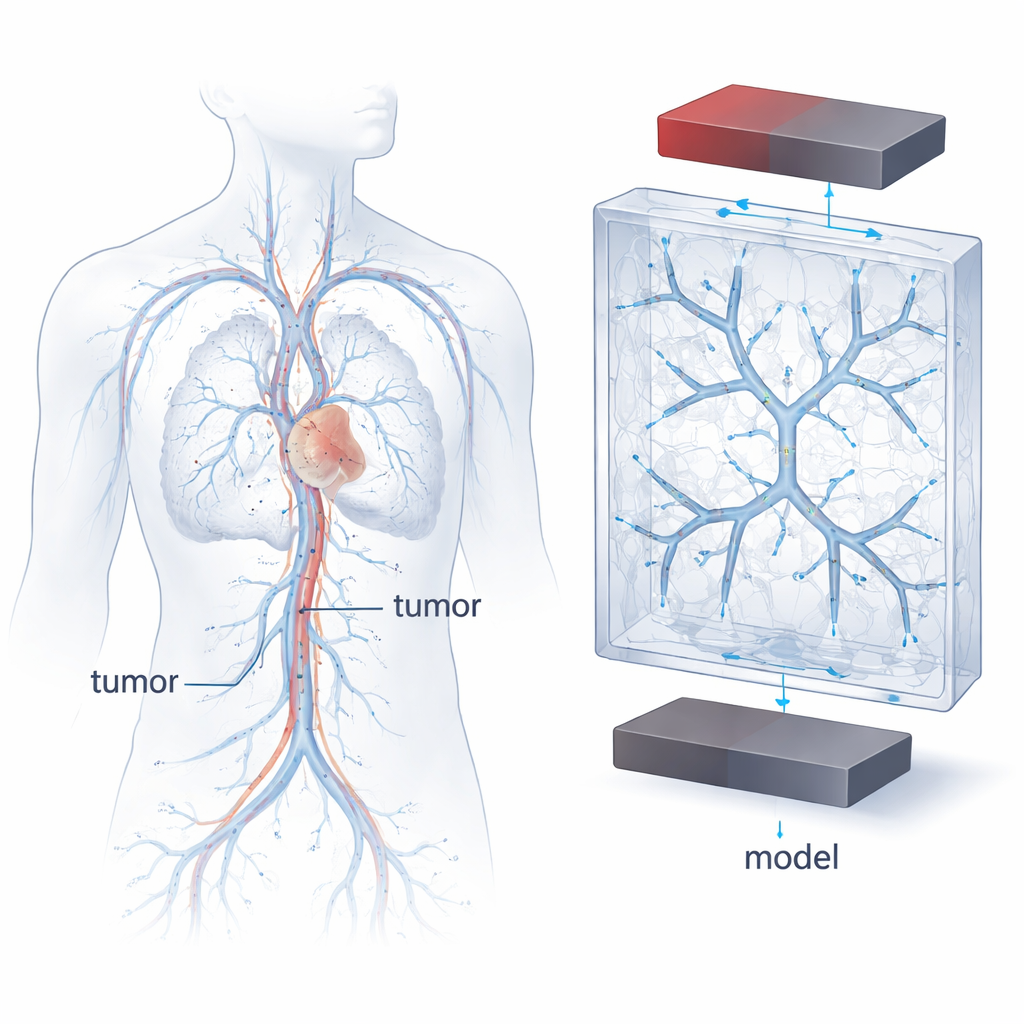
Magnetiska cancerterapier bygger på superparamagnetiska järnoxidnanopartiklar—SPIONs—som kan dras av ett magnetfält medan de transporterar läkemedel genom blodomloppet. Men blodkärl är inte enkla raka rör: de förgrenar sig, smalnar av, kröker och delar sig, och blodet ökar eller minskar hastigheten som svar. Dessa förändringar i form och hastighet påverkar hur partiklar rör sig, var de koncentreras och om de hinner nå kärlväggarna tillräckligt länge för att fästa. Verkliga patienters blodkärl är extremt varierande, vilket försvårar jämförelser mellan experiment eller förutsägelser om hur en ny terapi kommer att bete sig. Författarna gav sig därför i kast med att bygga en högt kontrollerad, upprepbar ”modellvasculatur” som ändå fångar de väsentliga dragen hos tumörförsörjande blodkärl.
Bygga idealiserade tumörblodnätverk
För att utforma dessa modellkärl använde teamet klassiska regler som beskriver hur verkliga artärer förgrenar sig. En sådan regel, Murrays lag, kopplar samman diametrarna hos föräldra- och dotterkärl i ett energieffektivt nätverk. Med kliniska mätningar från brösttumörer och dessa skalningslag genererade forskarna matematiskt förgrenande träd som efterliknar hur tumörförsörjande kärl avsmalnar mot kapillärnätet. De använde sedan högupplöst 3D-utskrift för att inbädda ihåliga kanalnätverk med två, tre eller fyra förgreningsnivåer i genomskinliga plastblock. Kanalerna följde ett symmetriskt förgreningsmönster och sträckte sig i tre dimensioner, vilket gav ett förenklat men fysiologiskt inspirerat landskap för att studera partikelrörelse.
Se magnetiska partiklar i aktion
Genom dessa utskrivna nätverk pumpade teamet vatten som ett substitut för blod, injicerade sedan SPION-haltig vätska uppströms och applicerade ett statiskt magnetfält runt modellen. Högfartsvideoinspelning gav en filmaktig dokumentation av hur de mörka partikelskyarna passerade olika grenar, medan datoranalys omvandlade ljusstyrkeförändringar till tidsupplösta signaler som speglar lokal partikelnärvaro. Genom att variera bakgrundsflödet, partikelkoncentrationen, förgreningskomplexiteten och närvaro eller frånvaro av en magnet kunde forskarna urskilja hur varje faktor formade partikelns fördelning, uppehållstid och slutliga deposition på kanalkärlväggarna.
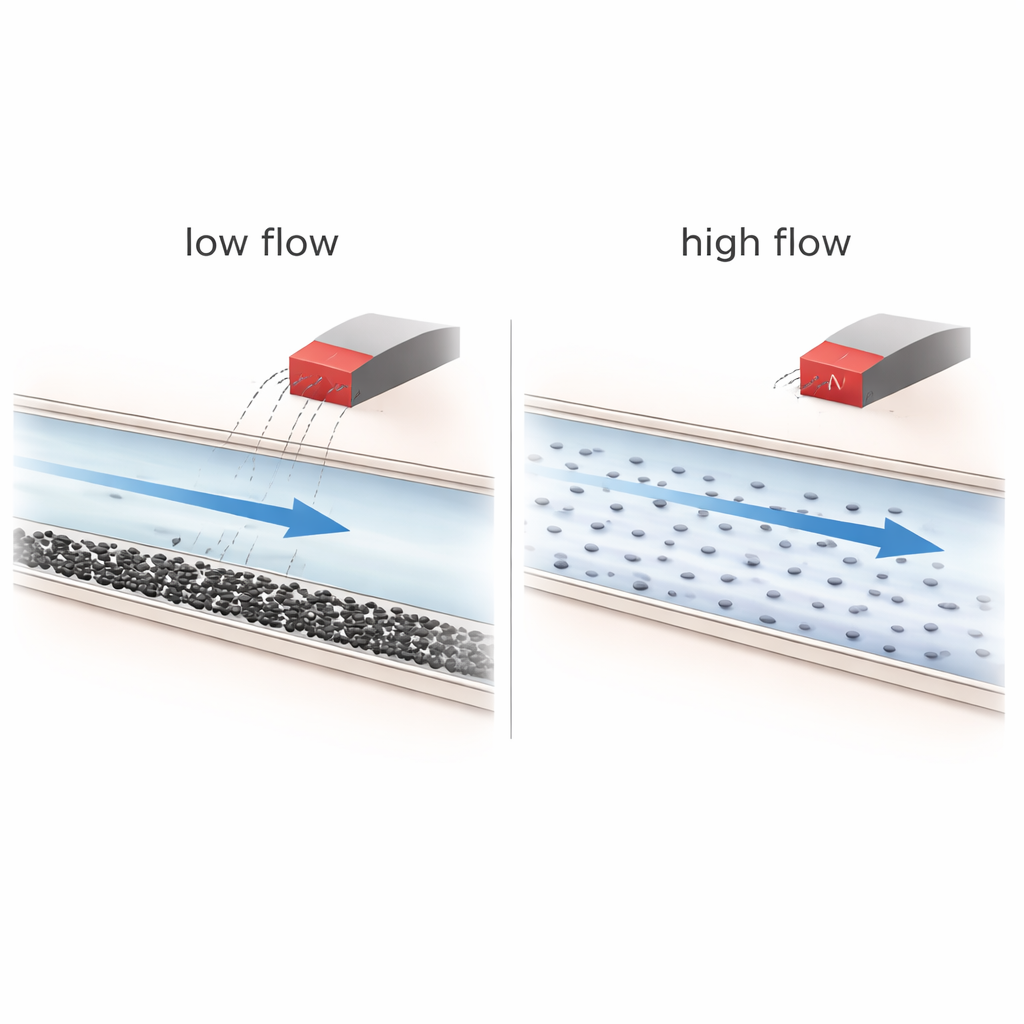
När magneter hjälper — och när de inte gör det
Experimenten visar att flödeförhållandena dominerar bilden. Vid högre flödeshastigheter blir vätskan väl blandad och nanopartiklarna färdas snabbt; under dessa förhållanden har magnetfältet nästan ingen inverkan, och partiklarna följer helt enkelt strömlinjerna genom nätverket. Vid låga flödeshastigheter däremot gör gravitation och koncentrationseffekter att partiklarna sjunker mot kanalernas botten, bildar stratifierade lager och ibland lösa kluster. I denna redan ojämna situation kan magneten knuffa fler partiklar in i vissa grenar och något förlänga deras uppehållstid, särskilt i mer komplexa, starkt förgrenade nätverk. Beräkningar visar ändå att den magnetiska kraften på en enskild 40-nanometers partikel är många storleksordningar svagare än den viskösa dragkraften från den flödande vätskan, vilket gör verklig »styrning av enstaka partiklar« fysiskt orealistisk under de testade förhållandena.
Vad detta betyder för framtida cancerbehandlingar
För en icke-specialist är huvudslutsatsen att magneter ensamma inte kan pålitligt dra fritt svävande nanopartiklar ur ett snabbflödande blodomlopp. Istället uppstår märkbara magnetiska effekter bara när partiklarna redan har bromsat in, lagt sig till ro eller klustrat sig — situationer som effektivt förstärker deras magnetiska respons. De generaliserade, 3D-utskrivna kärlmodellerna som presenteras här ger ett standardiserat sätt att utforska sådana effekter över olika nätverksgeometrier och flödesregimer. För framtida magnetisk läkemedelsstyrning antyder arbetet att framgångsrika strategier sannolikt behöver utnyttja kollektiva beteenden—såsom kontrollerad aggregering eller bärare—snarare än att förlita sig på att styra isolerade nanopartiklar genom stora, snabbt perfunderade kärl.
Citering: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
Nyckelord: magnetisk läkemedelsstyrning, nanopartiklar, tumörvasculatur, mikrofluidiska modeller, läkemedelsleverans