Clear Sky Science · sv
En tri-omisk och maskininlärningsbaserad ramverk identifierar prognostiska biomarkörer och metabola signaturer vid sepsis
Varför detta spelar roll för personer med allvarliga infektioner
Sepsis är en livshotande reaktion på infektion som kan få immunsystemet att gå på övervarv och leda till organsvikt. Läkare vet att tidig upptäckt av sepsis och individanpassad behandling kan rädda liv, men dagens blodtester är grova verktyg: de säger ofta lite om vem som kommer att bli bättre och vem som löper störst risk. I denna studie används en kraftfull kombination av tre typer av molekylära mätningar och modern maskininlärning för att leta efter mer precisa varningssignaler i blodet hos sepsispatienter.
Att betrakta blod genom tre olika linser
I stället för att fokusera på en enda typ av molekyl profilerade forskarna samma patienter på tre sätt samtidigt. De mätte vilka gener som var på- eller avskrivna (transkriptomik), vilka proteiner som faktiskt fanns och var aktiva (proteomik) och vilka små metabola molekyler som cirkulerade (metabolomik). De samlade blod från 21 sepsispatienter och 10 friska frivilliga och använde avancerad statistik för att se hur dessa tre lager förändrades tillsammans vid sjukdom. Denna "tri-omiska" vy hjälper till att övervinna ett centralt problem: vid sepsis kan genaktivitet och proteinnivåer bli frånkopplade, så att bara ett lager kan vara missvisande.
Att lära algoritmer att upptäcka högriskmönster
Från tusentals gener och proteiner använde teamet först en nätverksmetod för att hitta grupper som rörde sig gemensamt vid sepsis. De korsgranskade sedan dessa grupper med proteiner som tydligt skiljde patienter från friska kontroller och landade i 32 starka kandidater. För att ytterligare begränsa listan vände de sig till maskininlärning och använde två kompletterande algoritmer för att skala bort svagare signaler och behålla endast de mest informativa. När de testade hur dessa återstående gener relaterade till överlevnad i en stor offentlig sepsisdatamängd, framträdde två gener: TPR och ERN1. Patienter med högre TPR-nivåer tenderade att överleva längre, medan högre ERN1 förknippades med sämre utfall.
Att koppla immunceller och störd metabolism
Studien stannade inte vid gener och proteiner. Genom att skanna tusentals metaboliter i patientblod fann forskarna 136 små molekyler som följde TPR och ERN1 tätt. Många tillhörde vägar som hanterar cellmembranfetter och fettsyror, vilka är centrala för hur immunceller signalerar och hur inflammation sprids. Samtidigt visade en enkelcellsanalys — som undersöker individuella immunceller i blodet i stället för att blanda dem — att TPR och ERN1 är särskilt aktiva i monocyter, makrofager och natural killer‑celler. Tillsammans tyder dessa resultat på att de två markörerna sitter i korsningen mellan kroppens infektion‑bekämpande celler och hur dessa celler använder och omformar fetter och energi under sepsis.
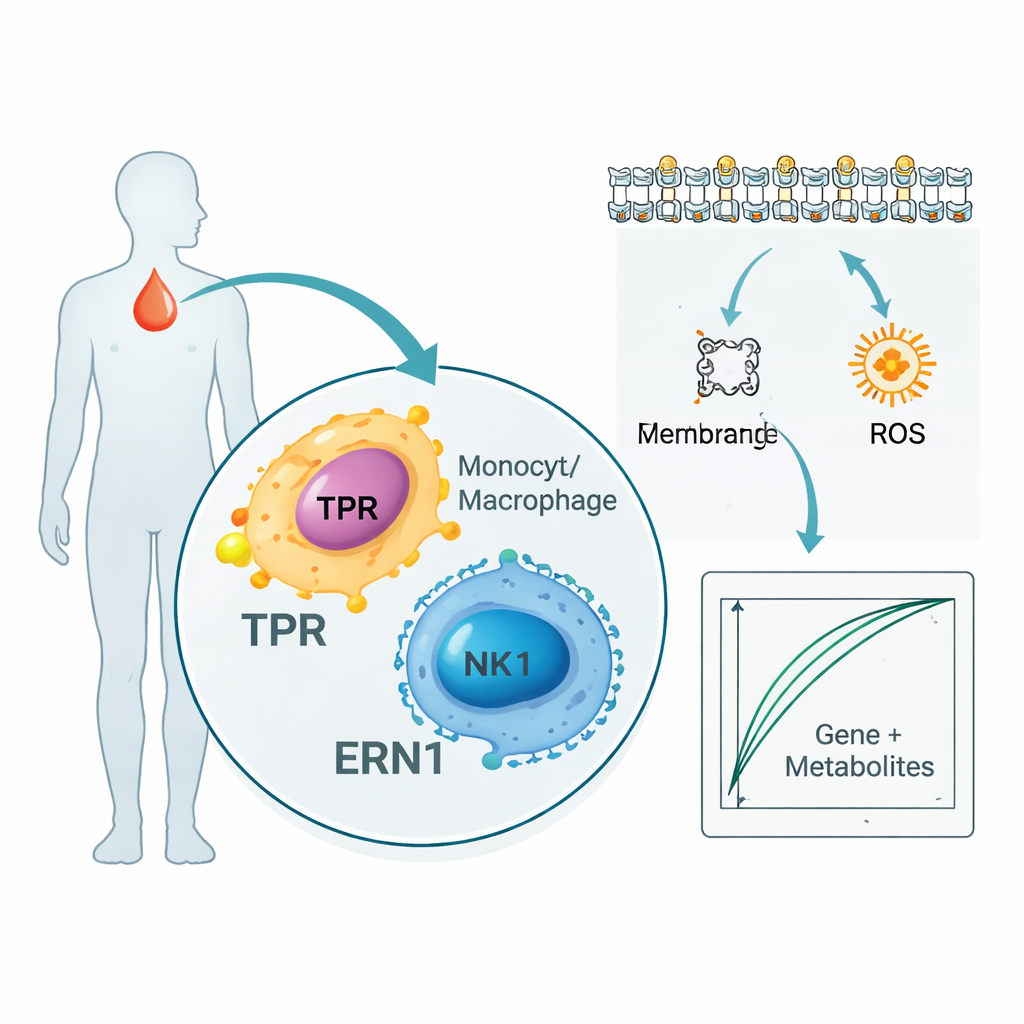
Att bygga ett proof‑of‑concept blodtest
För att undersöka hur dessa upptäckter kan översättas till praktik kombinerade författarna de två generna med fem av de mest informativa metaboliterna för att träna enkla datormodeller som skilde sepsispatienter från friska personer. I deras lilla interna datamängd kunde dessa kombinerade "gen‑plus‑metabolit" signaturer nästan perfekt avgöra vem som hade sepsis. Forskarna kontrollerade också stora offentliga databaser som kopplar blodproteiner till sjukdomsrisk i tiotusentals människor och fann att TPR‑ och ERN1‑proteinnivåer konsekvent var förknippade med sepsisrelaterade tillstånd, vilket ger ytterligare stöd. Författarna betonar dock att dessa modeller är tidiga verktyg avsedda att generera hypoteser, inte färdiga sängkantstester.
Växtbaserade föreningar som tidiga ledtrådar, inte botemedel
I ett slutsteg undersökte teamet om några naturliga molekyler kunde påverka TPR eller ERN1. De sökte i en specialiserad databas med nästan 500 renade föreningar från traditionella kinesiska läkemedel, var och en med sin egen genaktivitetsprofil. Flera föreningar verkade starkt höja eller sänka dessa två gener i labbodlade celler, vilket antyder att de en dag kan hjälpa forskare att utforska sepsisbiologin eller designa nya läkemedel. Dessa fynd bygger dock endast på datorbasad matchning: de visar inte att någon av dessa substanser är säkra eller effektiva för personer med sepsis.
Vad detta arbete egentligen berättar för oss
Denna studie erbjuder en detaljerad karta snarare än en färdig lösning. Genom att väva samman tre molekylära lager, enkelcellsdata och maskininlärning lyfter författarna fram TPR och ERN1 — och deras kopplade metabola förändringar — som lovande vägvisare för hur immunsystemet och metabolismen blir obalanserade vid sepsis. För en lekmannaläsare är huvudbudskapet att sepsis inte är en enhetlig sjukdom utan ett skiftande mönster av immun‑ och metaboliska tillstånd, och att smartare blodtester en dag kan hjälpa läkare att se vilket tillstånd en patient befinner sig i och anpassa behandlingen därefter. Innan det kan ske måste dessa tidiga signaler testas och bekräftas i mycket större, mångfaldiga patientgrupper och i laboratorieexperiment som kan bevisa orsak och verkan.
Citering: Li, X., Ke, G., Hu, Y. et al. A tri-omics and machine learning framework identifies prognostic biomarkers and metabolic signatures in sepsis. Sci Rep 16, 6648 (2026). https://doi.org/10.1038/s41598-026-37342-z
Nyckelord: sepsisbiomarkörer, mult-omik, maskininlärning inom medicin, immunmetabolism, precisionsdiagnostik