Clear Sky Science · sv
Att rikta in sig på Akt–EphA2‑axeln och cell–cell‑adhesion ökar anoikis‑känsligheten i cancerceller
Varför fritt flytande cancerceller spelar roll
När cancerceller lossnar från en tumör och färdas genom blodet bör de normalt dö eftersom de förlorar kontakten med den omgivande vävnaden. Detta inbyggda säkerhetssystem, kallat detachment‑induced cell death, hjälper till att förhindra att celler växer där de inte hör hemma. Metastatiska cancerceller lär sig dock ofta att ignorera denna signal och förbli vid liv medan de flyter, vilket gör det lättare för dem att anlägga nya tumörer. Denna studie ställer en bedrägligt enkel fråga: om vi återställer ett avgörande mekaniskt "känselintryck" i aggressiva bröstcancerceller, kan vi tvinga dessa kringströvande celler att dö, och om inte, vilka reservknep använder de för att överleva?
Att återväcka en förlorad känsel för beröring
Celller testar ständigt hur styv deras omgivning är genom att dra i de strukturer som förankrar dem. I frisk vävnad tenderar förlorad kontakt eller landning på en mycket mjuk yta att utlösa självdestruktion. Proteinet Tropomyosin 2.1 (Tpm2.1) är en viktig del av denna interna spänningsmaskin och saknas ofta eller är minskat i cancerceller. Forskarna använde en välstuderad metastatisk bröstcancellinje och konstruerade den för att producera mer Tpm2.1, vilket återställde stora delar av rigiditetssinnet. När dessa modifierade celler tvingades växa i särskilda non‑stick‑skålar som hindrar dem från att fästa, genomgick de mer celldöd, växte långsammare och rörde sig mindre än omodifierade cancerceller. Ändå var ungefär 70 % av Tpm2.1‑uttryckande cellerna fortfarande vid liv efter flera dagar i suspension, vilket tyder på att återupplivandet av deras känsel för beröring inte ensamt löser problemet fullt ut.
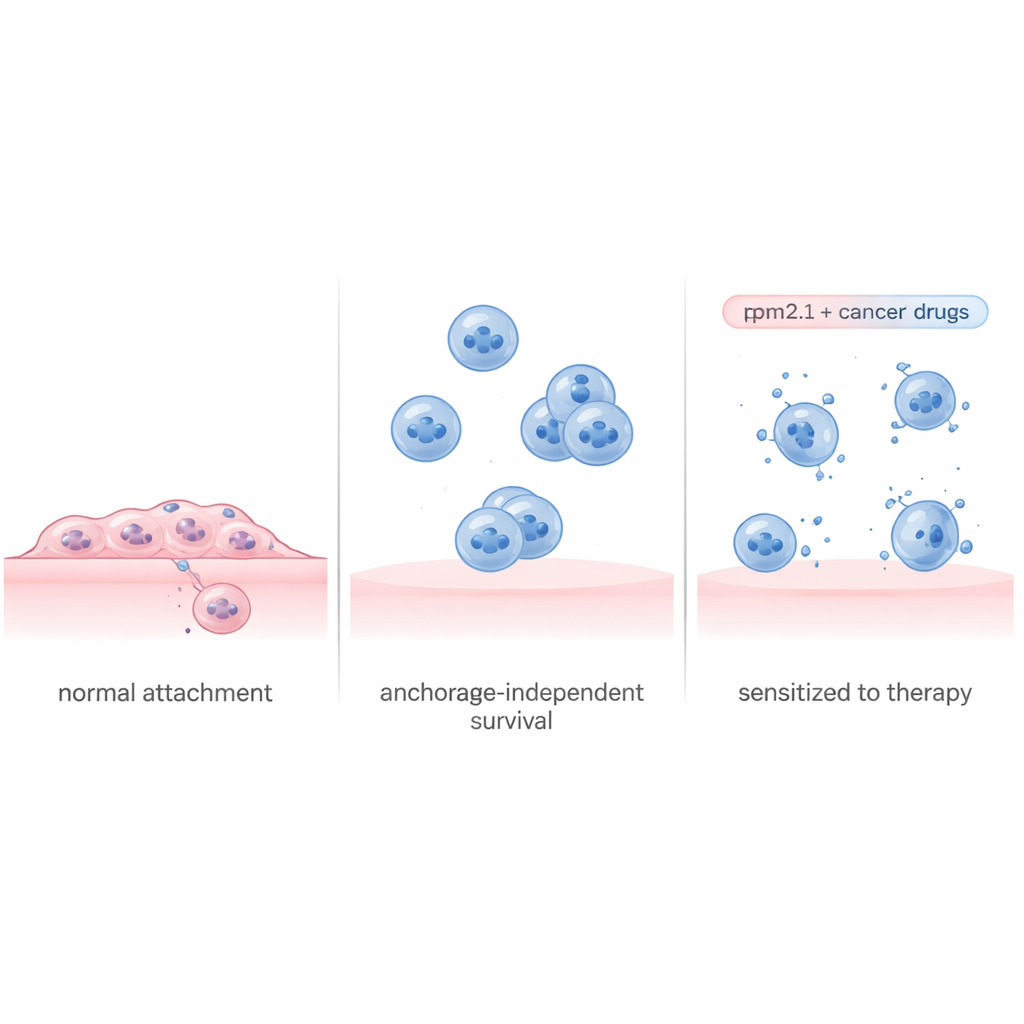
Att läsa cancercellernas överlevnadsplan
För att förstå varför vissa celler dog medan andra överlevde separerade teamet de flytande Tpm2.1‑uttryckande cellerna i två grupper: de som visade tidiga tecken på celldöd och de som verkade friska. De mätte sedan vilka gener som var aktiva eller avstängda i varje grupp över fyra dagar. De döende cellerna visade en bred nedstängning av program för cell‑delning, DNA‑reparation och fäste, tillsammans med stressignaler som såg ut som en enkelriktad väg mot självdestruktion. Däremot aktiverade de överlevande cellerna en samordnad överlevnadsplan. Tidigt efter detachment slog de på inflammatoriska och immunrelaterade vägar och senare ökade de stora tillväxt‑ och överlevnadskretsar, inklusive en välkänd väg centrerad på proteinet Akt. Samtidigt ökade de starkt gener som hjälper celler att fästa vid varandra, vilket gjorde det möjligt för dem att bilda skyddande kluster även utan att hålla i den omgivande matrixen.
Styrka i antal: hur cellkluster motstår död
Eftersom genundersökningarna pekade mot ökad cell–cell‑adhesion testade forskarna om enkel trängsel kunde hjälpa celler att överleva i suspension. När Tpm2.1‑uttryckande celler odlades i hög densitet, där klustring var enkel, dog betydligt färre celler än när de hölls glesa. Ett adhesionsmolekyl, ICAM1, stack ut som särskilt uppreglerad i de överlevande cellerna och är redan känt för att hjälpa kluster av cirkulerande tumörceller att bildas och fästa i avlägsna vävnader. Att blockera ICAM1 med en småmolekylär inhibitor gjorde att fler av de Tpm2.1‑uttryckande cellerna dog i suspension, medan det hade liten effekt på vanliga odlade, fästa kulturer. Dessa fynd stöder idén att när deras interna mekanik delvis återställts kan cancerceller fortfarande undkomma döden genom att bokstavligen hålla fast vid varandra istället för vid sin omgivning.
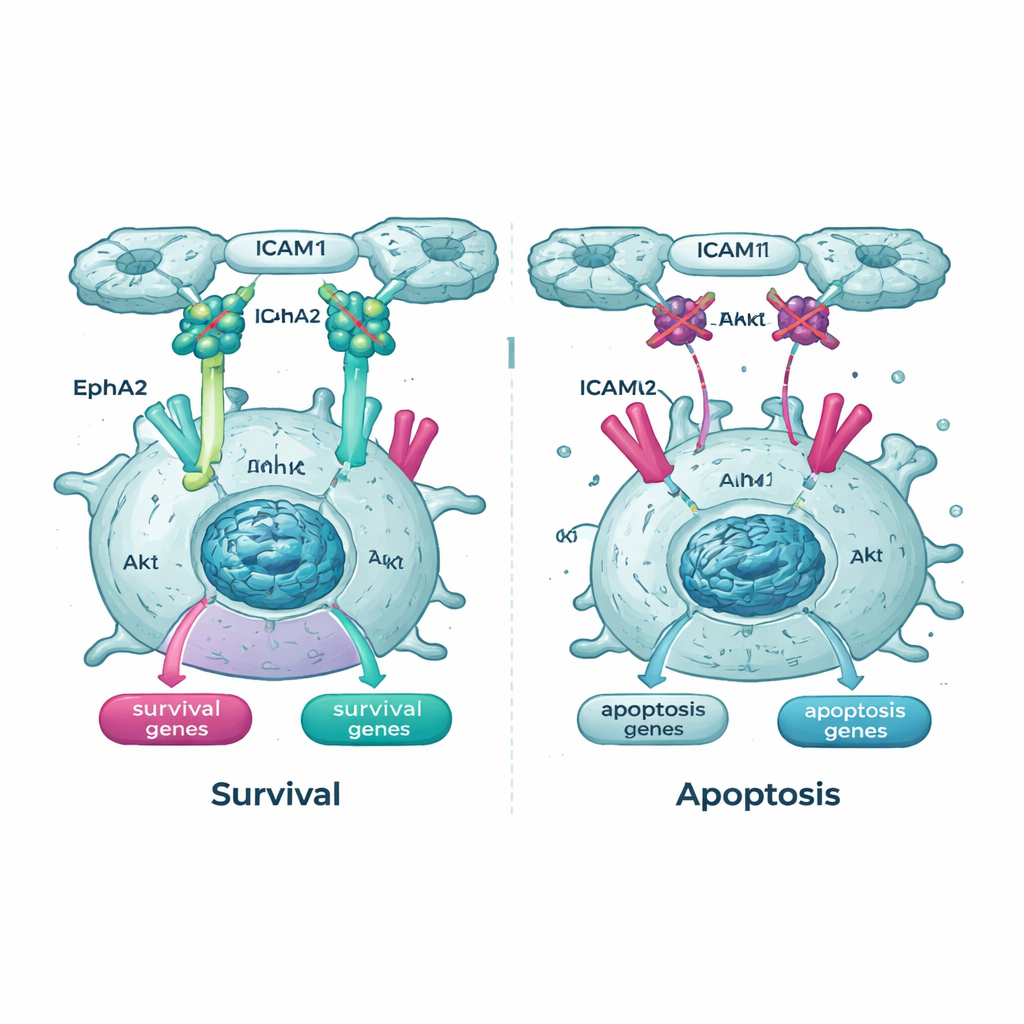
Att kapa viktiga livlinor inne i cellen
De genetiska undersökningarna framhävde också Akt‑vägen och en av dess partner, en receptor kallad EphA2, som viktiga livlinor för suspenderade cancerceller. I Tpm2.1‑uttryckande celler var den aktiva, fosforylerade formen av Akt lägre i suspension än i kontrollceller, och EphA2‑nivåer och aktivitet var också reducerade. När teamet behandlade cellerna med läkemedel som blockerar Akt eller EphA2 blev både normala och Tpm2.1‑uttryckande cancerceller mycket mer benägna att dö i suspension. Noterbart var att cellerna med återställd rigiditetssinnlighet var särskilt känsliga för dessa läkemedel över tid, vilket antyder att när deras mekaniska säkerhetskontroller delvis återaktiverats förlitar de sig mer på de kvarvarande överlevnadssignalerna.
Att förvandla ett primat till en dödlig svaghet
För en icke‑specialist är huvudbudskapet att åtgärdandet av en trasig säkerhetsbrytare i cancerceller — deras förmåga att känna och reagera på förlorad kontakt — är nödvändigt men inte tillräckligt för att få dem att självdö. De celler som överlever gör det genom att gå ihop och omdirigera sitt interna ledningsnät via alternativa tillväxt‑ och överlevnadsvägar. Detta arbete visar att återställandet av rigiditetssinnet med Tpm2.1 förflyttar metastatiska bröstcancerceller till ett "primat" tillstånd där de är närmare döden men inte ännu förpliktade. Genom att därefter blockera Akt–EphA2‑vägen och störa cell–cell‑adhesion via ICAM1 kan forskare driva dessa primade celler över kanten och kraftigt öka detachment‑induced cell death. I praktiska termer skisserar studien en strategi för framtida kombinationsbehandlingar som syftar till att utplåna fritt flytande tumörceller innan de kan anlägga nya metastaser.
Citering: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
Nyckelord: bröstcancer‑metastasering, celladhesion, anoikis, Akt‑signalering, rigiditetssinne