Clear Sky Science · sv
Påverkan av den definierade Oligo‑MM12‑mikrobiotan på tarmkolonisation och spridning av Listeria monocytogenes
Varför bakterierna i tarmen spelar roll
Många känner till Listeria monocytogenes som en farlig matburen bakterie kopplad till kontaminerade färdigätna livsmedel och svåra sjukdomsfall hos utsatta individer. Mindre uppenbart är att huruvida denna bakterie får fäste i kroppen inte bara beror på vårt immunsystem, utan också på det livliga samhälle av mikrober som redan lever i tarmarna. Denna studie använder särskilt utformade musmodeller och en miniatyriserad ”artificiell kolon” för att ställa en enkel men viktig fråga: hur påverkar tarmmikrobiomets komplexitet Listerias förmåga att kolonisera tarmen och sprida sig i kroppen?
Berättelsen om två mikrobiella grannskap
För att tackla frågan jämförde forskarna två sorters möss. Den ena gruppen, kallad SPF‑möss, bar på en rik, naturlig blandning av tarmbakterier liknande den som återfinns hos många laboratoriedjur. Den andra gruppen, Oligo‑MM12‑möss, hyste ett mycket enklare samhälle bestående av endast 12 välkarakteriserade bakteriestammar. Eftersom varje medlem i detta samhälle är känd och stabil över generationer, är Oligo‑MM12‑mössen ett kraftfullt verktyg för att dissekera vilka mikrober som hjälper till att blockera inkräktare och vilka som kan lämna luckor i vårt försvar. Genom att kontrastera dessa möss kunde teamet pröva hur ett tätt, diversifierat tarmekosystem skiljer sig från ett strömlinjeformat, minimalistiskt sådant i hur det hanterar en infektiös utmaning.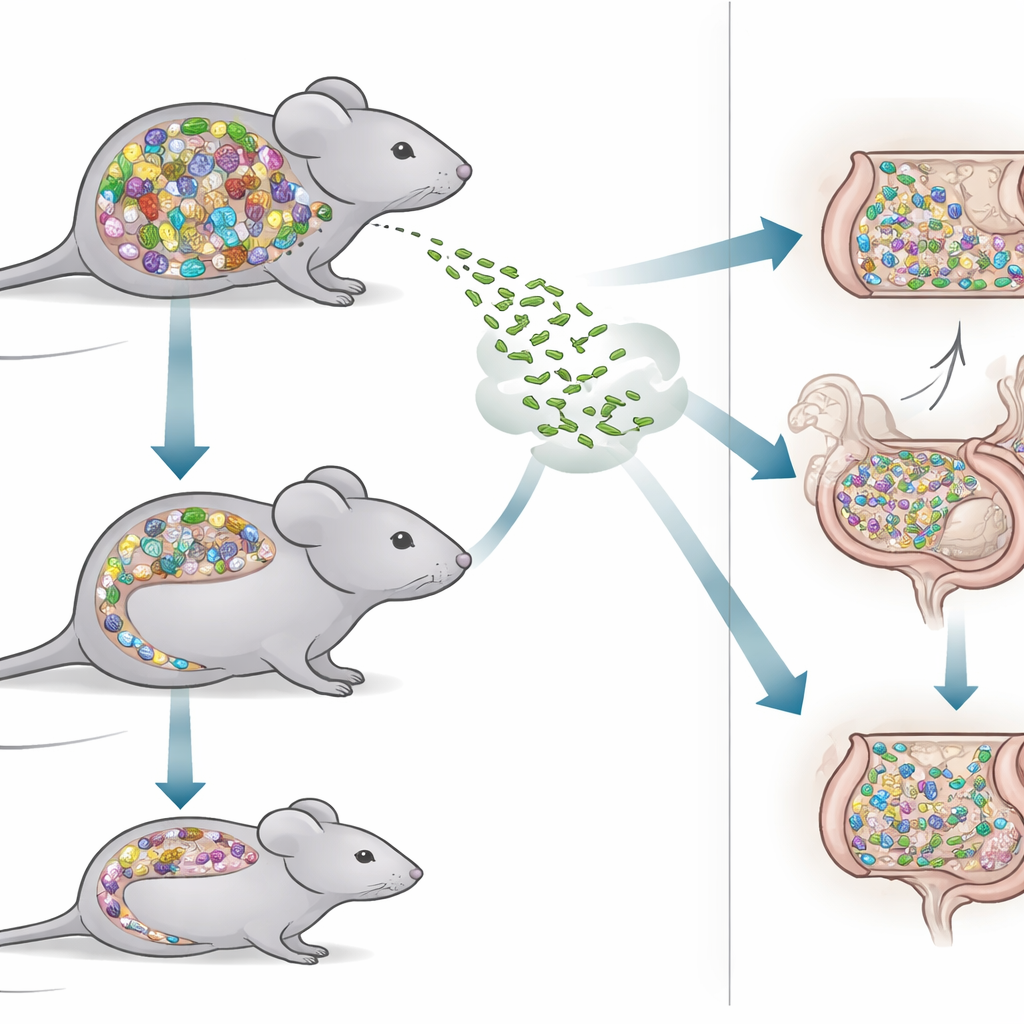
Följa Listeria genom tarmen och vidare
Forskarna infekterade båda musgrupperna med samma orala dos Listeria och spårade hur många bakterier som dök upp i avföring och inre organ under tre dagar. Intressant nog verkade det enklare Oligo‑MM12‑samhället initialt bättre på att hålla Listeria i schack: den första dagen efter infektion utsöndrade dessa möss färre Listeria‑celler i sina avföringsprover än SPF‑mössen. Denna tidiga fördel mattades dock ut. På den tredje dagen utsöndrade Oligo‑MM12‑mössen mer Listeria, medan SPF‑mössen stadigt pressat nivåerna nedåt. Trots dessa tydliga skillnader i tarmen var antalen Listeria i inre organ såsom lever, mjälte och lymfkörtlar likartade mellan de två musmodellerna, vilket tyder på att när Listeria väl når djupare vävnader spelar mikrobiomets komplexitet en mindre roll.
Simulera kolon i en kontrollerad låda
För att separera effekterna av värdvävnader och immunitet från mikrobernas eget beteende körde teamet även ett ex vivo‑experiment med en enhet kallad micro‑Matrix bioreactor. De skapade avföringsslurries från varje mustyp, tillsatte dem i ett näringsrikt medium i förslutna, syrefria brunnar och introducerade Listeria i några av dessa miniatyrkulturer medan andra lämnades som kontroller. Under fem dagar mätte de Listeria‑antal och sekvenserade bakterie‑DNA för att följa hur samhällena utvecklades. I denna artificiella kolon växte Listeria till liknande nivåer oavsett om den mötte den komplexa SPF‑mikrobiotan eller det enklare Oligo‑MM12‑samhället, och dess närvaro orsakade endast måttliga skift i den övergripande samhällssammansättningen. Denna kontrast mot de levande djuren understryker hur starkt immunsystemet, tarmens slemhinna samt gall- och slemflöden formar infektionen i den verkliga tarmen.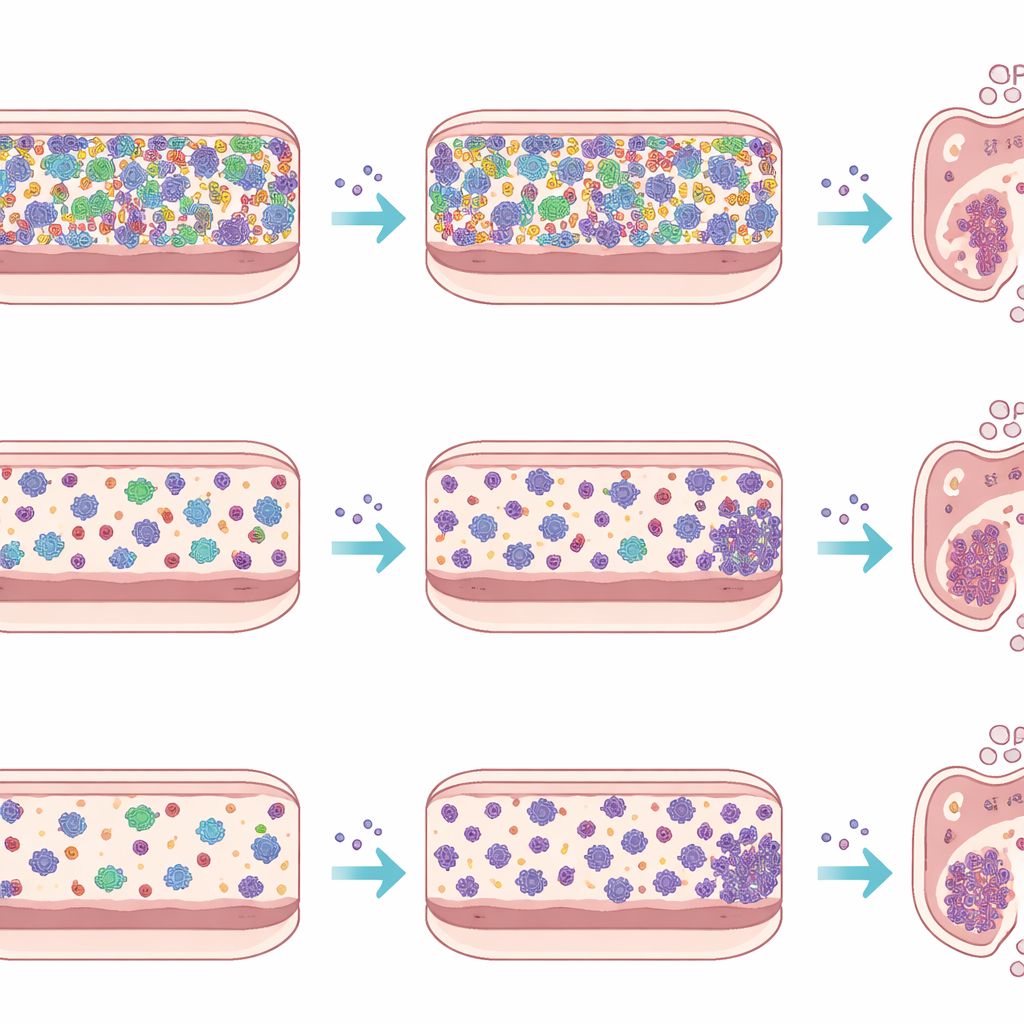
Viktiga mikrobiella vinnare, förlorare och åskådare
Genom att granska vilka bakteriegrupper som ökade eller minskade under infektionen identifierar studien kandidater som kan påverka Listerias framgång. Hos Oligo‑MM12‑mössen sjönk nivåerna av Akkermansia, en slemhinneassocierad bakterie ofta kopplad till tarmhälsa, på den andra dagen för att sedan återhämta sig kraftigt dag tre. Hos SPF‑mössen minskade flera släkten kända för att producera fördelaktiga metaboliter eller stödja barriärintegritet, såsom Blautia och Bacteroides, under infektionen, medan vissa Prevotella‑lika bakterier visade komplexa upp‑ och nedgångar som kan återspegla direkt målning av Listerias egna antimikrobiella föreningar. Ex vivo var dessa mönster i stort dämpade, vilket förstärker idén att många av de observerade skiften uppstår från trevägsinteraktioner mellan patogen, bofasta mikrober och värdmiljön snarare än från enkel mikro‑till‑mikro‑konkurrens alene.
Vad detta betyder för att skydda människor
För icke‑specialister är kärnbudskapet att inte alla till synes hälsosamma mikrobiom skyddar mot infektion på samma sätt, och att ”mer mångfald” inte alltid är bättre i varje ögonblick. Det förenklade Oligo‑MM12‑samhället gav starkt tidigt motstånd mot Listeria i tarmen, men över tid gjorde det mer intrikata SPF‑mikrobiomet ett bättre jobb med att rensa ut inkräktaren. Arbetet visar att noggrant konstruerade, lågkomplexa mikrobiota‑modeller, kombinerade med kontrollerbara ex vivo‑system, kan avslöja vilka bakteriegrupper och miljöfaktorer som är avgörande för att blockera farliga matburna patogener. I förlängningen kan sådana insikter vägleda riktade probiotika eller mikrobiom‑baserade terapier som stärker rätt mikrobiella allierade vid rätt tidpunkt för att förebygga allvarliga Listeria‑infektioner hos riskpatienter.
Citering: Cazzaniga, M., Bra, K.K., Herzog, M.K.M. et al. Impact of the defined Oligo-MM12 microbiota on intestinal colonisation and dissemination of Listeria monocytogenes. Sci Rep 16, 8434 (2026). https://doi.org/10.1038/s41598-026-37294-4
Nyckelord: Listeriainfektion, tarmmikrobiom, kolonisationsresistens, musmodell, probiotika