Clear Sky Science · sv
En ram för djupinlärningsensembler för klassificering av njurtumörer i flera undertyper med kontrastförstärkt CT
Varför det är viktigt att upptäcka njurtumörer tidigt
Njurcancer kan ligga tyst i flera år och ge få symptom tills den redan har spridit sig. Med moderna bildtekniker upptäcks många njurmassor av en slump vid undersökningar för ryggont eller andra problem. Den centrala frågan blir då: är massan farlig cancer som kräver operation, eller en ofarlig tillväxt som kan följas? Denna studie undersöker hur artificiell intelligens kan hjälpa läkare att läsa CT-bilder mer noggrant, minska onödiga operationer samtidigt som aggressiva tumörer fångas i tid.
Fem typer av njurtumörer, ett svårt beslut
Inte alla njurtumörer är likadana. Vissa, som angiomyolipom (AML) och renal onkocytom (RO), är godartade och kan aldrig hota en persons liv. Andra, samlade under njurcellscarcinom (RCC), är maligna och kan sprida sig till andra organ. Bland maligna njurcancerformer är klarcellig RCC (ccRCC) den vanligaste och mest benägna att metastasera; papillär RCC (pRCC) och kromofob RCC (chRCC) är generellt mindre aggressiva men ändå allvarliga. På vanliga bilder kan dessa undertyper dock se förvånansvärt lika ut, så läkare förlitar sig ofta på biopsi eller operation för en säker diagnos. Författarna ville undersöka om ett sofistikerat datorsystem tillförlitligt kunde skilja dessa fem tumörtyper enbart med kontrastförstärkta CT-bilder.
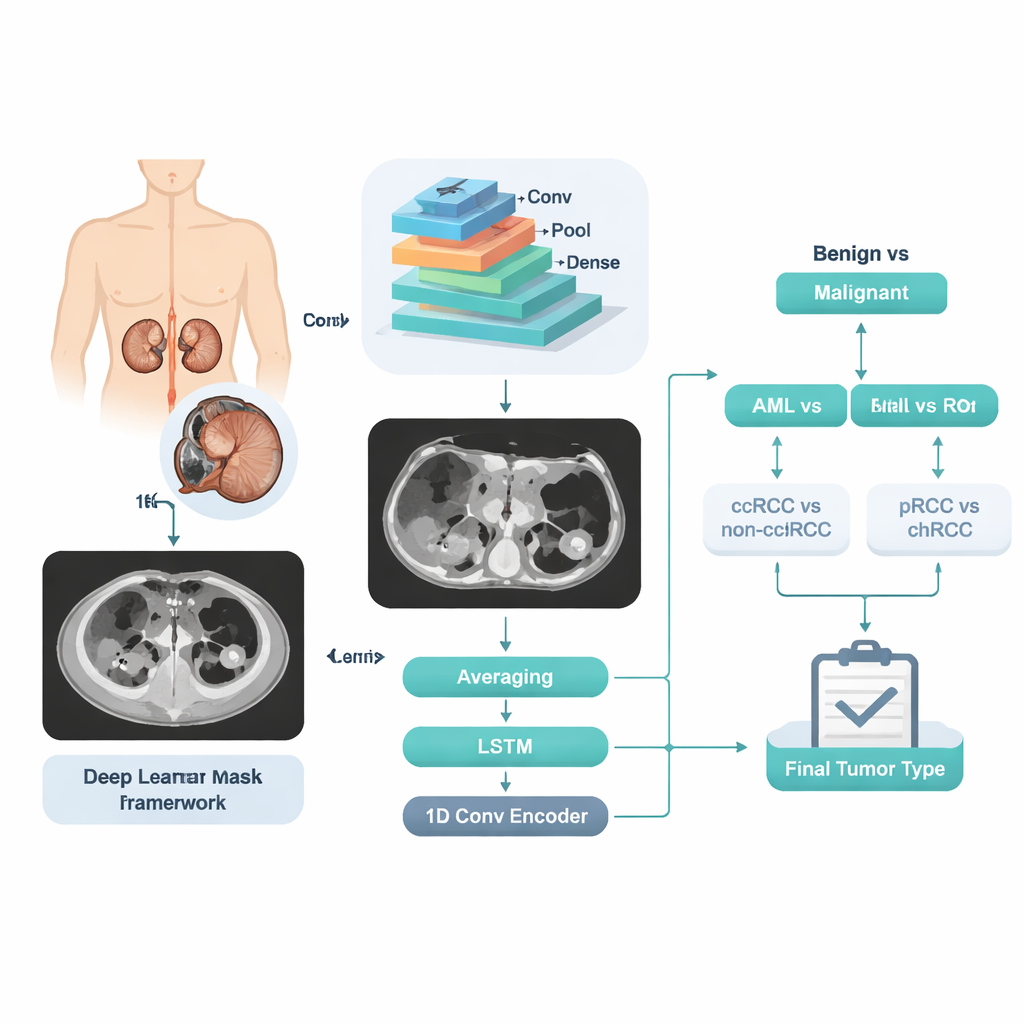
Att göra CT-bilder lärbara mönster
Teamet samlade kontrastförstärkta CT-bilder från 280 patienter vars njurtumörer redan bekräftats via vävnadsanalys. Expert-radiologer ritade noggrant ut varje tumör för hand, skiva för skiva, för att ge precisa "ground truth"-regioner som datorn kunde lära sig från. Endast en CT-fas—portalvenös fas, som vanligtvis används i rutinvård—användes, vilket betonar att metoden ska fungera med standardhospitalbildgivning. Datasatsen inkluderade slutligen fem tydligt etiketterade grupper: 84 ccRCC, 36 pRCC, 48 chRCC, 72 AML och 40 RO-fall, spridda över ett brett åldersspann och båda könen. Författarna delade sedan upp fallen i tränings-, validerings- och testset per patient, vilket säkerställde att bilder från samma individ aldrig förekom i mer än en grupp.
En steg‑för‑steg digital andra åsikt
I stället för att be datorn gå direkt från en bild till en av fem etiketter, utformade forskarna en stegvis beslutskedja som speglar en läkares resonemang. Först avgör systemet om en tumör är benign eller malign. Är den benign, skiljer ett andra beslut AML från RO. Om den är malign delar ett annat beslut upp ccRCC från de andra RCC-typerna, följt av ett sista steg som skiljer pRCC från chRCC. Vid varje steg undersöker en kraftfull bildanalysmotor, en konvolutionell neuralt nätverk, många skivor från samma patient. Dess interna numeriska ”features” bearbetas sedan på tre olika sätt: genom enkel medelvärdesbildning av skiveprediktioner, av en sekvenskänslig modell som ser hur tumören förändras över skivorna, och av ett kompakt kodningsnätverk som sammanfattar hela bildstacken till en enda signatur. De tre omdömena blandas till en slutlig sannolikhet för det skedet.
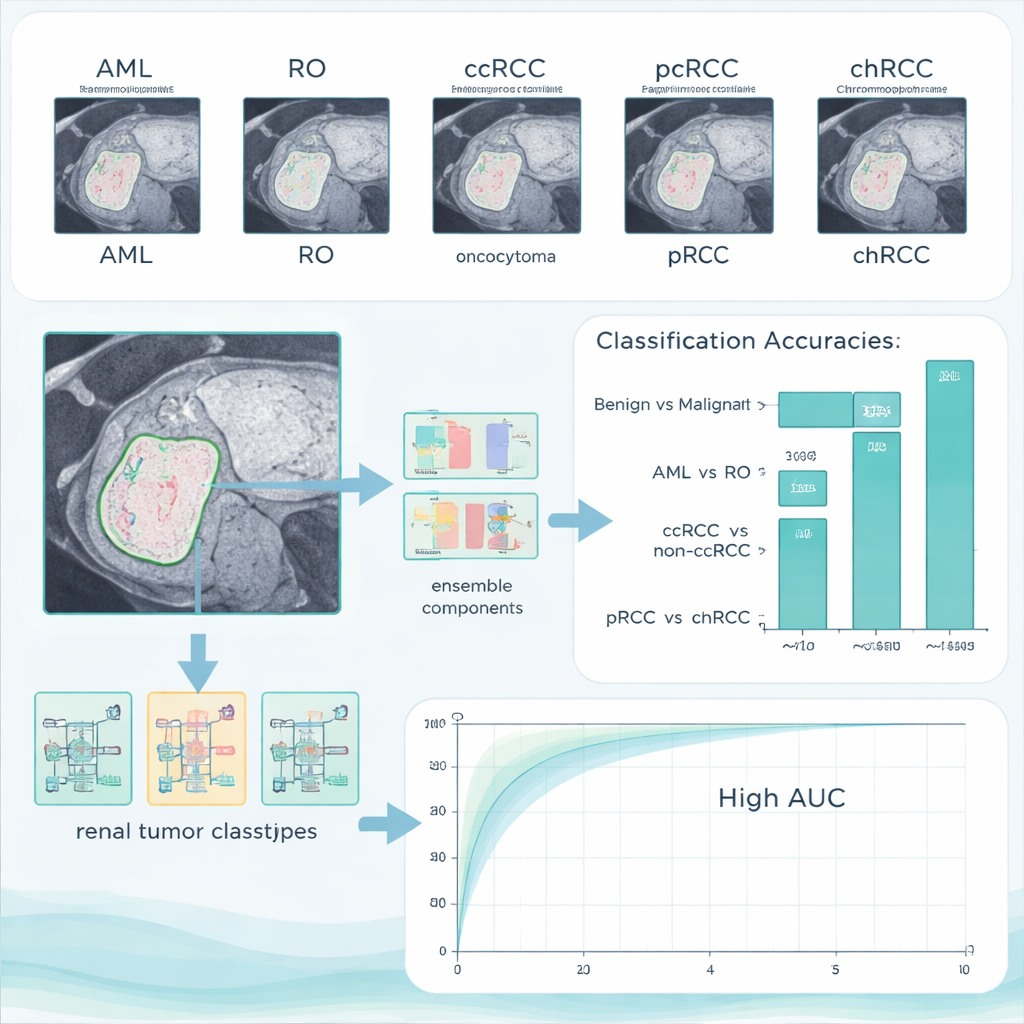
Hur väl AI-systemet presterade
På deras huvudsakliga testset uppnådde det kombinerade systemet 96,4 % noggrannhet i att skilja godartade från maligna tumörer, utan att några godartade fall felaktigt märkts som cancer och med endast ett litet antal missade cancerfall. När det ombads skilja de två godartade typerna uppnådde det perfekt 100 % noggrannhet. De mer subtila uppgifterna—att särskilja ccRCC från de andra RCC-typerna, och papillär från kromofob cancer—var svårare, men systemet klarade ändå noggrannheter över 90 %. Viktigt är att författarna också testade sin tränade modell på en helt annan publik dataset insamlad på annan plats. Prestandan förblev hög, vilket tyder på att metoden inte bara memoriserar en sjukhusbilddatabas utan kan generalisera till nya patienter och skannrar.
Vad detta kan innebära för patienter
Enkelt uttryckt visar denna forskning att en AI-"assistent" kan tolka njur-CT-bilder på ett sätt som ligger nära, och i vissa avseenden överträffar, nuvarande manuella metoder för att skilja ofarliga från farliga tumörer och identifiera viktiga cancernundertyper. Om metoden valideras vidare kan ett sådant system hjälpa radiologer att undvika onödiga biopsier och operationer för godartade tumörer samtidigt som det ger större säkerhet i tidiga behandlingsbeslut för aggressiva cancerformer. För patienter kan det innebära färre invasiva ingrepp, snabbare svar och mer personligt anpassad vård baserad på den exakta karaktären av deras njurtumör.
Citering: Abdeltawab, H., Alksas, A., Ghazal, M. et al. A deep learning ensemble framework for multi-subtype renal tumor classification using contrast-enhanced CT. Sci Rep 16, 6657 (2026). https://doi.org/10.1038/s41598-026-37283-7
Nyckelord: njurcancer, avbildning av njurtumörer, djupinlärning, CT-skanning, datorstödd diagnostik