Clear Sky Science · sv
Integrerad analys av globala regulatorer och efflux‑gener kopplade till återställning av antimikrobiell känslighet hos multiresistent Klebsiella pneumoniae
Varför dessa vårdburna bakterier är så svåra att döda
I sjukhus världen över har vissa stammar av bakterien Klebsiella pneumoniae blivit ökända för att vara svåra att behandla. De står emot flera antibiotika som tidigare fungerade pålitligt, vilket förvandlar rutininfektioner till livshotande nödlägen. Denna studie undersöker vad som händer under mikrobiens huva för att förstå en viktig mekanism dessa bakterier använder: mikroskopiska pumpar som spottar ut antibiotika ur cellen, och de genetiska strömbrytare som verkar skruva upp eller ner dessa pumpar.
Superbakterier och deras molekylära flyktvägar
Multiresistent Klebsiella pneumoniae förekommer nu på många sjukhus, inklusive det irakiska medicinska centrum där denna forskning utfördes. Dessa bakterier kan överleva flera stora antibiotikagrupper samtidigt, såsom fluorokinoloner, aminoglykosider och tredje generationens cefalosporiner. Ett sätt de gör detta på är genom att installera kraftfulla ”effluxpumpar” i sitt cellskikt. En av de viktigaste är ett system kallat AcrAB‑TolC, som går tvärs genom bakteriens membran och fungerar som en liten dräneringspump, fångar upp antibiotikamolekyler inne i cellen och skjuter ut dem innan läkemedlen kan göra allvarlig skada. När dessa pumpar är mycket aktiva hinner aldrig antibiotikakoncentrationen inne i bakterien bli tillräckligt hög för att vara dödlig.
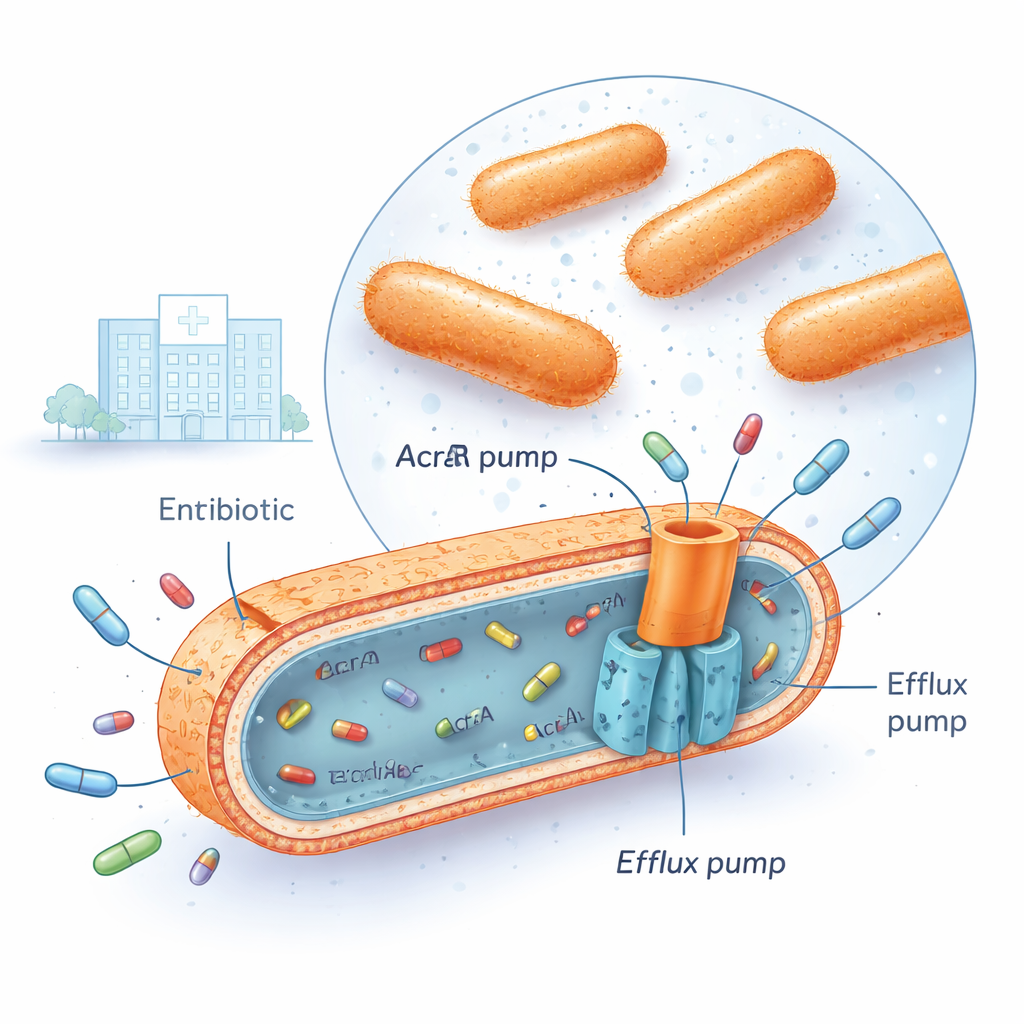
Genströmbrytare som följer med pumpöverdrev
Forskarna samlade in 30 kliniska isolat av multiresistent Klebsiella pneumoniae och jämförde dem med 10 antibiotikakänsliga isolat och en standardreferensstam. Med en teknik kallad kvantitativ realtids‑PCR mätte de hur mycket vissa gener var aktiverade. De fokuserade på tre ”globala regulatorer” — generna marA, soxS och rob — tillsammans med de tre delarna av AcrAB‑TolC‑pumpen (acrA, acrB och tolC). I de resistenta stammarna var två regulatorer, marA och soxS, vanligtvis uppreglerade cirka fyra till fem gånger jämfört med känsliga bakterier, medan acrB, en central pumpkomponent, ökade nästan åtta gånger. Statistisk analys visade att när nivåerna av marA och soxS var höga, var också acrB-nivåerna vanligen höga, och dessa stammar tenderade att tåla mycket högre doser av fluorokinolonantibiotika som ciprofloxacin. En tredje regulator, rob, förändrades lite och korrelerade inte med pumpaktiviteten, vilket tyder på att den spelar en mindre roll under de testade förhållandena.
Stänga av pumparna för att försvaga resistensen
Att hitta att pump- och regulatorgener är aktiva tillsammans är talande men räcker inte för att bevisa att de verkligen driver resistensen. För att testa om pumparna var funktionellt viktiga använde teamet ett kemiskt verktyg kallat PAβN. Denna förening används inte som läkemedel hos patienter, men i laboratoriet kan den täppa till AcrAB‑TolC‑liknande pumpar och hindra dem från att pumpa ut antibiotika. Forskarnas val föll på tio resistenta isolat som hade särskilt höga nivåer av acrB-genen och de mätte hur mycket ciprofloxacin som krävdes för att stoppa deras tillväxt, med och utan PAβN. I åtta av dessa tio stammar sänkte pumpblockeringen den nödvändiga ciprofloxacin‑dosen minst fyra gånger, och ibland så mycket som sexton gånger. Denna minskning visar att aktiva effluxpumpar i många av dessa superbakterier verkligen är en huvudorsak till att de kan tolerera höga antibiotikadoser.
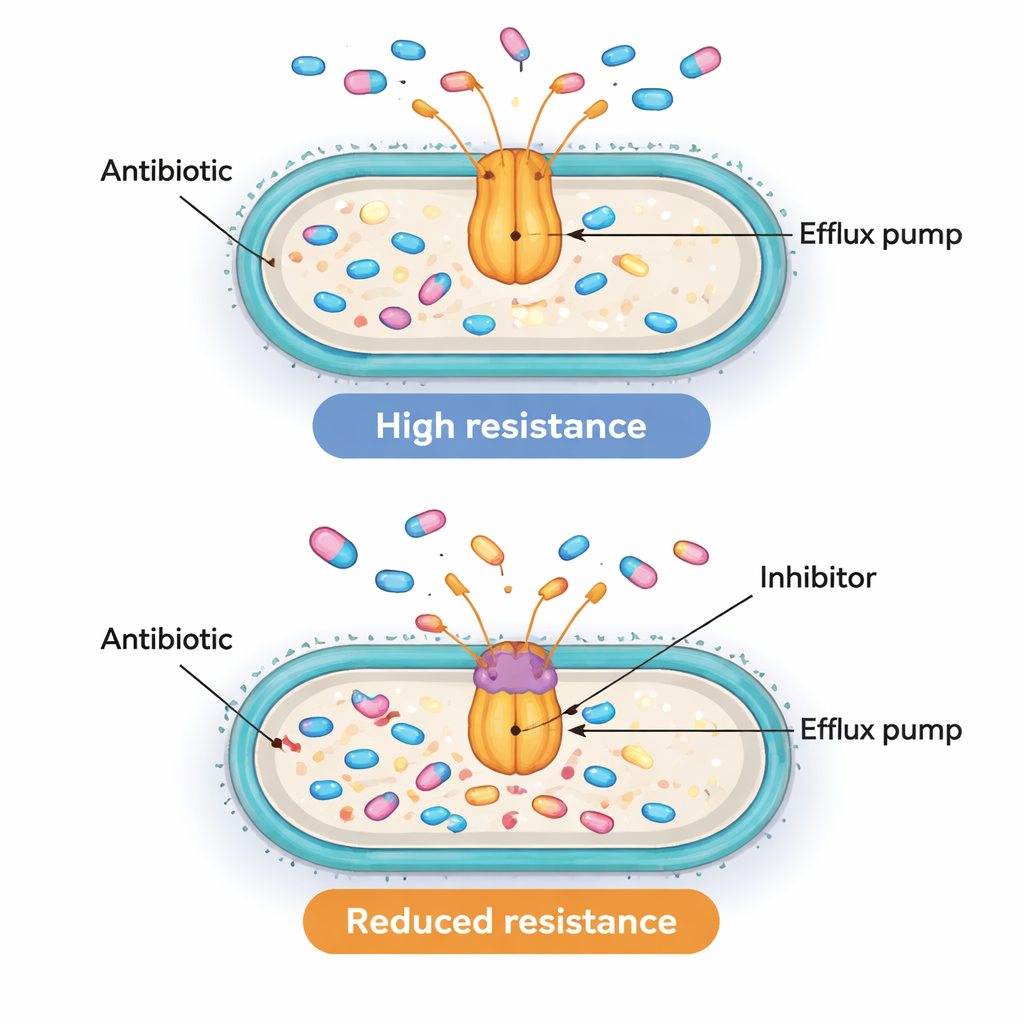
Ett komplext resistenspussel med lovande mål
Inte alla stammar uppträdde likadant. Vissa bakterier med stark uttryckta pumpgener återfick bara delvis känslighet när pumparna blockerades, vilket antyder att andra resistensvägar — såsom ändringar i antibiotikats mål inne i cellen, produktion av enzym som bryter ner läkemedel eller alternativa pumpar — också bidrar. Gentamicin, ett aminoglykosidantibiotikum, påverkades till exempel i stor utsträckning inte av de mönster som sågs i marA/soxS och AcrAB‑TolC‑generna, vilket understryker att multiresistens vanligtvis byggs upp av flera överlappande försvar snarare än en enskild mekanism.
Vad detta betyder för framtida behandlingar
För icke‑specialister är huvudbudskapet att vissa sjukhusbakterier kan överleva antibiotika inte bara genom att blockera eller sönderdela läkemedel, utan genom att aktivt kasta ut dem. Denna studie kopplar högre aktivitet hos två genetiska ”strömbrytare”, MarA och SoxS, till mer aktiva effluxpumpar och starkare resistens mot en vida använd klass av antibiotika. När pumparna experimentellt täpps igen blir många av dessa bakterier åtminstone delvis känsliga igen. Även om arbetet ännu inte bevisar exakt hur dessa regulatorer styr pumparna, lyfter det fram både regulatorerna och pumparna som attraktiva mål. I längden kan kombinationer av konventionella antibiotika med säkra pumpblockerare — eller läkemedel som dämpar dessa globala regulatorer — hjälpa till att återställa användbarheten hos befintliga behandlingar mot annars skrämmande multiresistenta infektioner.
Citering: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Nyckelord: antibiotikaresistens, effluxpumpar, Klebsiella pneumoniae, fluorokinoloner, återställning av resistens