Clear Sky Science · sv
Nedreglering av deubiquitinerande enzymet USP10 korrelerar med neuronal apoptos vid HTLV-1‑associerad myelopati
Varför detta betyder något för personer som lever med virala nervsjukdomar
Vissa virus orsakar inte bara kortvariga infektioner; de kan tyst skada nervsystemet under många år. Human T‑cells leukemi‑virus typ 1 (HTLV‑1) är ett sådant virus och kan leda till en kronisk ryggmärgssjukdom kallad HTLV‑1‑associerad myelopati (HAM). Personer med HAM förlorar gradvis styrka och kontroll i benen, tillsammans med blåsa‑ och sensoriska problem. Den här studien ställer en enkel men avgörande fråga: varför dör nervcellerna i ryggmärgen vid detta tillstånd, och kan en enda skyddande molekyl hjälpa förklara vem som drabbas hårdare eller klarar sig bättre?
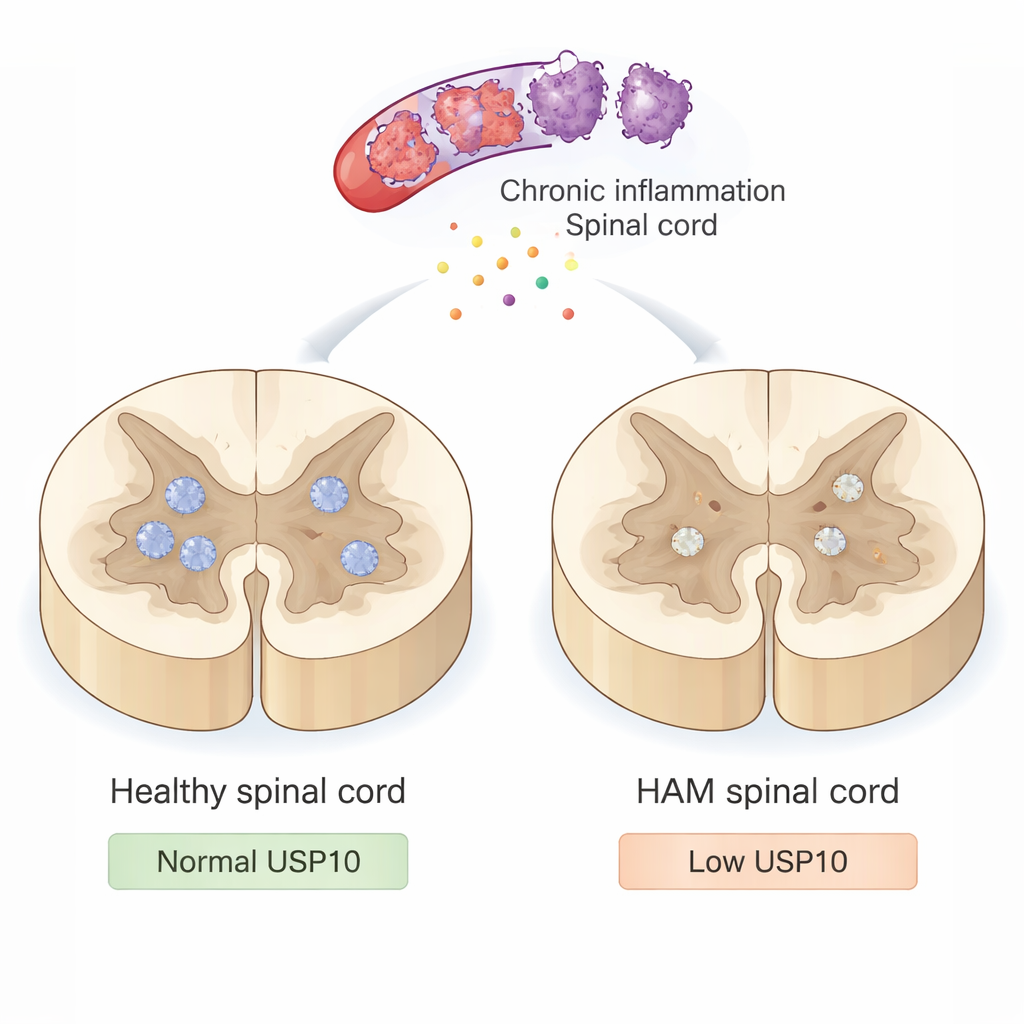
En långsam attack mot ryggmärgen
HAM orsakas inte av att viruset direkt infekterar nervceller. Istället infekterar HTLV‑1 immunceller som invaderar ryggmärgen och utlöser långvarig inflammation. Dessa överaktiva immunceller släpper ut giftiga ämnen och inflammatoriska signaler som, även om de är avsedda att kontrollera infektionen, också skadar närliggande neuroner och deras isolerande myelin. Med tiden leder denna glödande påverkan till stela, svaga ben och svårigheter att gå. Ändå förstår läkarna fortfarande inte helt varför vissa neuroner ger efter för denna inflammatoriska miljö medan andra överlever i årtionden.
Ett cellulärt "städnings"‑enzym under misstanke
Forskarna fokuserade på ett protein kallat USP10, ett enzym som hjälper till att hantera cellens proteins kvalitetskontrollsystem och som är känt för att begränsa cellulär stress och programmerad celldöd (apoptos). USP10 är aktivt i många vävnader, inklusive hjärnan och ryggmärgen, och tidigare arbete vid Parkinsons sjukdom, stroke och andra tillstånd tyder på att det hjälper neuroner att tåla oxidativ och inflammatorisk skada. Med ryggmärgsprover från åtta personer som avlidit med HAM och två neurologiskt friska kontroller använde teamet färgningstekniker för att se var USP10 fanns och hur starkt det uttrycktes i nervceller.
Mindre USP10, fler döende neuroner
I friska ryggmärgar var USP10 starkt synligt i många neuroner. I de flesta HAM‑fallen var dock USP10‑färgningen i neuroner tydligt reducerad, och i en patient var den nästan obefintlig. Forskarna letade sedan efter kännetecken för apoptos med två metoder: ett TUNEL‑test som detekterar fragmenterat DNA och färgning för aktivt caspase‑3, ett protein som är involverat tidigt i celldöd. I kontrollerna visade praktiskt taget inga neuroner dessa dödssignaler. I kontrast var en stor andel neuroner TUNEL‑positiva hos HAM‑patienterna och många visade aktivt caspase‑3. Viktigt är att prover med lägre USP10‑uttryck tenderade att ha fler apoptotiska neuroner och färre överlevande neuroner märkta med NeuN, en standardmarkör för neuroner. En anmärkningsvärd patient med HAM som fortfarande gick med endast en käpp efter 22 år hade starkt USP10‑uttryck och relativt bevarat neuronantal, vilket antyder att högre USP10 kan bidra till skydd mot svår funktionsnedsättning.
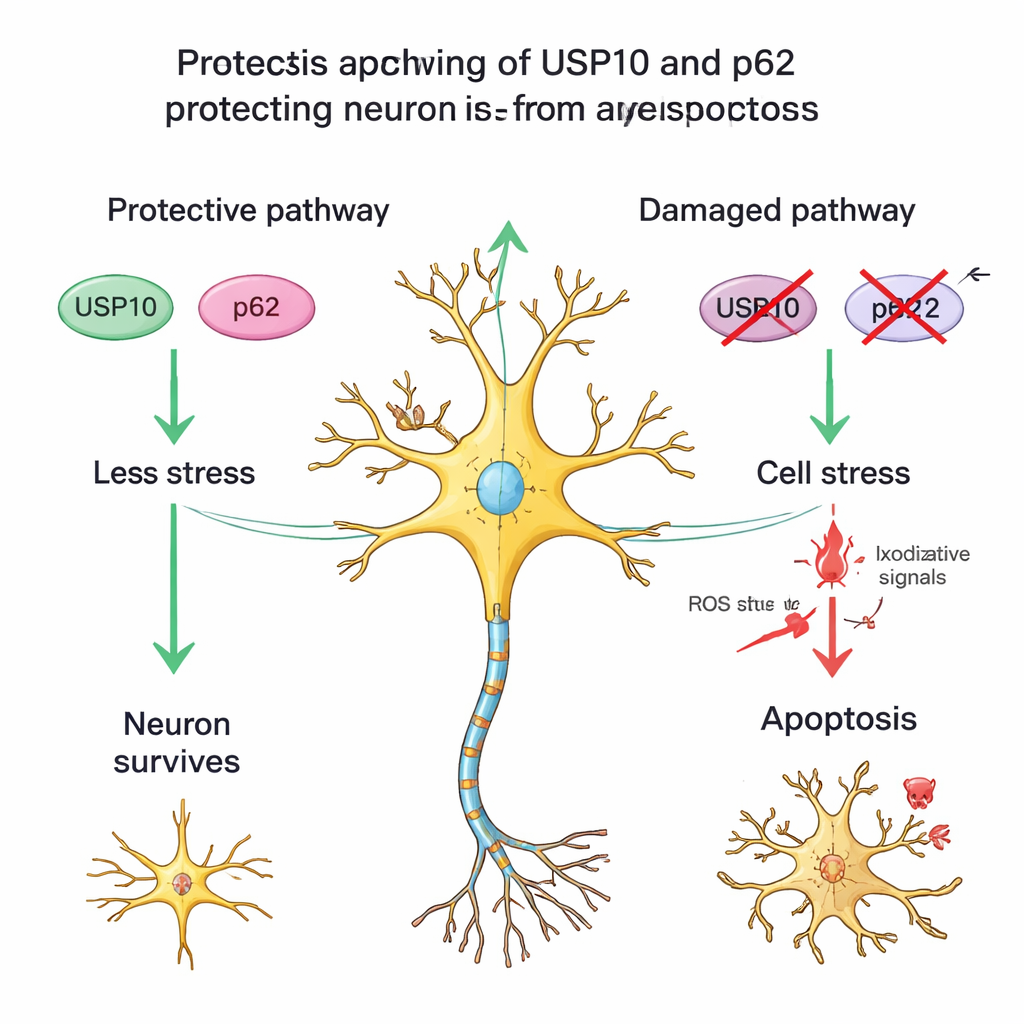
En partnerprotein och stressade men överlevande celler
Teamet undersökte också ett annat protein, p62, som samarbetar med USP10 i hanteringen av skadade proteiner och regleringen av stress‑ och överlevnadsvägar. I friska ryggmärgar var p62‑färgningen måttlig; bland HAM‑patienterna hade de med låg USP10 ofta också svagare p62‑färgning och färre överlevande neuroner. Detta mönster stöder idén om ett USP10–p62‑partnerskap som hjälper neuroner att stå emot kronisk inflammation. Forskarna lade dessutom märke till många nervceller i HAM‑vävnad som hade typisk nervcellsmorfologi men hade förlorat NeuN‑färgning, ett tecken som ses vid andra hjärnskador när neuroner är under allvarlig stress men inte fullständigt döda. Detta tyder på att vid HAM går inte bara vissa neuroner förlorade direkt utan att andra förblir i ett skadat, sårbart tillstånd, sannolikt därför att USP10‑kopplade försvar försvagats.
Vad detta kan innebära för framtida diagnostik och behandling
Denna studie bevisar inte att förlust av USP10 direkt orsakar neuronalt dödande, eftersom den baseras på ett litet antal obduktionsprover och inte kan följa förändringar över tid. Ändå pekar de konsekventa sambanden mellan låg USP10, minskat p62, fler tecken på apoptos och färre överlevande neuroner mot en gemensam väg som kan förena kronisk inflammation och långsam neurondegeneration i HAM. För patienter väcker detta en uppmuntrande möjlighet: att mäta eller stärka USP10‑relaterade vägar i ryggmärgen—eller eventuellt i mer lättåtkomliga prover som ryggmärgsvätska—skulle en dag kunna hjälpa till att identifiera dem med högre risk för snabb progression, styra uppföljning eller inspirera nya behandlingar utformade för att förstärka cellens egna stress‑skyddssystem vid virusinducerade neuroinflammatoriska sjukdomar.
Citering: Arishima, S., Takahashi, M., Dozono, M. et al. Downregulation of the deubiquitinating enzyme USP10 correlates with neuronal apoptosis in HTLV-1-associated myelopathy. Sci Rep 16, 6062 (2026). https://doi.org/10.1038/s41598-026-37271-x
Nyckelord: HTLV-1‑associerad myelopati, neuroinflammation, neuronal apoptos, USP10, ryggmärgsdegeneration