Clear Sky Science · sv
Antibakteriell verkan och cytotoxicitet hos trikalciumsilikatbaserade cement med olika antibakteriella tillsatser
Varför detta spelar roll för ditt nästa fyllningsingrepp
När du har en djup karies försöker tandläkare idag bevara så mycket naturlig tand som möjligt istället för att borra bort allt. Det innebär ofta att ett tunt lager mjuk, bakteriefylld dentin lämnas kvar under fyllningen. Denna studie ställer en enkel men avgörande fråga: kan vi förbättra ett vida använt reparationscement så att det tyst dödar kvarvarande bakterier utan att skada de levande cellerna inne i tanden?
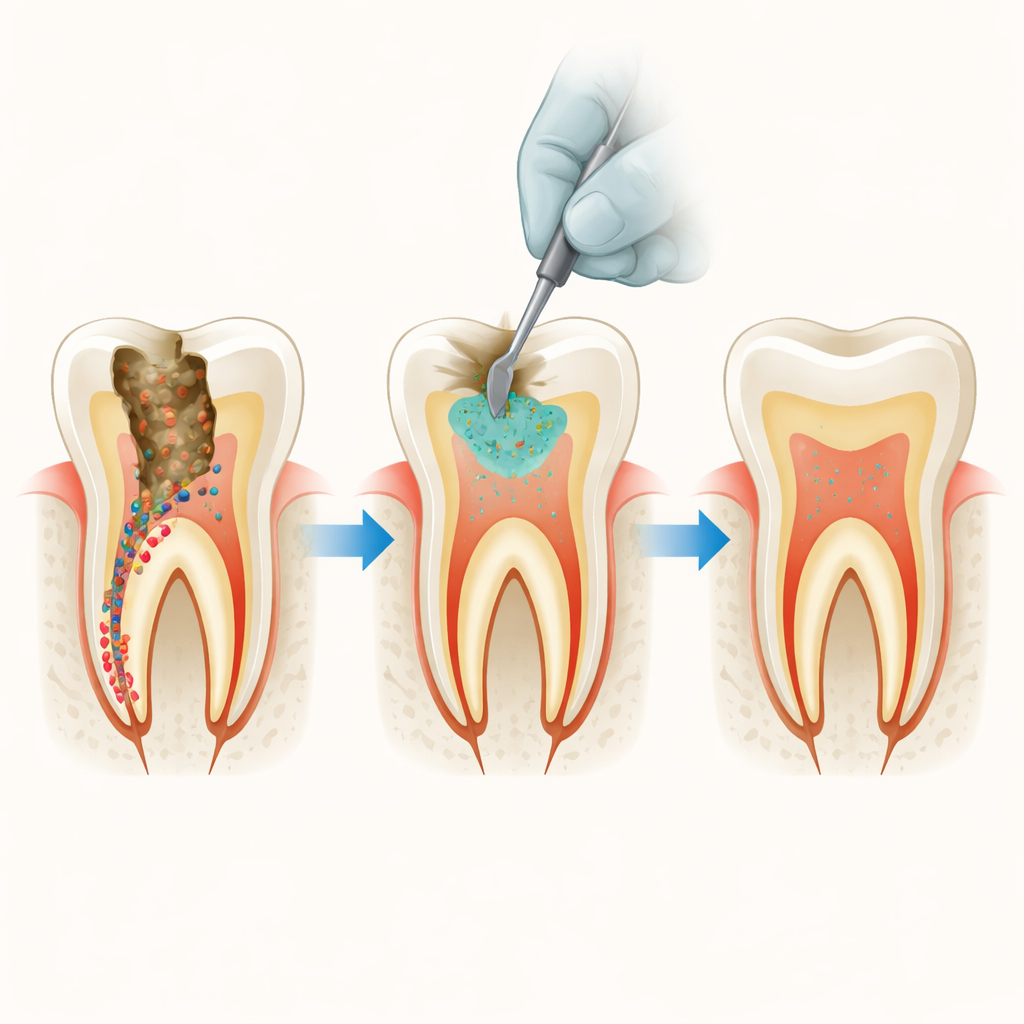
Djupa karier och dolda bakterier
Moderna ”minimalt borrande” tekniker syftar till att undvika att exponera tandens mjuka kärna, eller pulpa, genom att lämna kvar dentin som fortfarande kan mineraliseras igen. Nackdelen är att vissa kariesframkallande bakterier, såsom Streptococcus mutans och Lactobacillus‑arter, kan finnas kvar i det lagret. Med tiden kan dessa bakterier orsaka ny karies under en till synes frisk fyllning. Trikalciumsilikatbaserade cement är populära för tätning av djupa håligheter eftersom de främjar mineralbildning och skapar en tät barriär, men i sig är de inte särskilt effektiva mot bakterier.
Att förvandla ett vanligt cement till en bakteriekämpe
Forskarnas utgångspunkt var att blanda detta välkända cement med fem olika antibakteriella tillsatser i varierande styrkor. Två var organiska föreningar som ofta finns i desinfektionsmedel (benzalkoniumklorid och cetrimid), och tre var oorganiska ämnen som används i tandvårdsprodukter eller material (titandioxid, zinkoxid och tennfluorid). De pressade dessa blandningar till små skivor och placerade dem på plattor beströdda med fem bakterietyper kopplade till karies och orala infektioner. Genom att mäta de klara zonerna runt varje skiva där bakterier inte kunde växa kunde de avgöra hur väl varje recept höll bakterierna borta.
Att hitta balansen mellan att döda bakterier och skona celler
Då ett material som dödar bakterier men också förgiftar tandens celler vore oanvändbart i munnen, testade teamet också hur de mest lovande tillsatserna påverkade levande celler. De exponerade två mänskliga celltyper—fibroblaster, som är vanliga stödjeceller, och pulpastamceller, som hjälper till att reparera tandvävnad—för cementen indirekt. Ett färgförändringstest mätte hur många celler som förblev aktiva, och särskilda fluorescerande färgämnen visade levande (grönt) och döda (rött) celler i mikroskopet. Denna uppställning efterliknade den verkliga situationen i en djup karies där cementet är åtskilt från pulpan av ett tunt dentinlager och avger ämnen som diffunderar mot cellerna.
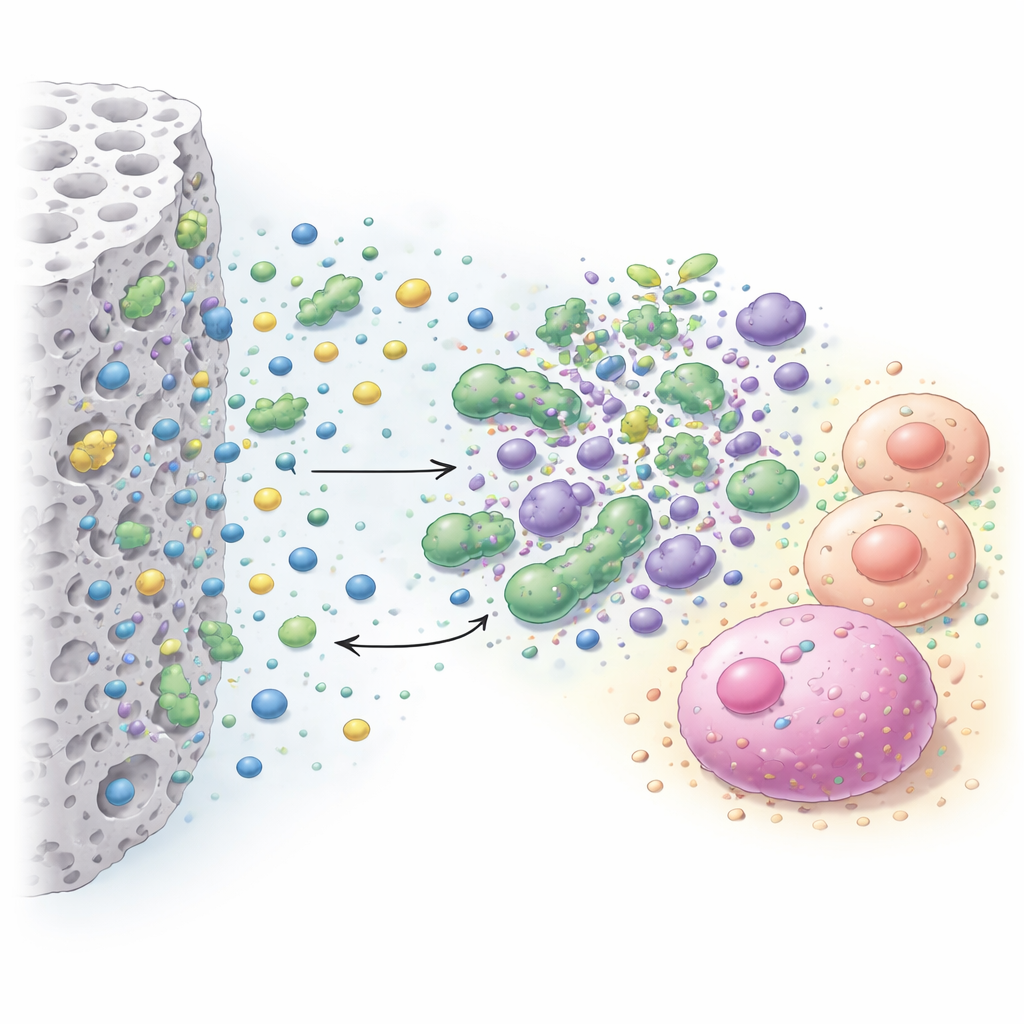
Vad som fungerade bäst och vad som var för hårt
Resultaten visade att både typ och mängd tillsats spelar stor roll. Benzalkoniumklorid gav den starkaste och mest omfattande antibakteriella effekten och skapade stora bakteriefria zoner mot alla testade arter, särskilt Lactobacillus‑stammarna som ofta finns i djup karies. Cetrimid hjälpte också, men krävde i allmänhet högre koncentrationer för att nå benzalkoniumets prestanda. De tre oorganiska medlen förbättrade bara cementets antibakteriella effekt vid de högre doserna som testades, och då främst mot vissa bakterier såsom S. mutans och Actinomyces. På säkerhetssidan var bascementet ensamt skonsamt mot båda celltyperna och verkade till och med stödja fibroblastens hälsa. Tillsättning av benzalkoniumklorid förblev ofarligt för fibroblaster upp till cirka 1 %, blev lätt skadligt vid 2–4 % och tydligt mer skadligt vid 7 %. Pulpa‑stamceller var känsligare överlag: både benzalkoniumklorid och cetrimid minskade deras överlevnad, med cetrimid som blev måttligt toxisk från 2 % och uppåt.
Vad detta kan innebära för framtida tandvård
Sammantaget pekar studien på ett särskilt lovande recept: trikalciumsilikatbaserat cement med 1 % benzalkoniumklorid. På den nivån undertryckte materialet starkt skadliga bakterier samtidigt som fibroblaster förblev fullt levande och pulpastamceller mestadels livskraftiga. I praktiska termer antyder det att framtida djupa fyllningar skulle kunna göras av ett cement som tyst bekämpar kvarvarande bakterier under ytan samtidigt som det är tillräckligt skonsamt mot den levande vävnaden inne i tanden. Mer arbete behövs—särskilt i komplexa, verkliga munförhållanden—men denna balanserade formulering kan hjälpa tandläkare att bättre skydda tänder som behandlats med minimalt invasiva tekniker.
Citering: Banon, R., Martens, L., De Coster, P. et al. Antibacterial activity and cytotoxicity of tricalcium silicate-based cements with different antibacterial additives. Sci Rep 16, 8349 (2026). https://doi.org/10.1038/s41598-026-37269-5
Nyckelord: djup dental karies, antibakteriellt tandcement, trikalciumsilikat, benzalkoniumklorid, biokompatibilitet hos pulpaceller