Clear Sky Science · sv
Avbildning av intercellulära biomolekyler med fluorescerande proteinindikatorer fästa med lipid-PEG-ankare
Att se celler kommunicera i realtid
Våra hjärnor och kroppar är beroende av en ständig kemisk konversation mellan celler. Joner och signalsubstanser förmedlar meddelanden över små springor, men dessa snabba, flyktiga signaler är svåra att iaktta utan att störa dem. Denna studie presenterar ett enkelt sätt att ”måla” levande celler med lysande sensorer som fäster vid deras yttre yta, vilket gör det möjligt för forskare att i realtid och med detaljer se dessa budskap—särskilt kaliumjoner och signalsubstansen glutamat. 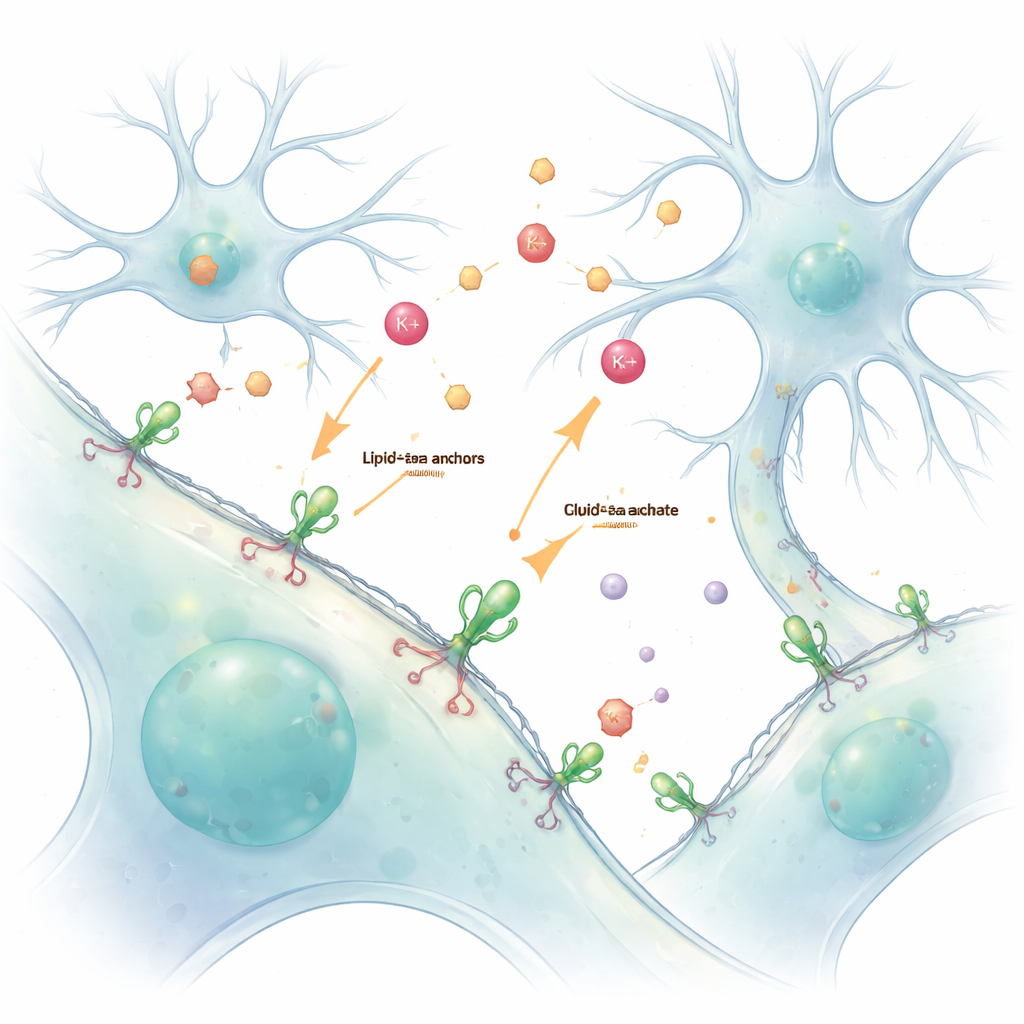
Ett nytt sätt att tagga cellmembranet
Traditionellt konstruerar forskare celler att själva tillverka fluorescerande proteinsensorer genom genetiska metoder. Trots styrkan i detta tillvägagångssätt hamnar sensorerna ofta felaktigt inuti cellen, vilket försvårar att skilja vad som händer inne i cellen från vad som sker utanför. Författarna löste detta genom att använda ett kemiskt handtag kallat lipid–PEG-ankare. Den ena änden av denna molekyl bäddas in i det yttre membranet, medan den andra änden är kemiskt kopplad till en fluorescerande proteinsensor. När dessa förberedda sensorer enkelt tillsätts till levande celler täcker de spontant utsidan och bildar ett stabilt, lysande lager som rapporterar vad som händer i omgivande vätska.
Att göra kalium och glutamat synliga
Teamet anpassade två existerande fluorescerande indikatorer: GINKO2, som reagerar på kaliumjoner, och R-iGluSnFR1, som reagerar på glutamat. De renade dessa proteiner från bakterier och kopplade sedan på lipid–PEG-ankaren. I odlade humana celler bildade det ankade kaliumsensorn en jämn kontur längs cellytan och ljusnade när extracellulärt kalium ökade, för att sedan avta när nivåerna sjönk. Viktigt är att dess ljusemitterande egenskaper och känslighet i provrörstester stämde väl överens med den ursprungliga, omodifierade sensorn, vilket visar att förankringen inte försämrade dess prestanda. Detsamma gällde för glutamatsensorn, som förblev responsiv efter förankring och tydligt framhävde glutamat i utrymmet precis utanför cellerna.
Lyssna på neuroner i kulturer och skivor
Forskarna gick därefter vidare till nervceller från musens hippocampus, en hjärnregion viktig för inlärning och minne. De belade dessa neuroner med det lipid–PEG–ankrade glutamatsensorn och fyllde insidan av samma celler med en separat kalciumsignalfläck som rapporterar elektrisk aktivitet. Med totalreflektionsmikroskopi kunde de samtidigt se röda blixtar från glutamat vid cellytan medan gröna signaler inne i cellerna visade när de sköt aktionspotentialer. Denna tvåfärgade vy visade att de ankade sensorerna kunde följa spontan signalsubstansfrisättning utan någon genetisk modifiering av neuronerna själva.
Kartlägga kemiska vågor i hjärnvävnad
Nästa steg var att testa metoden i akuta hjärnskivor, som bevarar hippocampusens naturliga kopplingar. De applicerade den ankade kaliumsensorn på skivorna och elektriskt stimulerade nervfibrer. Den ankade sensorn gav klara, reproducerbara fluorescensökningar efter varje stimulus, medan icke-ankrade sensorer snabbt diffunderade bort och gav svaga, instabila signaler. Genom att bada skivorna i lösningar med kända kaliumnivåer, och korrigera för vävnadens egen svaga glöd, byggde författarna en kalibreringskurva och skattade faktiska extracellulära kaliumkoncentrationer. Vilonivåer var cirka 2,5 millimolar och steg till ungefär 3,4 millimolar vid måttlig stimulering, i linje med klassiska elektrodmätningar. Ankade sensorer för både kalium och glutamat visade hur dessa signaler sprids olika: glutamatsvängningar höll sig nära aktiva synapser, medan kaliumökningar sträckte sig flera hundra mikrometer, vilket antyder bredare effekter på nätverkets excitabilitet. 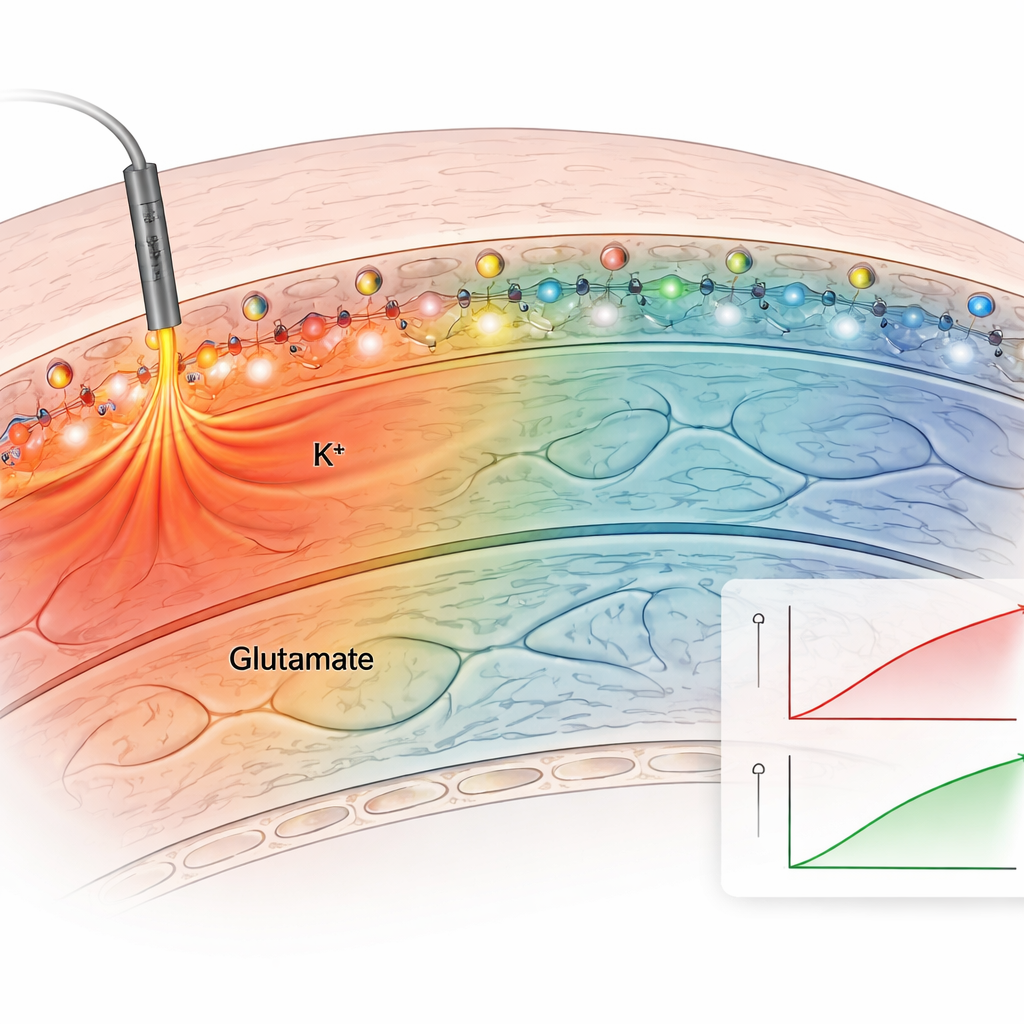
Undersöka hur hjärnan rensar och genererar signaler
Eftersom sensorerna sitter fixerade vid cellytan kunde författarna urskilja vilka processer som formar dessa extracellulära vågor. Blockering av glutamattransportörer, som normalt plockar upp glutamat, gjorde att den ankarförsedda glutamatsensorn visade större och mer långvariga signaler, vilket bekräftar att lokal upptagning begränsar glutamatspridning. Blockering av AMPA-typens glutamatreceptorer minskade både elektriska responser och kaliumsignaler, vilket indikerar att större delen av kaliumökningen kommer från postsynaptiska neuroner aktiverade av synaptisk input. Blockering av natriumkanaler med tetrodotoxin nästan eliminerade kaliumförändringarna, vilket knyter dem direkt till aktionspotentialer. Tillsammans visar dessa experiment hur ankade sensorer kan omvandla komplex, distribuerad kemi till intuitiva filmer och kartor.
Varför detta är viktigt för framtida hjärnforskning
För icke-specialister är huvudbudskapet att detta arbete erbjuder ett snabbt, icke-genetiskt sätt att belägga levande celler och vävnader med mycket känsliga molekylära rapportörer. Istället för att omkonstruera varje celltyp kan forskare tillsätta färdiga sensorproteiner utifrån och omedelbart visualisera hur joner och signalsubstanser förändras i realtid vid cellytan. Detta tillvägagångssätt förbättrar kontroll, reproducerbarhet och rumslig precision samtidigt som utmaningarna med genleverans undviks, särskilt i känsliga preparationer som akuta hjärnskivor. Allteftersom fler fluorescerande indikatorer utvecklas för olika kemikalier kan samma lipid–PEG-förankringsstrategi bli ett allmänt använt verktyg för att iaktta cellernas kemiska språk över hela kroppen.
Citering: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Nyckelord: extracellulär signalering, fluorescerande biosensorer, glutamatavbildning, kaliumdynamik, hippokampala neuroner