Clear Sky Science · sv
Dynamisk grafkonvolution med omfattande beskärning och GNN-klassificering för precis upptäckt av lymfkörtelmetastas
Varför små förändringar i lymfkörtlar spelar roll
När bröstcancer sprider sig är lymfkörtlar ofta den första anhalten — små filter som ligger längs kroppens dräneringssystem. Att avgöra om cancerceller nått dessa körtlar är ett av de viktigaste spåren läkare använder för att välja kirurgi, kemoterapi och strålbehandling. Även erfarna patologer kan dock missa mycket små cellkluster i digitala mikroskopbilder, särskilt när de nästan är omöjliga att skilja från frisk vävnad. Denna studie presenterar ett nytt artificiellt intelligens-ramverk som behandlar vävnad som ett nätverk av sammanlänkade regioner, vilket gör att det kan hitta subtila tecken på spridning med anmärkningsvärd noggrannhet.
Att omvandla vävnadsbilder till nätverk
Forskarna arbetar med enorma digitala snitt av färgade vävnader, så kallade whole-slide images, från bröstcancerlymfkörtelbiospier. Dessa bilder innehåller miljontals pixlar och en förvirrande blandning av celltyper, färger och texturer. För att hantera denna komplexitet rengör teamet först bilderna: de normaliserar ljusstyrka och färg, minskar brus och skapar förstärkta kopior genom att rotera och spegla bildlappar så att datorn lär sig hantera naturlig variation. Varje bildlapp delas sedan upp i små, relativt homogena regioner (”superpixlar”), som blir punkterna — eller noderna — i en graf, medan relationerna mellan grannregioner bildar förbindelserna — eller kanterna. Denna nätverksvy bevarar de oregelbundna formerna och arrangemangen i verklig vävnad bättre än traditionella rutnätsbaserade bildmetoder.
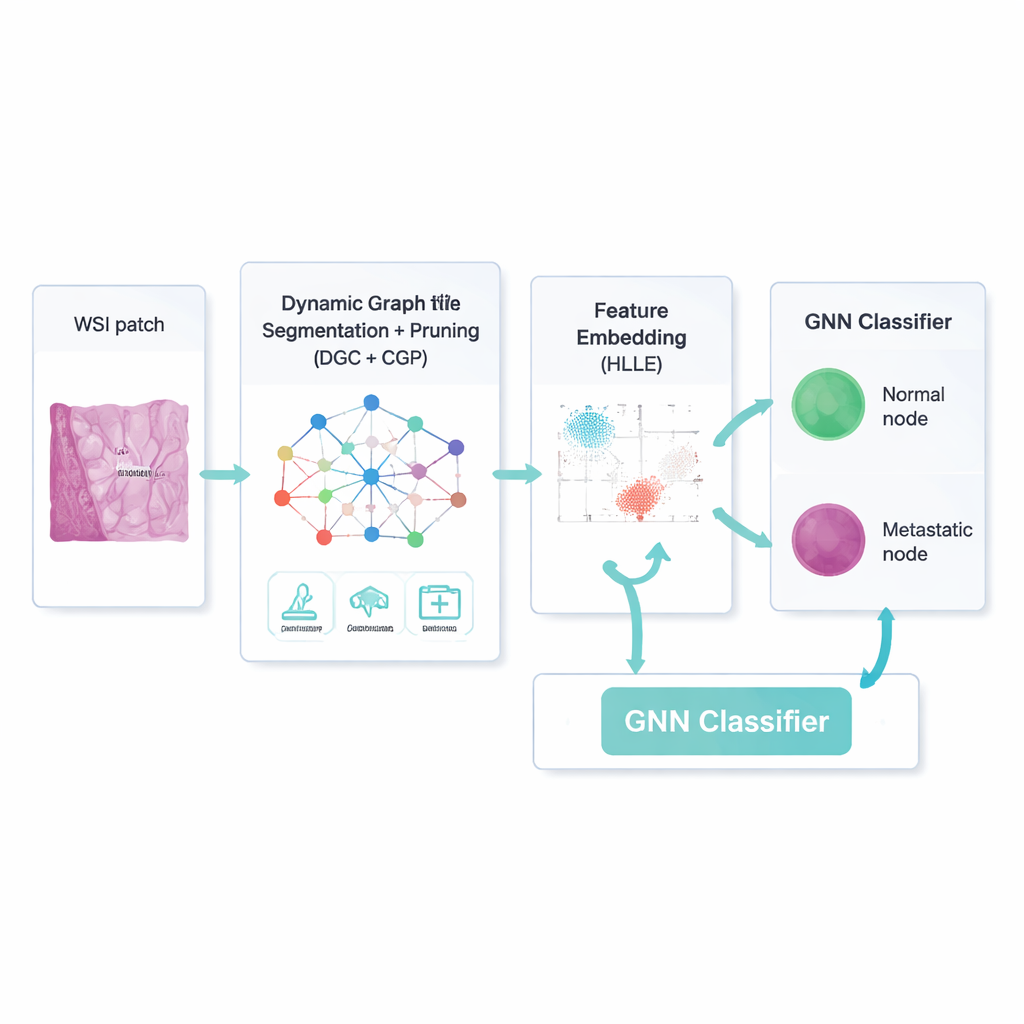
Ett smartare sätt att fokusera på det som betyder något
Att bara bygga ett nätverk räcker inte; många förbindelser och bildfunktioner är irrelevanta eller till och med vilseledande. Ramverket använder därför en dynamisk grafkonvolutionell autoencoder — en typ av neuralt nätverk som lär sig både hur varje region ser ut och hur regioner påverkar varandra. En tillagd ”attention”-mekanism lär modellen att vikta vissa bildkanaler mer än andra, till exempel genom att betona kanter vid en tumörgräns. Samtidigt beskärs oönskade delar successivt med en strategi som kallas Comprehensive Graph Gradual Pruning: svaga kopplingar mellan regioner, mindre användbara numeriska funktioner och lågpåverkande modellvikter plockas bort. Denna beskärning sker under träningen, inte efteråt, så systemet lär sig att göra mer med mindre och blir både snabbare och lättare att tolka.
Komprimera mönster utan att tappa formen
När modellen har separerat sannolika lymfkörtelregioner från bakgrundsvävnad måste varje region ändå beskrivas på ett kompakt men meningsfullt sätt. För detta använder författarna en teknik kallad Hessian-baserad Locally Linear Embedding. Enkelt uttryckt pressar den många numeriska funktioner ner till en mindre uppsättning samtidigt som den försöker bevara den krökta ”formen” i hur verkliga exempel är ordnade i funktionsrummet — till exempel hur små metastaser skiljer sig från normala immunceller via subtila textur- eller färgmönster. Dessa komprimerade beskrivningar blir indata till en grafneuronnätverksklassificerare, som återigen arbetar på nätverket av regioner och deras rensade förbindelser och avgör för varje nod om den är metastatisk eller inte.
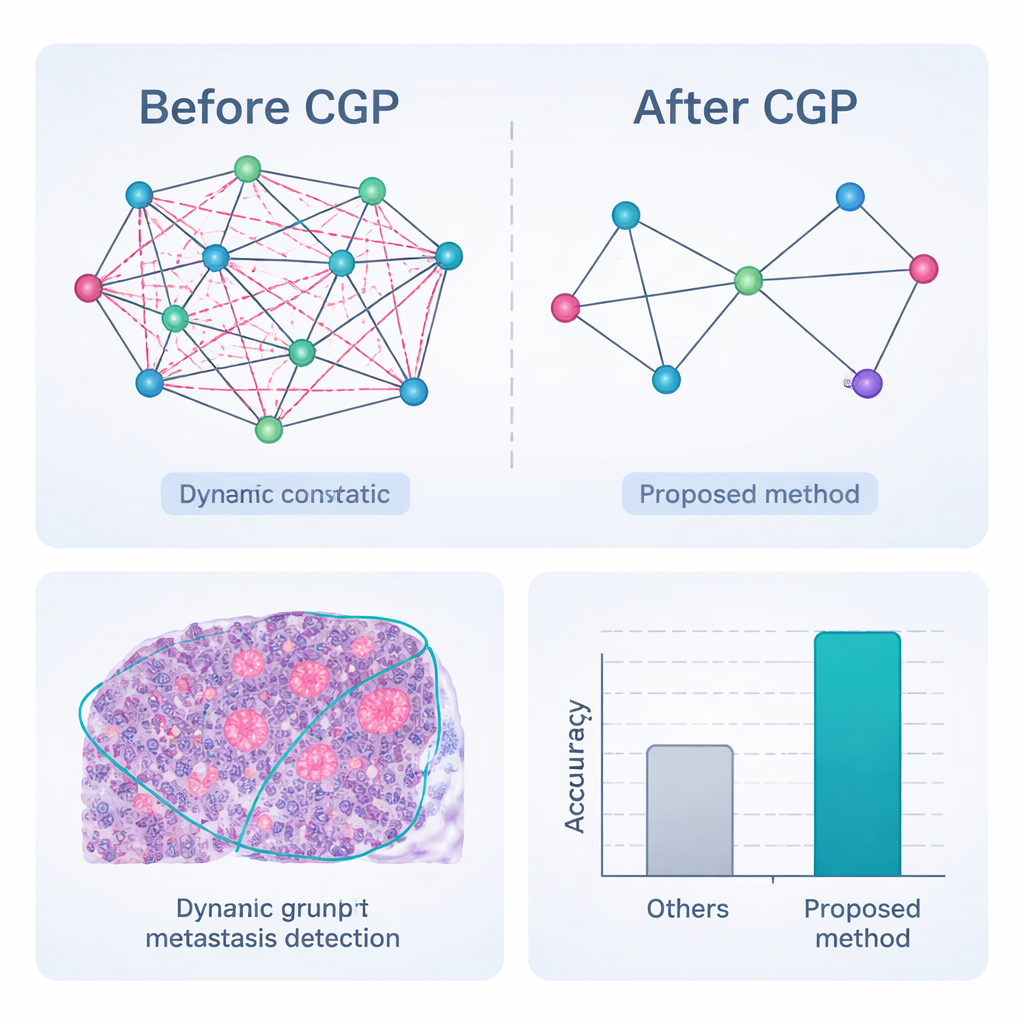
Sätta ramverket på prov
Den kompletta pipeline—förbearbetning, dynamisk grafsegmentering med beskärning, funktionsinbäddning och grafbaserad klassificering—utvärderades på CAMELYON17, en offentlig samling av 1 000 expertannoterade lymfkörtelsnitt från bröstcancerpatienter. Jämfört med en rad starka djupinlärningskonkurrenter, inklusive populära konvolutionsnätverk och hybrida transformermodeller, uppnådde den nya metoden högst poäng i nästan alla mått. Den klassificerade noder korrekt som cancerösa eller inte i 98,65 % av fallen och visade bättre överensstämmelse med experters konturer av tumörområden, särskilt för mycket små eller svaga metastaser. Avgörande är att eftersom grafen beskärs aggressivt uppnås dessa resultat med betydligt färre beräkningar och lägre minnesanvändning, vilket gör metoden bättre lämpad för realtidsanvändning i upptagna patologilabb.
Vad detta betyder för patienter och kliniker
I praktiska termer visar detta arbete hur det att betrakta vävnad som ett smart beskuret nätverk av sammankopplade regioner kan hjälpa datorer att fungera som oerhört noggranna andra granskare av lymfkörtelsnitt. Genom att rikta uppmärksamhet och beräkningskraft mot de mest informativa strukturerna samtidigt som brus avlägsnas, är ramverket bättre på att upptäcka små cancertäckare som annars kunde missas, och det gör det effektivt nog för att vara praktiskt. Även om ytterligare klinisk validering behövs kan sådana verktyg stötta patologer att leverera snabbare och mer konsekventa beslut om huruvida cancer har spridit sig — information som direkt påverkar behandlingsplaner och i slutändan patientutfall.
Citering: H. N., C., N., S., S., A.R. et al. Dynamic graph convolution with comprehensive pruning and GNN classification for precise lymph node metastasis detection. Sci Rep 16, 6682 (2026). https://doi.org/10.1038/s41598-026-37193-8
Nyckelord: lymfkörtelmetastas, digital patologi, grafneuronnätverk, medicinsk bildsegmentering, bröstcancer