Clear Sky Science · sv
Strukturell karaktärisering av metallbindning i mänskliga tyrosylproteinsulfotransferas 2, TPST2
Varför små metalljoner spelar roll för cellsignalering
Inuti våra celler finjusterar otaliga molekylära maskiner tyst hur vävnader växer, hur hormoner verkar och hur immunceller kommunicerar. En sådan maskin, ett enzym kallat TPST2, fäster en liten sulfatmarkör på vissa proteiner när de passerar cellens transportcentral, Golgiapparaten. Denna studie visar hur enkla metalljoner som natrium och mangan hjälper TPST2 att arbeta effektivare genom att subtilt stabilisera delar av dess struktur — en insikt som kan koppla mineralbalans i celler till cancer och hormonsjukdomar. 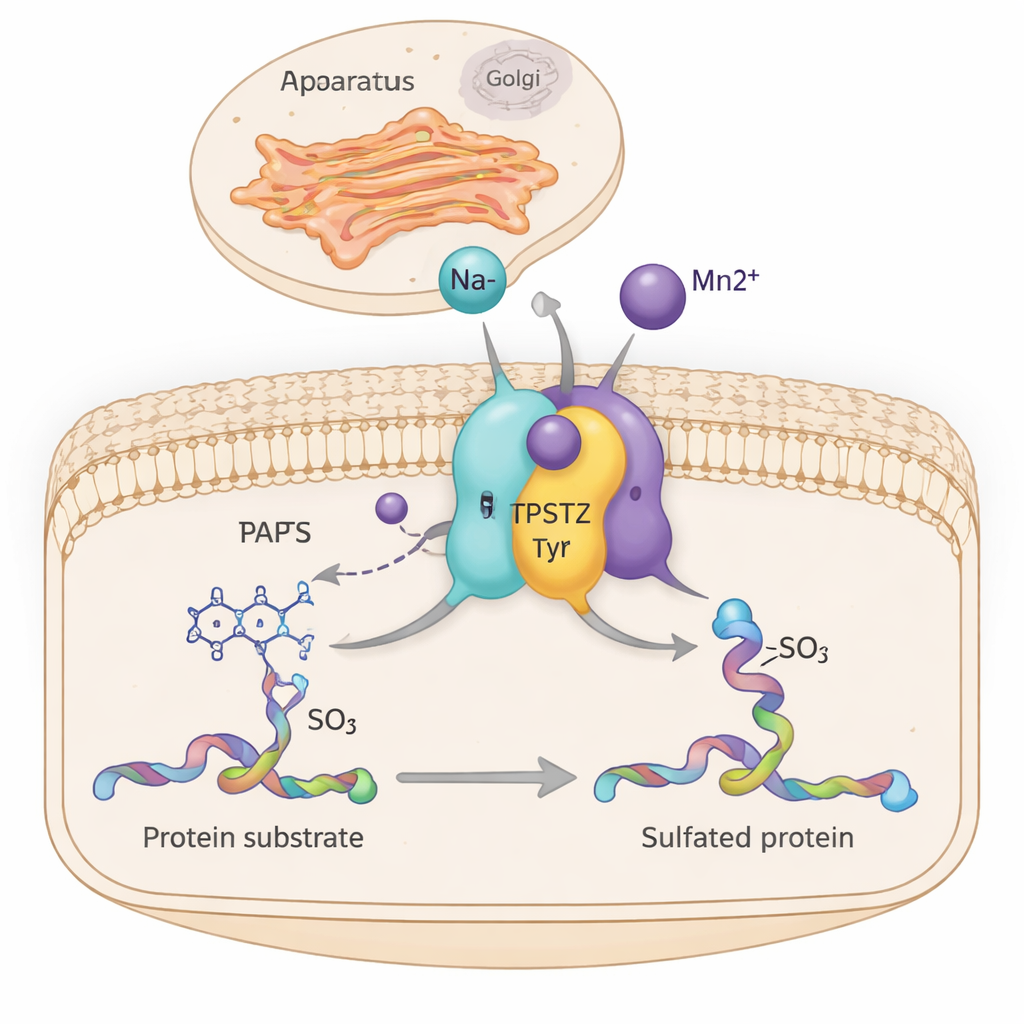
Ett protein som pyntar andra proteiner
TPST2 tillhör en familj enzymer som utför "tyrosinsulfatering", en kemisk modifiering som läggs till specifika tyrosinrester på proteiner. Dessa sulfatmarkerade proteiner spelar viktiga roller utanför cellen och påverkar blodkoagulation, vita blodkroppars rörelse, hormon–receptorbindning och till och med hur virus tränger in i celler. Hos människor finns två huvudenzym för sulfatering, TPST1 och TPST2, som är förankrade i Golgi-membranet och modifierar proteiner när de förbereds för utskeppning. Studier på mus visar att förlust av TPST2 stör produktionen av sköldkörtelhormon, hämmar tillväxt och orsakar manlig infertilitet, vilket understryker dess betydelse för normal fysiologi.
Kopplingar till cancer och immunflykt
Nyare forskning har direkt kopplat TPST2 till sjukdom. I melanom modifierar TPST2 en komponent i interferonreceptorn på ett sätt som försvagar immunsignaler, och blockering av TPST2 förstärker effekten av immunterapier som riktar sig mot PD-1. I pankreascancer hjälper en TPST2-beroende väg att stabilisera ett protein (integrin β4) som främjar tumörtillväxt och spridning. Inhibering av TPST2 i dessa modeller saktar ner cancercellernas delning och invasion. Eftersom TPST2 verkar på proteiner vid cellytan omkopplar det i praktiken hur celler känner av och svarar på sin omgivning, vilket gör det till ett attraktivt mål för nya terapier.
Att hitta metallernas "på-knappar"
Biokemister har länge känt att TPST2 blir mycket mer aktiv när tvåvärda metaller som mangan (Mn²⁺) finns närvarande, men den strukturella förklaringen saknades. I denna studie producerade författarna den katalytiska kärnan av mänskligt TPST2 och kristalliserade den tillsammans med en reaktionsrest och antingen natrium (Na⁺) eller mangan. Med högupplöst röntgenkristallografi upptäckte de två små metallbindningsfickor i enzymet, vardera med en prydlig sexsidig (oktaedrisk) arrangemang av omgivande atomer. Genom att justera röntgenvåglängden till olika metals unika signaturer bekräftade de att Mn²⁺ selektivt ockuperar dessa platser, medan metaller som zink och koppar antingen binder svagt på andra ställen eller inte alls.
Förstärkning av viktiga rörliga delar istället för omformning av hela proteinet
Överraskande nog såg TPST2 med natrium och TPST2 med mangan nästan identisk ut i helhet; det fanns ingen dramatisk öppning eller stängning av proteinet. Istället påverkade metallerna huvudsakligen två flexibla regioner nära ingången till den aktiva ytan: en helix kallad α3 och en närliggande slinga känd som α12–α13-slingan. I metallfria eller löst bundna tillstånd rör sig dessa segment och är delvis oordnade. När Na⁺ binder blir de mer ordnade; Mn²⁺ spänner dem ytterligare, vilket visas av minskad termisk rörelse i röntgendata och av datorbaserade flexibilitetsanalyser. Denna extra styvhet höjer måttligt enzymets smältpunkt och antas sänka den "entropiska" kostnaden för att organisera den aktiva ytan — vilket gör det lättare och snabbare för TPST2 att föra substrat till rätt position för sulfatering. 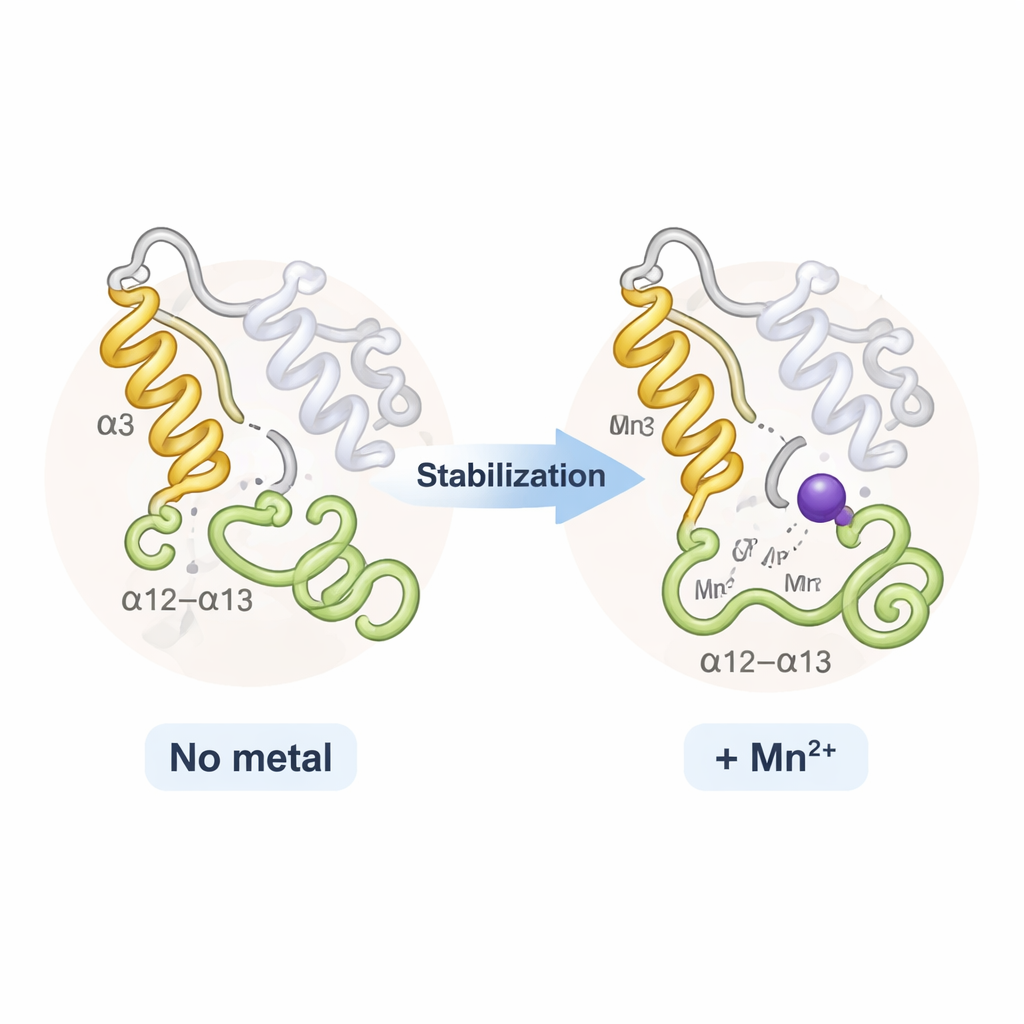
Från cellmineral till signalreglering
Författarna föreslår en "aktivering-genom-ordning"-modell. I avsaknad av bundet metall är TPST2 slappt kring ingången till den aktiva ytan och arbetar ineffektivt. Natrium, som är rikligt i celler, kan binda samma platser och skapa ett delvis ordnat, måttligt aktivt tillstånd. Mangan, som finns i Golgi i noggrant kontrollerade mikromolära mängder, binder starkare och låser nyckelregionerna i en optimalt ordnad konfiguration, vilket maximerar katalytisk effektivitet. Detta antyder att subtila ändringar i Golgi-mangannivåer kan ställa in hur starkt TPST2 modifierar sina mål. Eftersom TPST2 påverkar hormonproduktion och cancersignalering, lyfter arbetet fram en potentiell koppling mellan metalljonbalans, proteinens "pynt" och sjukdom — och ger en strukturell grund för att designa läkemedel som modulerar TPST2-aktivitet genom att efterlikna eller störa metallbindningen.
Citering: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Nyckelord: tyrosinsulfatering, TPST2, mangan, Golgiapparaten, proteinmodifiering