Clear Sky Science · sv
Genomövergripande skärmar identifierar kärnregulatorer för uttryck av prionproteinet på cellytan
Varför detta är viktigt för hjärnhälsa
Prionsjukdomar, såsom Creutzfeldt–Jakobs sjukdom hos människor och "galna ko"-sjukdomen hos nötkreatur, är sällsynta men alltid dödliga sjukdomar i hjärnan. En central bov är ett normalt hjärnprotein, kallat prionprotein, som kan veckas fel och sprida skada från cell till cell. Ju mer av detta protein som sitter på ytan av nervceller, desto lättare får sjukdomen fäste. Denna studie syftade till att kartlägga, över hela genomet, vilka gener som styr hur mycket prionprotein som visas på utsidan av neuronliknande celler. Den kartan kan hjälpa forskare att utforma nya sätt att sänka detta protein och potentiellt bromsa flera neurodegenerativa sjukdomar.
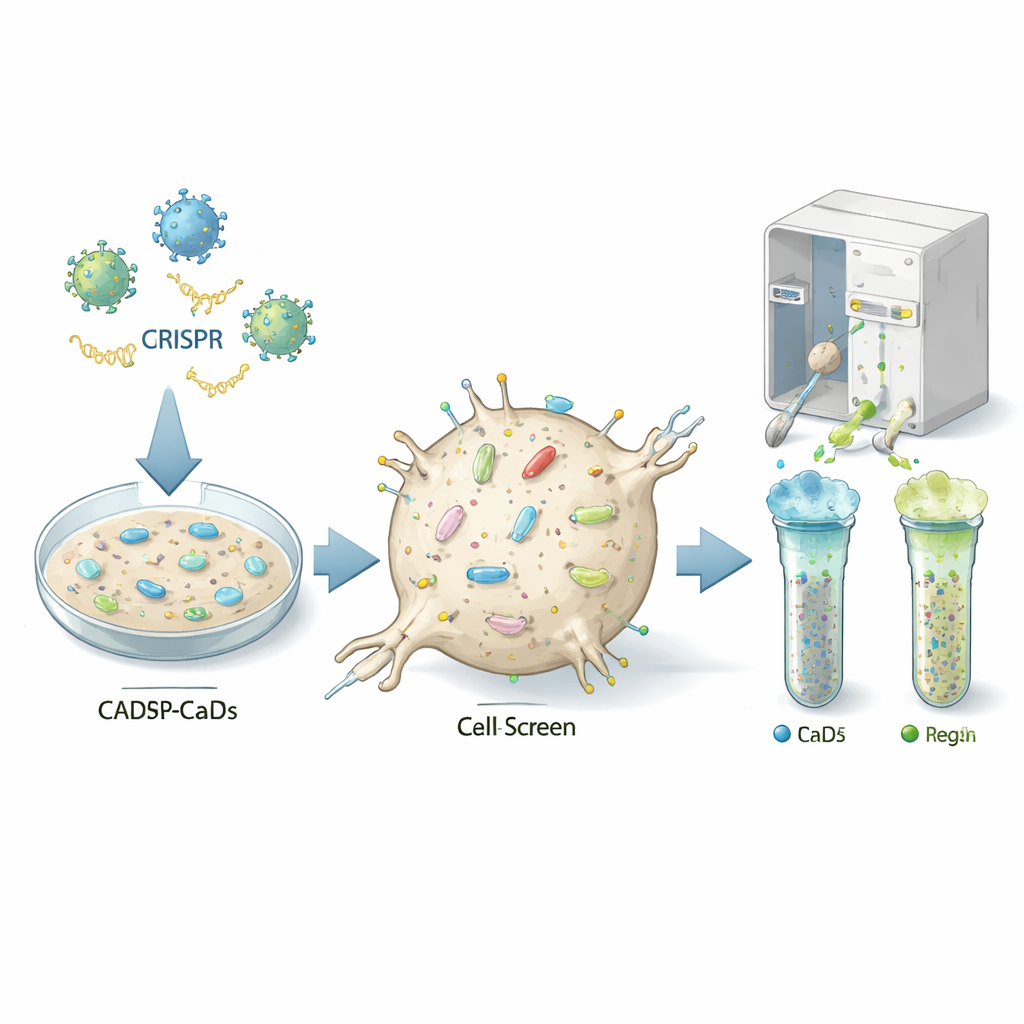
Att hitta cellens knappar för kontroll
Författarna använde en kraftfull genredigeringsmetod kallad CRISPR för att stänga av nästan varje gen, en efter en, i en mus neuronliknande cellinje som kan infekteras av prioner (kallad CAD5). Varje cell fick en olika genetisk "träff", så den resulterande populationen innehöll miljontals varianter, var och en saknad en specifik gen. Teamet färgade sedan cellerna med fluorescerande antikroppar som känner igen det normala prionproteinet på cellytan och använde en cellsorteringsmaskin för att skilja ut celler med ovanligt låga eller höga nivåer av detta protein. Genom att sekvensera vilka guide-RNA som var berikade i de låga respektive höga grupperna kunde de härleda vilka utstängda gener normalt fungerar som på- eller av-knappar för prionproteinet på cellytan.
Två celltillstånd, överlappande svar
Neuroner ser inte alla likadana ut eller beter sig likadant under sin livstid, så forskarna undersökte om samma gener styr prionprotein i olika celltillstånd. CAD5-celler kan hållas i ett snabbväxande, mindre specialiserat tillstånd eller pressas, genom att ta bort serum från odlingsmediet, att anta en mer mogen, neuronlik form. Teamet körde samma genomövergripande CRISPR-skärm i båda tillstånden. I odifferentierade (mindre mogna) celler validerade de 46 gener som ökar, och 21 som minskar, ytuttrycket av prionprotein när de är aktiva. I differentierade (mer neuronlika) celler bekräftade de 41 positiva och 13 negativa regulatorer. Tjugotre gener — främst de som hjälper till att fästa ett lipidt "ankare" på proteinet — delades mellan båda celltillstånden, vilket lyfter fram en kärnregulatorisk maskineri som fungerar oberoende av mognadsgrad.
Viktiga monteringslinjer som spelar störst roll
Ytterligare analys visade att många av de nyligen identifierade generna tillhör kända cellulära "monteringslinjer" som modifierar proteiner när de färdas mot cellytan. En huvudväg bygger GPI-ankaret, en liten fettrik struktur som förankrar prionproteinet i cellmembranets yttre sida. Att störa nästan vilket steg som helst i denna väg minskade hur mycket prionprotein som nådde ytan, i både omogna och mogna celler. En andra väg involverar N-länkad glykosylering, där komplexa sockergrupper läggs till proteiner när de passerar genom cellens interna membran. Gener i denna sockerläggande väg framträdde främst som viktiga i de mindre mogna cellerna. När forskarna behandlade celler med små molekyler som blockerar specifika glykosyleringssteg sjönk nivåerna av ytligt prionprotein med ungefär en tredjedel utan att döda cellerna, vilket bekräftade de genetiska fynden.
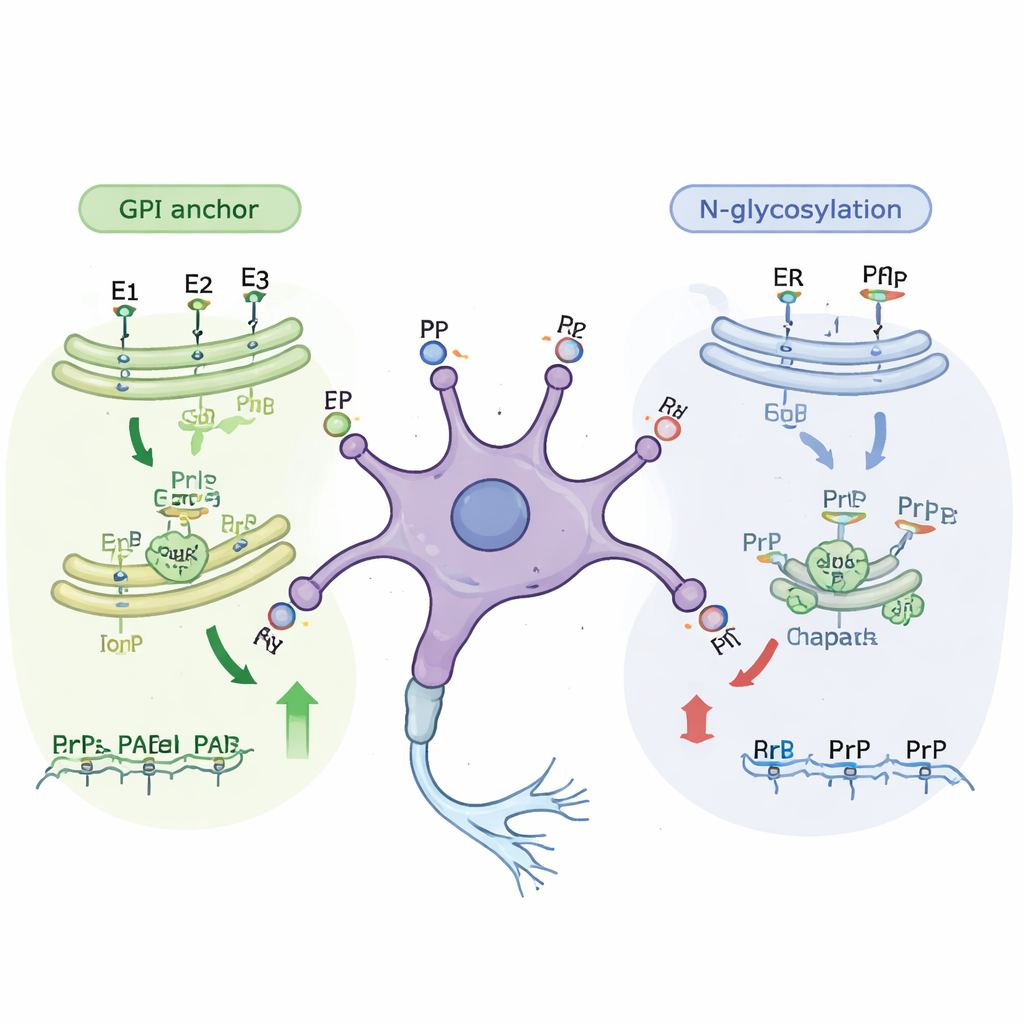
Hjälpproteiner och stressrespons
Skärmarna belyste också molekylära chaperoner — proteiner som hjälper andra proteiner att veckas korrekt — som viktiga prionregulatorer. Särskilt Hspa5 (även kallad BiP), en central chaperon i cellens proteinveckningskompartment, framträdde som en positiv regulator i de mer neuronlika cellerna. När forskarna använde ett läkemedel för att hämma Hspa5 föll nivåerna av ytligt prionprotein i båda celltillstånden, återigen utan uppenbar skada på cellerna. Andra träffar inkluderade gener involverade i transport av proteiner genom cellen, styrning av geners aktivitet och flera proteiner kopplade till synapsfunktion och andra hjärnsjukdomar såsom Alzheimers och ALS. Tillsammans visar dessa resultat att nivåerna av prionprotein på cellytan formas av ett nätverk av vägar som spänner över proteinproduktion, modifiering, transport och kvalitetskontroll.
Vad detta betyder för framtida behandlingar
Detta arbete tillhandahåller den första omfattande katalogen över gener som styr hur mycket prionprotein som visas på ytan av neuronliknande celler som är mottagliga för prioninfektion. Några av dessa gener, särskilt de i GPI-ankarets och N-glykosyleringsvägarnas samt Hspa5-chaperonsystemets komponenter, framträder som lovande startpunkter för läkemedelsupptäckt: att dämpa deras aktivitet bör minska mängden prionprotein tillgängligt för felveckning, och tidigare studier visar att även partiella minskningar kan avsevärt fördröja sjukdom hos djur. Samtidigt understryker de tydliga skillnaderna mellan omogna och mogna celler att hjärncellens tillstånd spelar roll när man väljer måltavlor. Medan mer arbete behövs för att testa hur manipulation av dessa gener påverkar faktisk prioninfektion och andra neurodegenerativa tillstånd i levande hjärnor, erbjuder denna studie en färdplan över cellulära spakar som forskare kan utforska för att bromsa eller förebygga dessa förödande sjukdomar.
Citering: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
Nyckelord: prionprotein, CRISPR-skärm, neurodegeneration, proteinglykosylering, GPI-ankare