Clear Sky Science · sv
Tryckförstärkt dubbelsolid-yta ultrarapidkylning förbättrar återhämtning efter upptining i hepatocyter och precisionsskurna leverfragment
Varför det är viktigt att frysa levervävnad
Att hålla celler och vävnader vid liv utanför kroppen är ett av modern medicins tysta arbetsdjur. Frysta leverceller hjälper forskare att testa nya läkemedel, modellera sjukdomar och kan en dag reparera sviktande organ. Men att frysa levande material är knepigt: om iskristaller växer inne i eller mellan celler rivs ömtåliga strukturer sönder. Denna studie undersöker ett nytt sätt att frysa leverceller och tunna leverbitar så snabbt och under så kontrollerade förhållanden att skadliga iskristaller knappt hinner bildas.
Problemet med is och kemiska skyddsmedel
Konventionell kryopreservering förlitar sig på två ofullkomliga verktyg: kyla och kemikalier. När prover kyls tenderar vatten att bilda is, vilket kan punktera membran och störa vävnader. För att motverka detta tillsätter forskare kryoprotektiva ämnen, såsom dimetylsulfoxid (DMSO), som hjälper vattnet att stelna till ett glasliknande tillstånd istället för kristallin is. Men vid de höga koncentrationer som vanligtvis används kan dessa ämnen själva förgifta celler eller orsaka skadliga svullnader och krympningar när de rör sig in och ut ur vävnaden. Författarnas mål var att minska mängden DMSO som behövs samtidigt som man fortfarande undviker skadlig isbildning, vilket skulle göra levercell- och vävnadsförvaring säkrare och mer praktisk.
Ett nytt sätt att pressa och kyla samtidigt
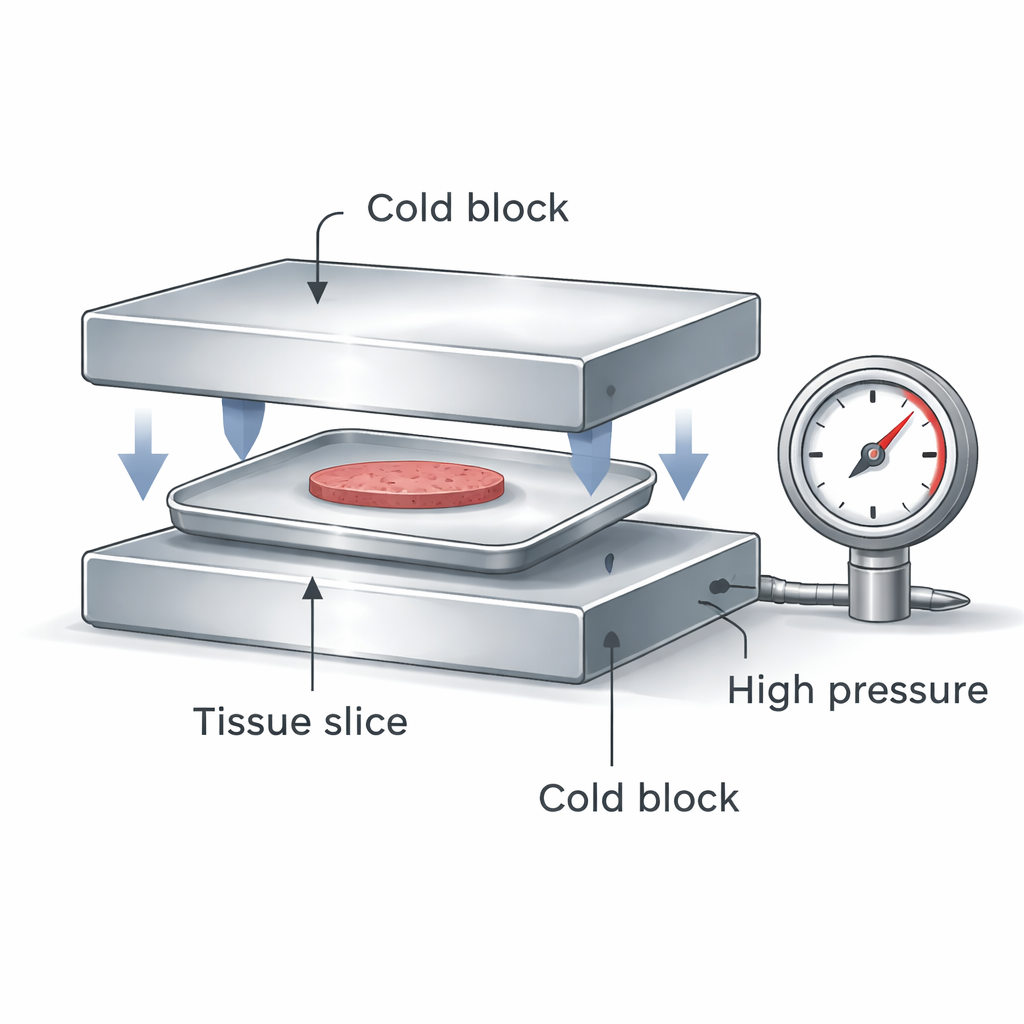
Gruppen designade en kompakt anordning som sandwichar en förseglad, platt aluminiumbehållare med leverceller eller precisionsskurna leverbitar mellan två extremt kalla metallblock. När blocken pressar ihop gör de två viktiga saker samtidigt: de skapar högt tryck inuti den förseglade behållaren och de avleder värme från provet både uppifrån och underifrån. Högt tryck förändrar vattnets beteende så att is bildas vid lägre temperaturer och lösningen blir glasartad lättare. Dubbelkontakt ger en mycket snabbare och mer jämn kylhastighet än att helt enkelt doppa ett plastprov i flytande kväve, och den förseglade behållaren håller provet isolerat från kontaminering.
Hitta balanspunkten för säkerhet och överlevnad
För att se om metoden var tillräckligt skonsam för levande material kontrollerade forskarna först att aluminiumbehållaren i sig inte skadade leverderiverade HepG2-celler under de korta handteringstider som användes. Cellöverlevnaden förblev i stort sett oförändrad. De exponerade sedan dessa celler för olika DMSO-nivåer före frysning och bekräftade en välkänd avvägning: mer DMSO undertrycker isbildning bättre men blir uppenbart giftigt vid 30 %, medan 20 % förblir i stort sett tolererbart. För musleverbitar testade de hur mycket tryck vävnaden kunde tåla i frånvaro av frysning. Korta pulser upp till 150 megapascal hade liten effekt på vitaliteten, men 200 megapascal orsakade ungefär en 30 % minskning, vilket markerade en övre gräns för säker drift.
Bättre bevarade leverbitar efter upptining
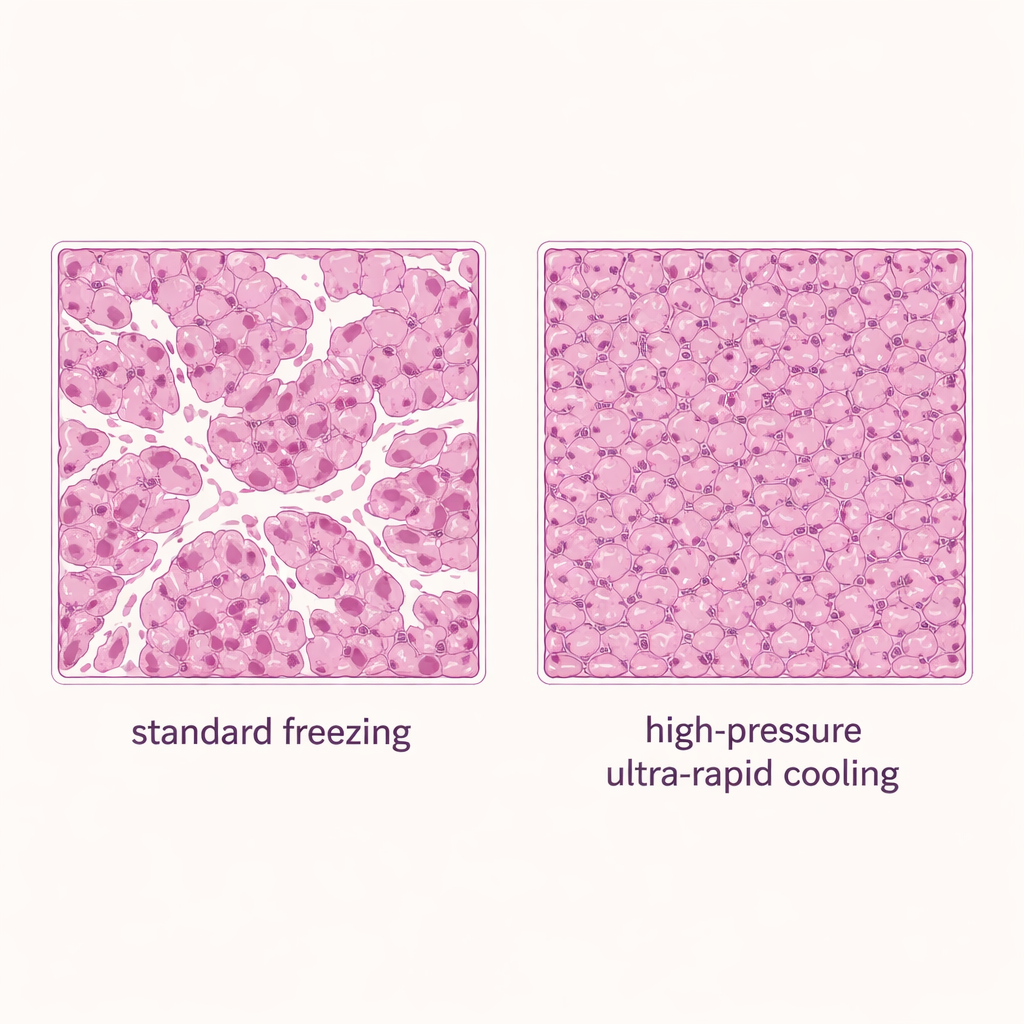
Med säkra intervall fastställda jämförde författarna tre frysningsmetoder för leverbitar: standard nedsänkning av den förseglade behållaren i flytande kväve (en konvektions- eller vätskebaserad metod), solid-ytkyln ing utan tillsatt tryck, och solid-ytkyln ing med högt tryck vid 150 megapascal. Alla grupper använde 20 % DMSO. Tryckassisterad metod gav bäst resultat: cirka 80 % av vävnadens ursprungliga viabilitet bibehölls, vilket var bättre än både standardfrysning och solid-yta utan tryck. Mikroskopi av färgade vävnadsnitt stödde dessa fynd. Prover frysta genom konventionell nedsänkning visade många öppna vita utrymmen—kännetecken på is-skada—medan tryckförstärkt solid-ytkyln ing gav tätare, mer intakt vävnad med betydligt färre mellanrum.
Vad detta betyder för framtida vävnadsförvaring
Sammanfattningsvis visar studien att genom att pressa en förseglad, aluminiuminkapslad leverbit mellan två ultrakalla block under noggrant kontrollerat högt tryck kan man avsevärt förbättra hur väl vävnaden klarar upptining. Genom att kombinera snabbare, jämnare kylning med tryckpåverkat vattens beteende begränsar metoden tillväxten av skadlig is samtidigt som den använder en måttlig, kliniskt bekant koncentration av DMSO. För en lekmannaläsare är slutsatsen att smartare ingenjörsarbete—hur vi paketerar och kyler vävnad—kan vara lika viktigt som de kemikalier vi tillsätter. Denna dubbelsidiga, högtrycksmetod kan bli ett steg mot säkrare, mer pålitlig förvaring av levervävnad och så småningom andra organ för forskning och terapi.
Citering: Amini, M., Benson, J.D. Pressure enhanced dual-solid-surface ultra-rapid cooling improves post-thaw recovery in hepatocytes and precision cut liver slices. Sci Rep 16, 5994 (2026). https://doi.org/10.1038/s41598-026-37136-3
Nyckelord: kryopreservering, levervävnad, vitrifiering, högtryckskylning, isfri frysning