Clear Sky Science · sv
Identifiering av RBX1 som en regulator av LIPT1-transkription och dess roll i kopparinducerad celldöd i GBM-celler
Varför koppar och hjärntumörer är viktiga
Glioblastoma multiforme är en av de dödligaste formerna av hjärncancer, där de flesta patienter överlever bara en kort tid efter diagnos trots aggressiv kirurgi, strålbehandling och kemoterapi. Denna studie utforskar en oväntad allierad mot dessa tumörer: metallen koppar. Forskarna undersöker en nyligen erkänd form av celldöd som utlöses av koppar och identifierar en molekylär väg som kan hjälpa läkare att utnyttja denna process för att försvaga tumörer och potentiellt stärka immunsystemets angrepp mot cancerceller.
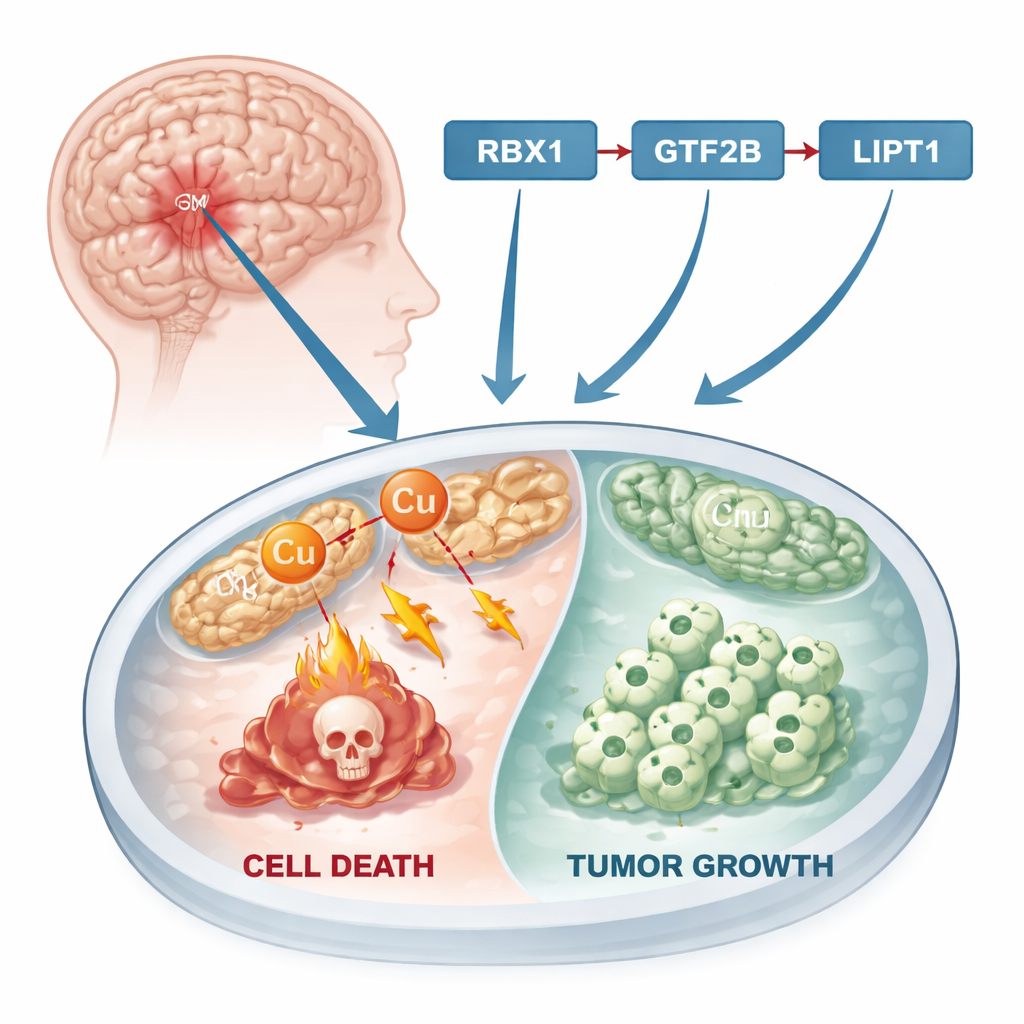
Ett nytt sätt för celler att dö
I årtionden har cancerforskning fokuserat på välkända former av celldöd såsom apoptos, där skadade celler tyst stänger ner sig själva. Nyligen upptäckte forskare en annan väg som kallas kopparinducerad celldöd, eller ”cuproptos”. I denna process byggs överflödig koppar upp i cellens energifabriker, mitokondrierna. Där stör den nyckelproteiner så att giftiga klumpar bildas och slutligen dödar cellen. Eftersom många tumörer har förändrad metallmetabolism och högre kopparnivåer än normala vävnader, erbjuder cuproptos en potentiell svag punkt: om forskare kan driva tumörceller mot denna koppardrivna undergång kan de kanske bromsa eller stoppa cancerutvecklingen.
Framhävning av en nyckelgen i glioblastom
Författarna började med att undersöka en grupp gener som redan är kända för att vara involverade i cuproptos och frågade hur de beter sig i glioblastomprover jämfört med normal hjärnvävnad. En gen i synnerhet, kallad LIPT1, stack ut. Den var mer aktiv i glioblastomvävnad och i flera glioblastomcellinjer än i normala hjärnceller. Viktigt är att patienter vars tumörer hade högre LIPT1-aktivitet tenderade att ha längre tid utan återfall efter behandling. Höga LIPT1-nivåer kopplades också till en större närvaro av CD8 T‑celler, immunsystemets frontlinjekämpare mot cancer, vilket tyder på att denna gen kan hjälpa till att göra tumörmiljön mer sårbar för immunsvar.
Vad händer när koppardödsknappen dämpas
För att testa om LIPT1 verkligen påverkar koppardriven celldöd exponerade teamet glioblastomceller för en kopparbärande läkemedelskombination som pålitligt utlöser cuproptos. De använde sedan genetiska verktyg för att minska LIPT1‑nivåerna. När LIPT1 undertrycktes blev tumörcellerna mer motståndskraftiga mot kopparinducerad död, överlevde bättre och visade starkare förmåga att migrera och invadera — beteenden som förknippas med mer aggressiv cancer. I blandade kulturer av tumörceller och mänskliga CD8 T‑celler minskade sänkningen av LIPT1 även frisättningen av immunsignalmolekyler och gjorde cancercellerna svårare för T‑celler att förstöra. Tillsammans visar dessa experiment att LIPT1 ökar känsligheten för kopparinducerad död och stödjer antitumör immunaktivitet.
Följa kommandokedjan upp till RBX1
Nästa utmaning var att förstå varför LIPT1 är uppreglerat i glioblastom. Genom att kombinera flera stora gen- och proteindatabaser identifierade forskarna en transkriptionsfaktor — en sorts huvudströmbrytare för gengenuttryck — kallad GTF2B som binder nära LIPT1-genen och sannolikt ökar dess uttryck. De frågade sedan vad som kontrollerar GTF2B själv. Ett andra protein, RBX1, framträdde som en stark kandidat. RBX1 är en del av cellens märknings- och nedbrytningssystem som markerar andra proteiner för förstörelse. I glioblastomceller var RBX1‑nivåerna lägre än i normala hjärnceller, medan GTF2B och LIPT1 var högre. Laboratorieanalyser visade att RBX1 kan fästa små ”förstör mig”-taggar på GTF2B, vilket leder till dess nedbrytning; när RBX1 ökade sjönk GTF2B‑nivåerna och LIPT1‑aktiviteten, och blockering av cellens nedbrytningsmaskineri återställde denna effekt.
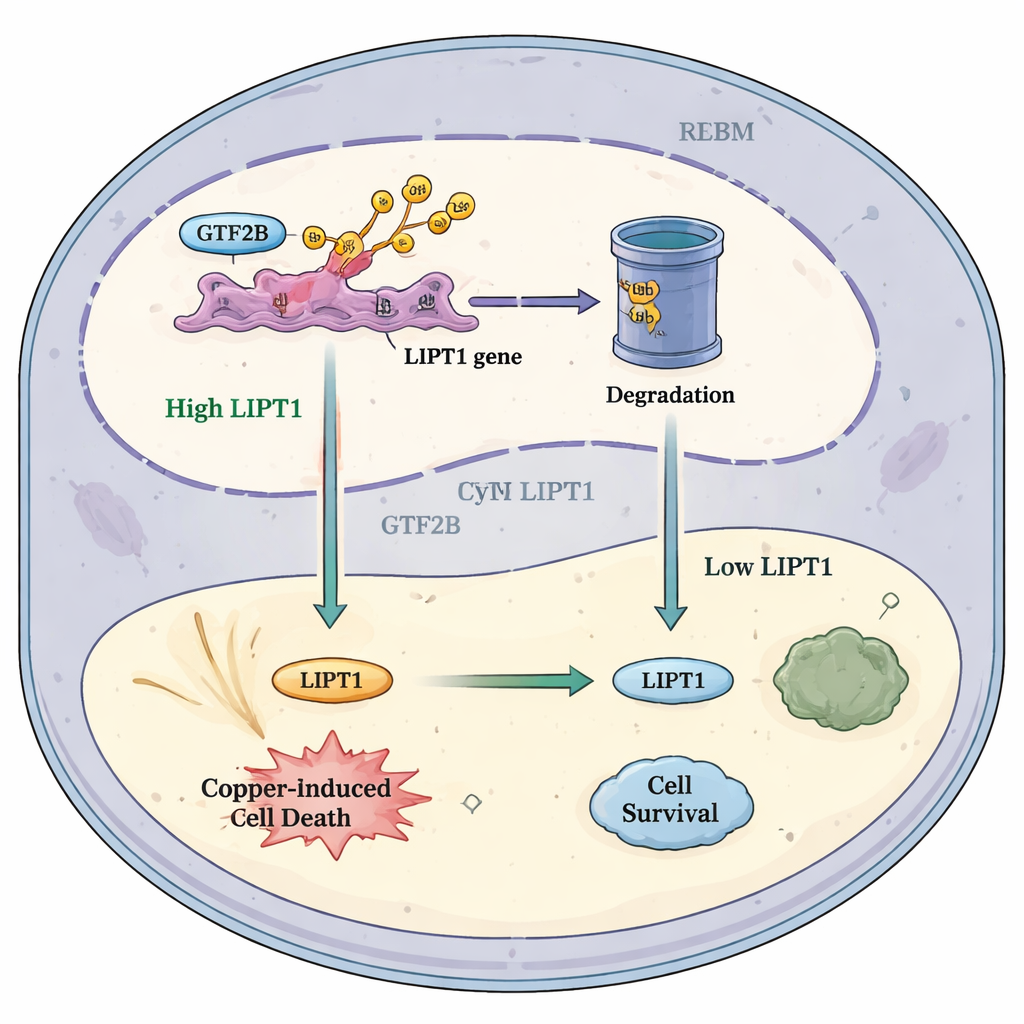
Hur denna väg kan hjälpa framtida behandlingar
Sammantaget föreslår författarna en enkel modell: under friska förhållanden håller RBX1 GTF2B i schack och begränsar hur starkt det aktiverar LIPT1-genen. I glioblastom innebär reducerat RBX1 att mindre GTF2B bryts ner. Extra GTF2B ökar då LIPT1, vilket ökar tumörcellernas känslighet för kopparinducerad död och lockar fler cancerbekämpande immunceller. Denna modell tyder på att noggrann finjustering av RBX1–GTF2B–LIPT1‑vägen, eventuellt tillsammans med kopparinriktade läkemedel och immunterapier, kan rubba balansen i hjärntumörer mot självförstörelse. Även om mycket arbete återstår innan denna idé kan nå patienter, framhäver studien en lovande mötespunkt mellan metallbiologi, genreglering och cancerimmunologi som kan öppna nya terapeutiska vägar för en av de mest envisa cancerformerna.
Citering: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Nyckelord: glioblastom, kopparinducerad celldöd, LIPT1, tumörimmunologi, RBX1-väg