Clear Sky Science · sv
Integrering av maskininlärning och fysikbaserad modellering för prediktiv design av gemcitabin‑lastade nanokompositer
Smartare cancerläkemedel genom design
Cancerläkemedel som gemcitabin kan rädda liv, men beter sig ofta mer som trubbiga verktyg än som precisionsinstrument: de bryts ner snabbt, missar sina mål och ger hårda biverkningar. Denna studie undersöker hur datorer kan hjälpa forskare att ”förtesta” nya små bärarsystem på skärmen istället för enbart i laboratoriet, för att göra gemcitabinbehandlingar mer effektiva, längre verkande och potentiellt säkrare för patienter.
Varför små bärare spelar roll
Traditionell cytostatikabehandling översvämmar kroppen med läkemedelsmolekyler som cirkulerar överallt, inte bara i tumörer. Nanokompositer — konstruerade partiklar tusentals gånger mindre än ett sandkorn — erbjuder ett sätt att paketera gemcitabin så att det skyddas i blodomloppet och levereras mer direkt till cancercellerna. Två nyckeltal avgör i stort om en design är användbar. Laddningseffektivitet talar om hur mycket läkemedel som hamnar inne i varje partikel, medan inkapslingseffektivitet mäter vilken andel av utgångsläkemedlet som faktiskt fastnar istället för att gå förlorad. Höga värden för båda betyder färre injektioner, mindre bärarmaterial och större chans att slå hårt mot tumören utan att överbelasta resten av kroppen.
Från trial-and-error till datastyrd design
Att designa dessa nanobärare för hand är som att försöka stämma en radio med hundratals rattar — partikelstorlek, ytladning, material, beläggningar och tillverkningsmetoder interagerar alla på komplexa sätt. Hittills ändrade forskare mest en eller två parametrar åt gången och mätte resultatet, en långsam och kostsam cykel som bara avslöjar en liten del av helheten. I det här arbetet samlade författarna 59 noggrant granskade recept för gemcitabin‑bärare från vetenskaplig litteratur och kompletterade dem med ytterligare fysikbaserade exempel genererade på datorn. Denna kombinerade datamängd gjorde det möjligt att testa flera maskininlärningsmetoder — datorprogram som lär sig mönster ur data — för att förutsäga laddnings‑ och inkapslingseffektivitet utifrån designvalen ensam.
Låta fysiken styra algoritmerna
De flesta maskininlärningssystem är kraftfulla kurvanpassare: de kan hitta mönster men vet inte när ett svar bryter mot naturens lagar. För att undvika orealistiska förutsägelser byggde forskarna en hybridmetod som blandar data med grundläggande fysiska regler om hur läkemedelsmolekyler rör sig, binder och håller jämvikt i ett slutet system. I deras ramverk straffas försiktigt varje förutsägelse som till exempel skulle innebära att man skapar mer läkemedel än ursprungligen tillsattes, eller som ignorerar hur molekyler diffunderar genom ett material, under träningen. Detta "fysikinformerade" angreppssätt styr modellen mot svar som är kemiskt och fysikaliskt rimliga, särskilt i delar av designrymden där verkliga mätningar är knappa.
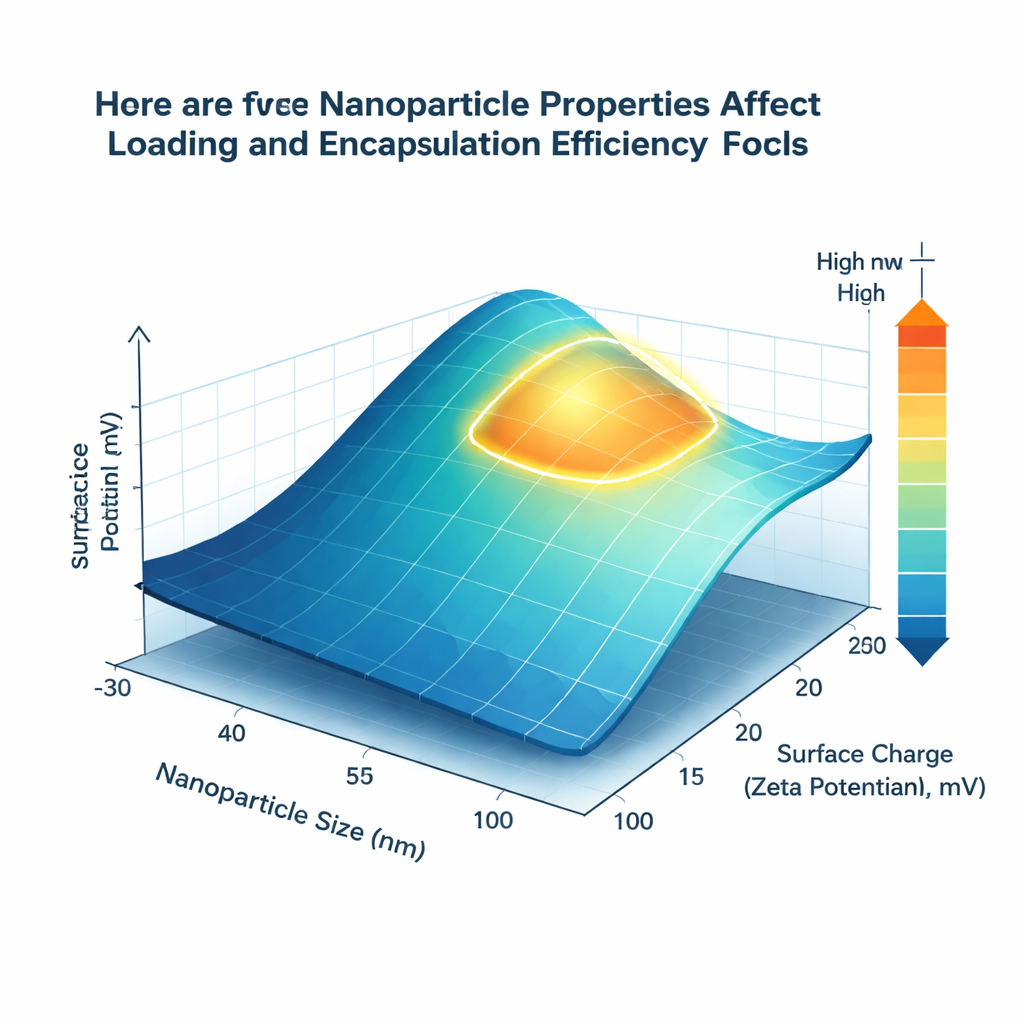
Vad modellerna upptäckte
Bland de testade teknikerna gav en avancerad ensemblealgoritm kallad XGBoost de mest precisa prognoserna och matchade väl rapporterade experimentella resultat för båda nyckeleffektiviterna. Men utöver noggrannhet ville teamet ha förståeliga designregler. Med en metod kallad SHAP, som rangordnar hur starkt varje faktor trycker prognosen uppåt eller nedåt, fann de att partikelstorlek och ytladning konsekvent dominerar prestandan. Nanobärare i storleksintervallet ungefär 80 till 150 nanometer i diameter erbjöd den bästa balansen mellan yta och inre volym, vilket ökade både laddning och inkapsling. En lätt positiv ytladning, i spannet cirka +15 till +25 millivolt, kopplades till bättre fångst av gemcitabin, troligen eftersom de positivt laddade bäraroytorna interagerar gynnsamt med läkemedlets negativt laddade grupper.
En digital karta för framtida cancerbehandlingar
Slutresultatet är inte ett färdigt läkemedel utan ett kraftfullt planeringsverktyg. Studien levererar en slags "designkarta" som pekar forskare mot nanobärarrecept som sannolikt kan hålla och skydda gemcitabin väl, samtidigt som den undviker miljontals opraktiska kombinationer. Författarna betonar att deras förutsägelser fortfarande måste bekräftas i nya laboratorie‑ och djurstudier, och att deras datamängd — om än noggrant samlad — är blygsam i storlek. Trots det visar detta fysikmedvetna maskininlärningsramverk hur datorer kan hjälpa till att begränsa sökområdet efter bättre cancerläkmedelsbärare, vilket minskar kostnader och påskyndar vägen från idéer till mer precisa, patientvänliga behandlingar.
Citering: Rahdar, A., Fathi-karkan, S. & Shirzad, M. Integrating machine learning and physics-based modeling for predictive design of gemcitabine-loaded nanocomposites. Sci Rep 16, 6268 (2026). https://doi.org/10.1038/s41598-026-37098-6
Nyckelord: nanomedicin, gemcitabin, läkemedelsleverans, maskininlärning, nanopartiklar