Clear Sky Science · sv
MCT1 som en kritisk regulator av insulinsignalering, energihomeostas och podocytfunktion
Varför njurcellernas val av bränsle spelar roll
Våra njurar filtrerar tyst hundratals liter blod varje dag, och mycket av det arbetet vilar på små celler kallade podocyter som omsluter njurens filter. Dessa celler måste ständigt omforma sig för att hålla protein i blodet och avfallsämnen i urinen. Denna studie undersöker hur podocyter får den energi de behöver, vad som händer när en av deras stora ”bränsledingar” blockeras, och varför det kan vara viktigt för vanliga tillstånd som diabetes och njursjukdom. 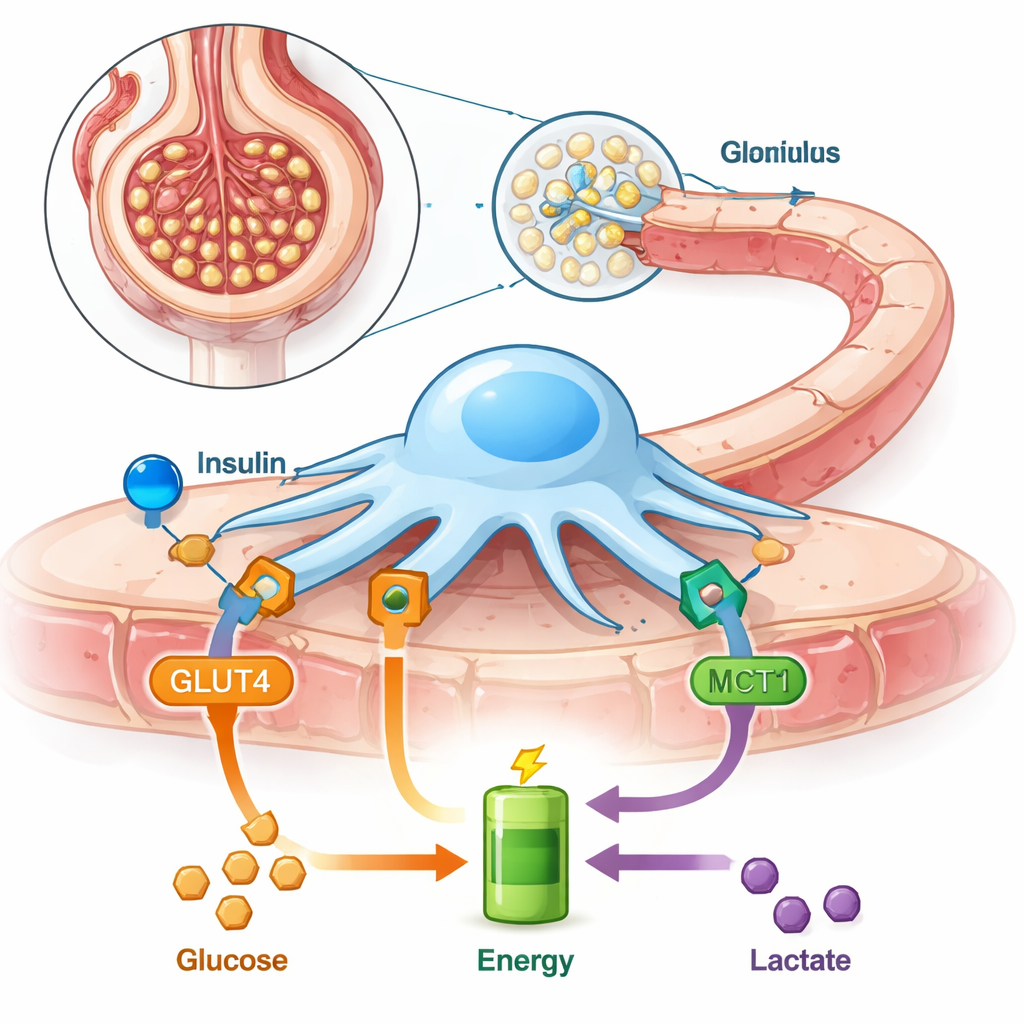
Grindvaktceller vid filtret
Podocyter sitter på utsidan av varje njurfilter och skickar ut fina fotliknande utskott som hakar i varandra och bildar den sista barriären innan urin produceras. Eftersom de ständigt anpassar sin form förbrukar de mycket energi. Till skillnad från många andra celler förlitar sig podocyter i hög grad på sockerupplösning utan syre (en väg kallad glykolys) och de är särskilt känsliga för insulin, som signalerar åt dem att ta upp mer socker från blodet via en transportör kallad GLUT4. Författarna har tidigare visat att podocyter också kan använda laktat, en liten molekyl ofta avfärdad som ”avfall”, vilket antyder att dessa celler är mer flexibla än man tidigare trott.
Laktatdörren: MCT1
Laktat rör sig in och ut ur celler genom speciella transportproteiner. En av de viktigaste är monocarboxylattransportör 1 (MCT1), som kan föra in laktat i celler för att användas som bränsle. I denna studie använde forskarna odlade råttpodocyter och blockerade MCT1 med en kemisk hämnare. De undersökte sedan hur detta påverkade insulins förmåga att driva sockerupptag, hur mycket energi cellerna kunde producera, hur deras inre skelett såg ut och hur ”läckig” barriären blev för ett stort blodprotein kallat albumin. De testade också hela isolerade njurfilter (glomeruli) från råttor för att se hur laktat och MCT1‑blockad ändrade proteinläckage i ett mer intakt system.
När bränsledörren stängs
Blockad av MCT1 gav flera iögonfallande effekter. För det första minskade det hur mycket glukos podocyterna tog upp, både i vila och efter insulinstimulering, och försvagade en viktig växling i insulinsignaleringen (ett protein kallat Akt) utan att störa själva insulinreceptorn. Samtidigt dämpades den normala omlokaliseringen av GLUT4‑transportören mot cellytan. Mätningar av cellernas metabolism visade att den totala energiproduktionen föll när MCT1 blockades, och cellerna skiftade bort från glykolys mot mer syreberoende förbränning i mitokondrierna. Även när insulin eller laktat tillsattes korrigerades inte detta energibrist fullt ut, vilket tyder på att MCT1 är centralt för hur podocyter balanserar sina energikällor. 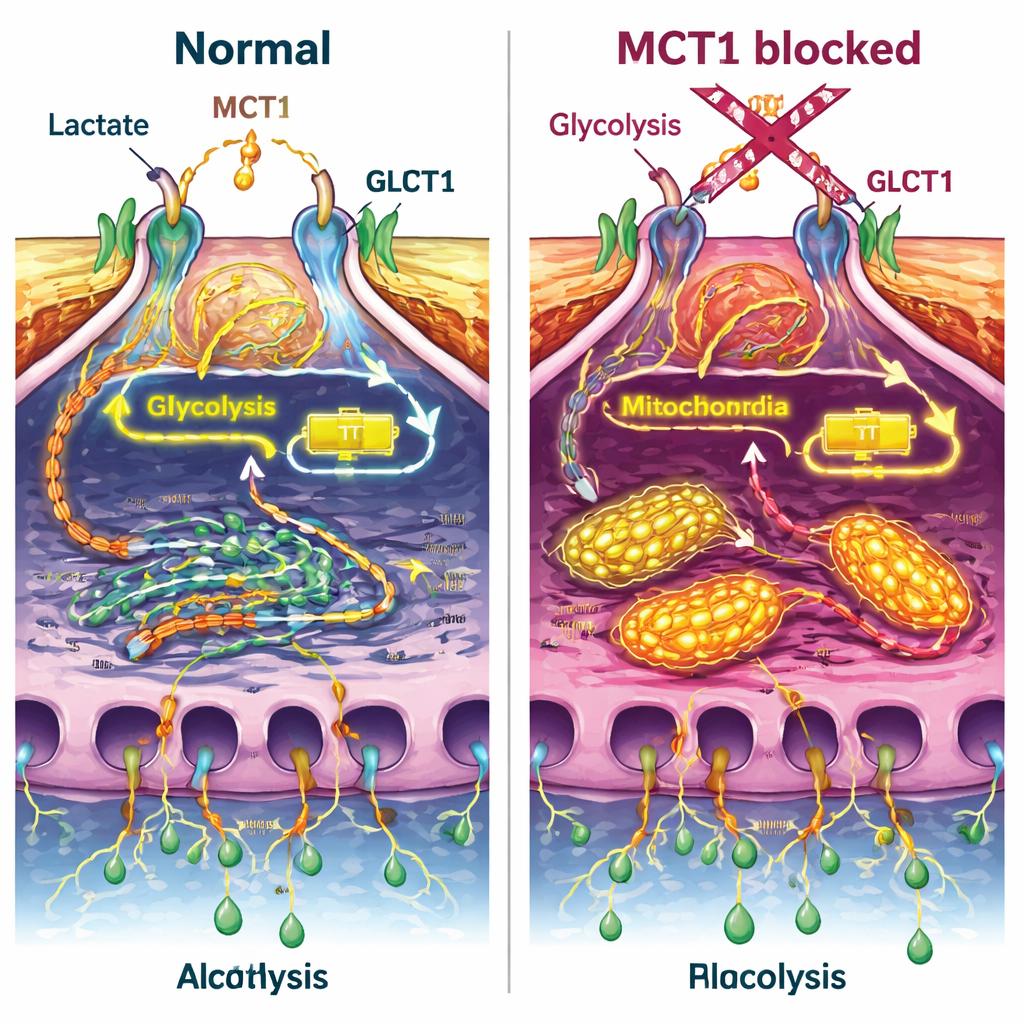
Läckande filter och stressade skelett
Energiförändringarna var tätt kopplade till fysisk skada. När MCT1 blockades släppte podocytlager i odling igenom mer albumin, liknande effekten av insulin ensam. Laktat i sig gjorde barriären mer läckande, och att kombinera laktat eller insulin med MCT1‑blockad höll genomsläppligheten hög. Inuti cellerna blev aktinfilamenten som formar deras struktur mer bundna och oordnade, ett mönster som förknippas med förlust av de fina fotutskotten som bygger upp filtret. Ett annat nyckelprotein, nephrin, som hjälper till att hålla filtret samman och också stöder insulins effekter, minskade eller fellokaliserades när MCT1 hämmdes. I isolerade hela filter från råttnjurar ökade tillsats av laktat snabbt albuminläckaget, och MCT1‑blockad gav en liknande ökning, vilket stöder idén att störd laktathantering direkt försvagar filtret.
Konsekvenser för diabetes och njurhälsa
Författarna föreslår att korrekt rörelse av laktat genom MCT1 är nödvändig för att podocyter ska kunna driva sitt föredragna energiprogram, svara på insulin och upprätthålla en tät filtrationsbarriär. När denna laktat"dörr" störs — genom MCT1‑blockad eller genom kroniskt högt blodsocker som ändrar laktatbalansen — förlorar podocyter metabol flexibilitet, förbrukar mindre socker, blir överberoende av mitokondrier och blir strukturellt instabila och läckande. För människor antyder detta arbete att subtila förändringar i hur njurceller hanterar laktat kan bidra till insulinresistens och tidig njurskada långt innan den övergripande njurfunktionen verkar onormal. Att förstå och i framtiden rikta in sig på detta laktattransportsystem kan öppna nya vägar för att skydda njurfiltren vid diabetes och andra metabola sjukdomar.
Citering: Szrejder, M., Audzeyenka, I., Rachubik, P. et al. MCT1 as a critical regulator of insulin signaling, energy homeostasis and podocyte function. Sci Rep 16, 5906 (2026). https://doi.org/10.1038/s41598-026-37093-x
Nyckelord: njurens podocyter, laktatmetabolism, insulinresistens, glomerulärt filtrationsbarriär, MCT1‑transportör