Clear Sky Science · sv
Automatisk kvantifiering av tumörinfiltrerande lymfocyter med maskininlärning avslöjar prognostiska och immunogenomiska drag i lungcancer
Varför det spelar roll att räkna små immunceller i lungtumörer
Lungcancer är fortfarande en av de dödligaste cancerformerna, men inte alla tumörer beter sig likadant. Vissa är kraftigt bevakade av immunceller som tränger in i tumören, medan andra förblir nästan opåverkade. Dessa tumörinfiltrerande lymfocyter, eller TILs, kan ge ledtrådar om hur en patient kommer att klara sig och om hen kan ha nytta av moderna immunterapier. Utmaningen är att TILs idag vanligtvis räknas för hand i mikroskop, vilket är långsamt och subjektivt. Denna studie ställer en aktuell fråga: kan vi använda maskininlärning för att automatiskt mäta dessa celler på rutinmässiga patologiska snitt, och vad avslöjar det om lungcancerbiologin och patientöverlevnad?
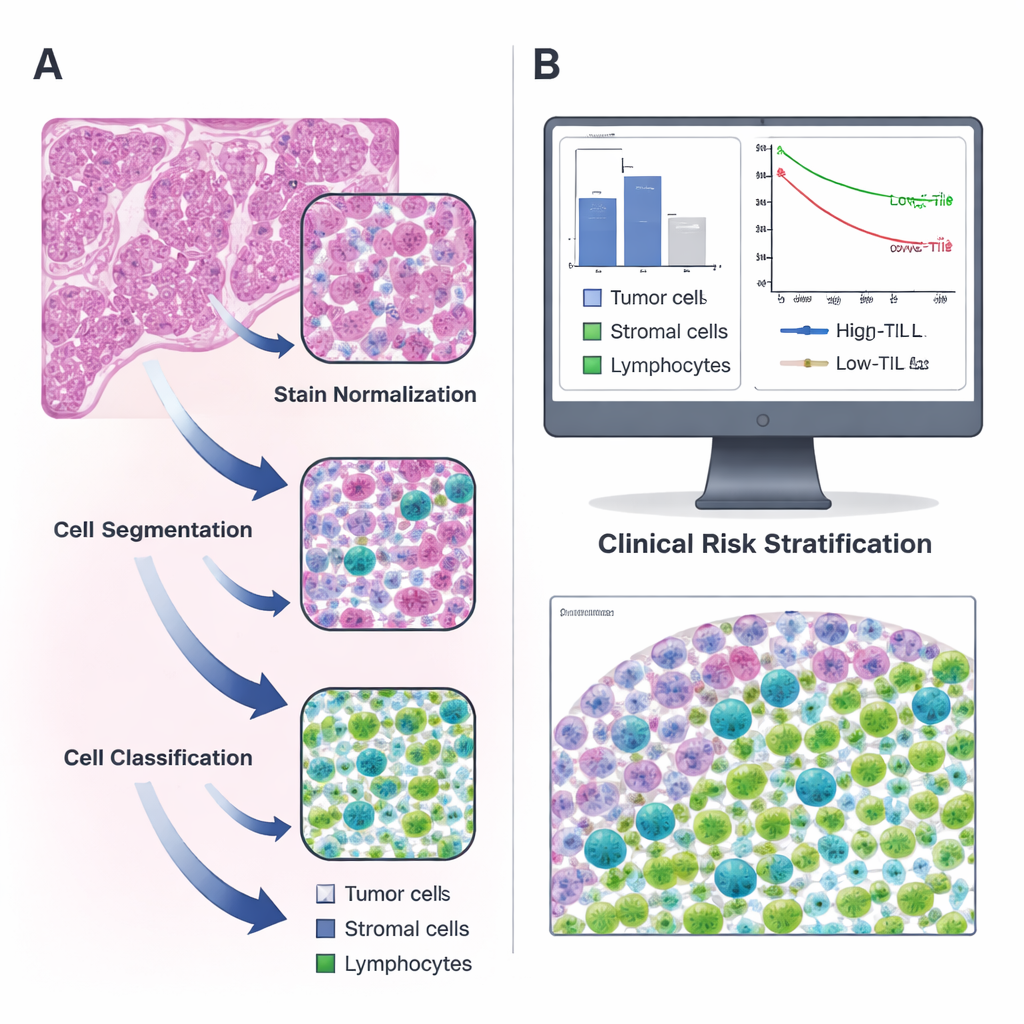
Att förvandla vanliga snitt till digitala kartor
Forskarna fokuserade på lungadenokarcinom, en vanlig typ av lungcancer, och använde offentliga data från The Cancer Genome Atlas tillsammans med en oberoende patientgrupp från deras eget sjukhus. För varje patient analyserade de standardiserade hematoxylin- och eosinfärgade (H&E) vävnadssnitt — de rosa- och lila-bilder som varje patolog känner väl. Med hjälp av öppen källkodsmjukvaran QuPath byggde de en stegvis pipeline: först korrigerade de färgskillnader mellan snitten; därefter använde de en watershed-algoritm för att separera överlappande cellkärnor; slutligen klassificerade en tränad dator varje upptäckt cell som tumör, stödjevävnad (stroma) eller lymfocyt. Två erfarna patologer granskade och korrigerade maskinens arbete upprepade gånger tills den pålitligt kände igen de olika celltyperna på egen hand.
Kopplingen mellan immuncellsantal och patientresultat
När systemet säkert kunde identifiera celler beräknade teamet hur många lymfocyter som fanns per kvadratmillimeter tumörvävnad för mer än 300 patienter. De fann att TIL-nivåerna varierade mycket och i genomsnitt utgjorde de bara en liten andel av alla celler. Med en statistisk metod för att hitta den mest informativa gränsen valde de 135 TILs per kvadratmillimeter som skiljelinje mellan ”höga” och ”låga” TIL-tumörer. Patienter vars tumörer översteg denna tröskel levde längre än de med sparsam immuncellsinfiltration, och detta mönster höll i både ursprungs- och valideringsgrupperna. Med andra ord fångade ett enkelt tal producerat av ett automatiserat verktyg meningsfulla skillnader i överlevnad, i linje med tidigare mer arbetsintensiva studier som förlitade sig på manuell räkning.
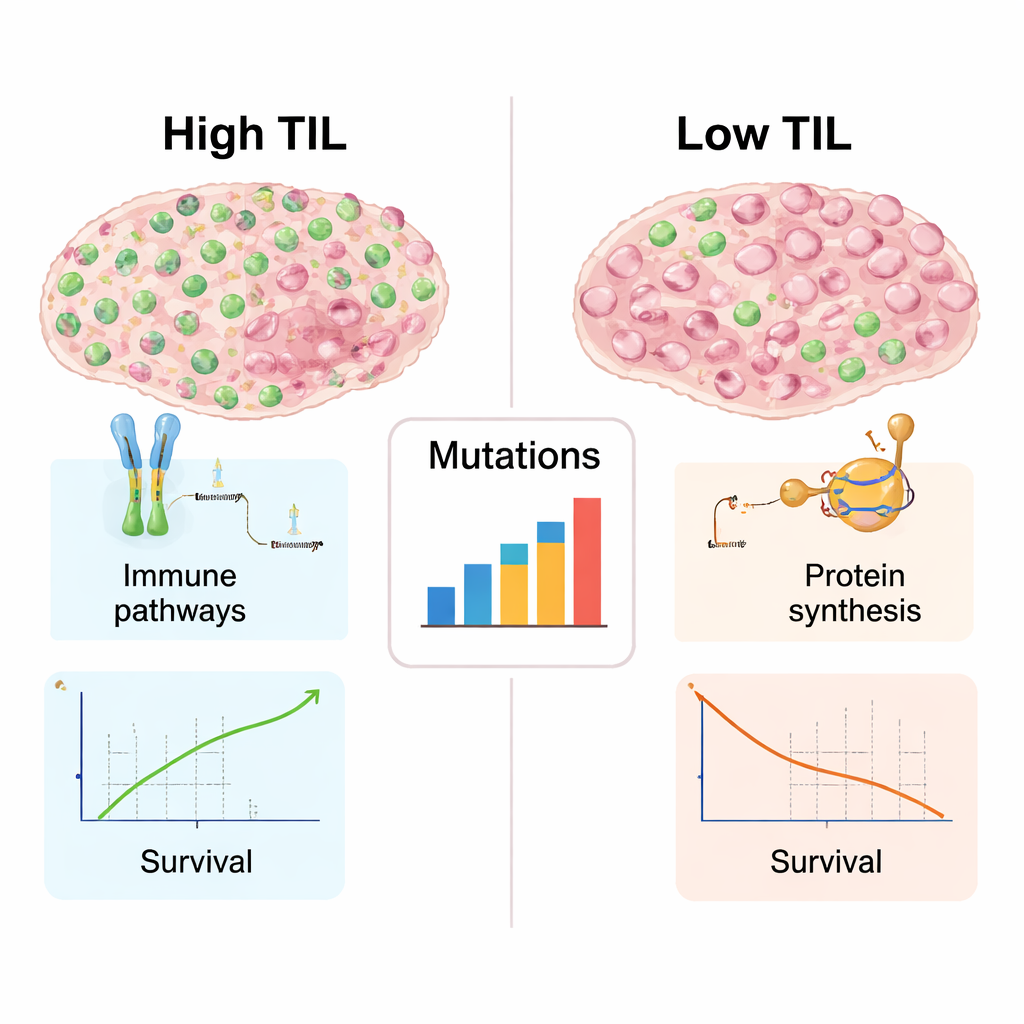
Hur immunrika tumörer ser ut under ytan
Eftersom genetiska och molekylära data fanns tillgängliga för många av dessa tumörer kunde författarna utforska vad som skiljde hög‑TIL från låg‑TIL tumörer bortom rena cellräkningar. Tumörer täta med lymfocyter visade starkare tecken på immunaktivitet: gener involverade i att känna igen onormala proteiner, presentera dem för T‑celler och samordna immunangrepp var alla mer aktiva. Dessa tumörer bar också en bredare blandning av DNA‑mutationer, vilket kan skapa nya mål för immunsystemet. Däremot favoriserade låg‑TIL tumörer gener kopplade till att bygga ribosomer och producera proteiner — ett tecken på intensivt tillväxtmaskineri men relativt låg immunaktivitet. Denna uppdelning speglar kontrasten mellan så kallade ”heta” tumörer, rika på immunceller och mer benägna att svara på immunterapi, och ”kalla” tumörer som immunsystemet till största delen ignorerar.
Att lära en dator förutsäga immunstatus
Teamet gick ett steg vidare och frågade om en kompakt uppsättning bildfunktioner kunde förutsäga om en tumör skulle hamna i hög‑ eller låg‑TIL‑kategorin utan att räkna varje enskild lymfocyt. De sammanfattade subtila texturmönster i snitten — hur pixelintensiteter förändras över små områden — till så kallade Haralick‑funktioner och kombinerade dessa med tumörens kliniska stadium i en random forest‑modell. I korsvalidering separerade denna klassificerare korrekt hög‑ från låg‑TIL tumörer med god noggrannhet, och den behöll rimlig prestanda i en oberoende sjukhusgrupp. Viktigt är att hela metoden körs på vanliga datorer med fritt tillgänglig programvara, vilket tyder på att många patologilabb i princip skulle kunna anta den utan specialiserad hårdvara.
Vad detta betyder för framtida lungcancerbehandling
För en icke‑specialist är huvudbudskapet att en dator kan tränas att läsa rutinmässiga lungcancersnitt på ett sätt som fångar hur starkt immunsystemet engagerat tumören. Höga nivåer av infiltrerande lymfocyter signalerar en mer aktiv immunkamp, ett rikare mutationslandskap och bättre totalöverlevnad. Även om mer forskning krävs — särskilt hos patienter som faktiskt behandlats med immunterapi — kan denna automatiserade metod så småningom hjälpa läkare att snabbt och konsekvent sortera tumörer i immunologiskt ”heta” och ”kalla” kategorier. Det kan i sin tur vägleda beslut om vilka som mest sannolikt har nytta av immunbaserade behandlingar och inspirera nya strategier för att göra kalla tumörer heta.
Citering: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
Nyckelord: lungadenokarcinom, tumörinfiltrerande lymfocyter, maskininlärning, digital patologi, cancerimmunoterapi