Clear Sky Science · sv
Potentiella biomarkörer för tidig parodontal inflammation: undersökning av CD5+ B‑celler, salivariska cytokiner och oral mikrobiom
Varför ditt tandkött påverkar hela kroppen
Blödande tandkött är lätt att bortse från, men inflammationen bakom kan tyst erodera benet som håller tänderna på plats och är kopplad till hjärtsjukdom, diabetes och andra åkommor. Denna studie undersökte om tidiga varningstecken för sådan skada kan hittas i ett vardagligt prov — saliv — tillsammans med vissa immunceller i blodet och blandningen av bakterier som gömmer sig under tandköttskanten. Att hitta pålitliga tidiga markörer skulle kunna hjälpa tandläkare att identifiera högriskpatienter långt innan irreversibel tandförlust inträffar.
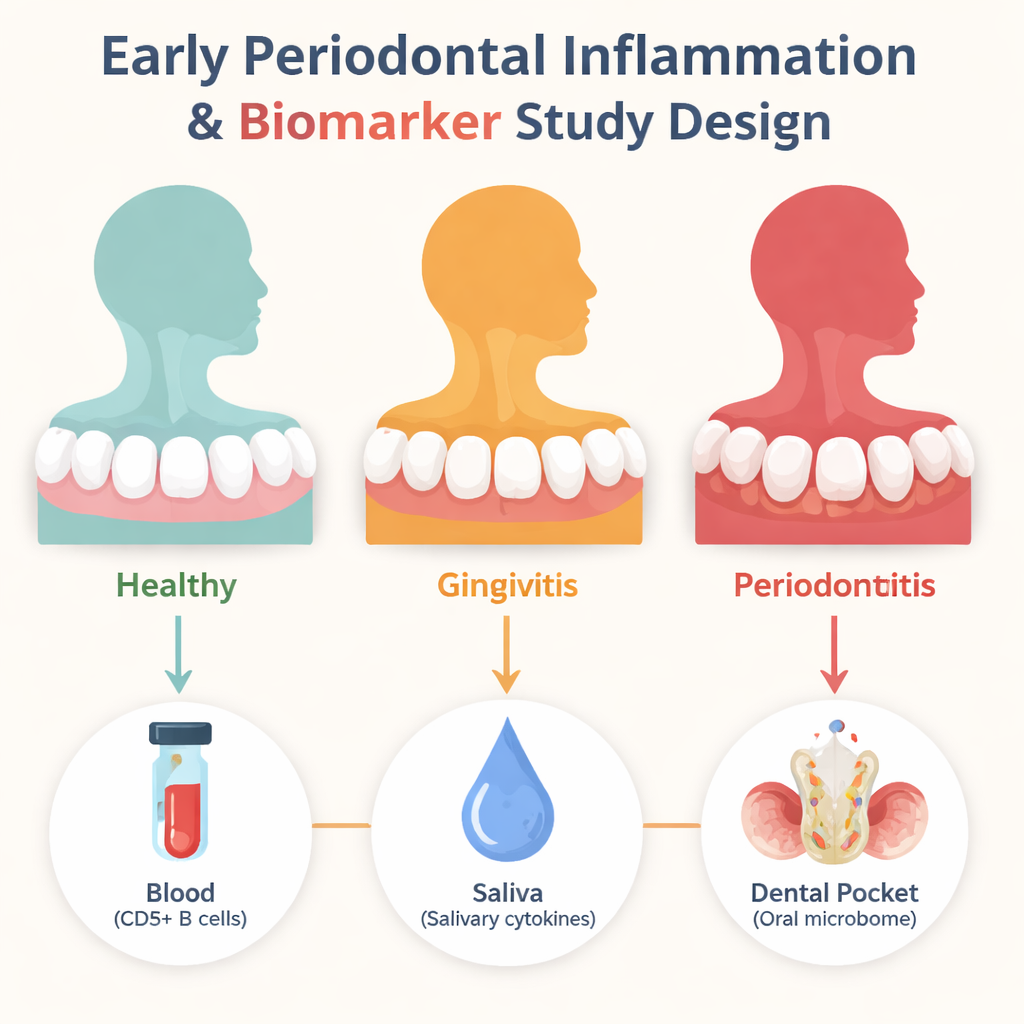
Letar efter tidiga varningslampor
Forskarna fokuserade på tre sorters ledtrådar. För det första granskade de en särskild grupp immunceller i blodet kallade CD5-positiva B‑celler, vilka vid svår tandköttssjukdom och reumatoid artrit har kopplats till bennedbrytning och självförsvarande immunangrepp. För det andra mätte de dussintals signalproteiner, eller cytokiner, i saliv som fungerar som kemiska larm när vävnader irriteras. För det tredje sekvenserade de bakteriellt DNA från vätska tagen från tandköttsfickor för att se hur det orala mikrobiomet förändras när hälsa övergår till gingivit och sedan till måttlig parodontit. Sextio icke‑rökande vuxna grupperades noggrant som friska, gingivit eller måttlig kronisk parodontit utifrån fickdjup, blödning och plackpoäng.
Immunceller i blod förblir tysta
Med tanke på tidigare arbete vid avancerad sjukdom förväntade sig teamet att personer med parodontit redan kunde uppvisa förhöjda nivåer av CD5‑positiva B‑celler i blodomloppet, vilket skulle markera en kroppsomfattande reaktion på kronisk tandköttsinfektion. Överraskande nog var de totala antalen av dessa celler i princip desamma i alla tre grupper, omkring en femtedel av alla B‑celler. Även när forskarna delade upp dem i utvecklingsstadier — omogna, naiva och flera typer av minnesceller — nådde inget tydligt mönster statistisk signifikans. Vissa minnesceller, särskilt de kopplade till långvariga svar, tenderade att vara färre hos personer med sjukdom, vilket antyder att de kan lämna blodet för att ansamlas i inflammerad tandköttsvävnad, men större studier behövs för att bekräfta denna subtila trend.
Saliv och bakterier berättar en starkare historia
Tvärtom speglade saliv och den bakterieflora som finns under tandköttet tydligt sjukdomsstadie. Personer med parodontit hade ungefär dubbla mediannivån av kemokinen IL‑8 i saliven jämfört med friska eller gingivitdeltagare, och var mycket mer benägna att ha detekterbar IL‑17A samt tecken på IL‑6 och IL‑1β‑aktivitet. Dessa molekyler hjälper till att rekrytera immunceller och driva processer som löser upp ben, så deras ökning tyder på att inflammatoriska kretsar redan är aktiva även vid måttlig sjukdom. Samtidigt visade DNA‑sekvensering att friska munnar dominerades av ofarliga, syreälskande bakterier såsom Rothia och Streptococcus. Vid gingivit och särskilt parodontit skiftade balansen mot syreuvilliga, gramnegativa arter inklusive Tannerella, Fusobacterium, Treponema och Fretibacterium, som är kända eller framväxande aktörer i tandköttsunderminering.
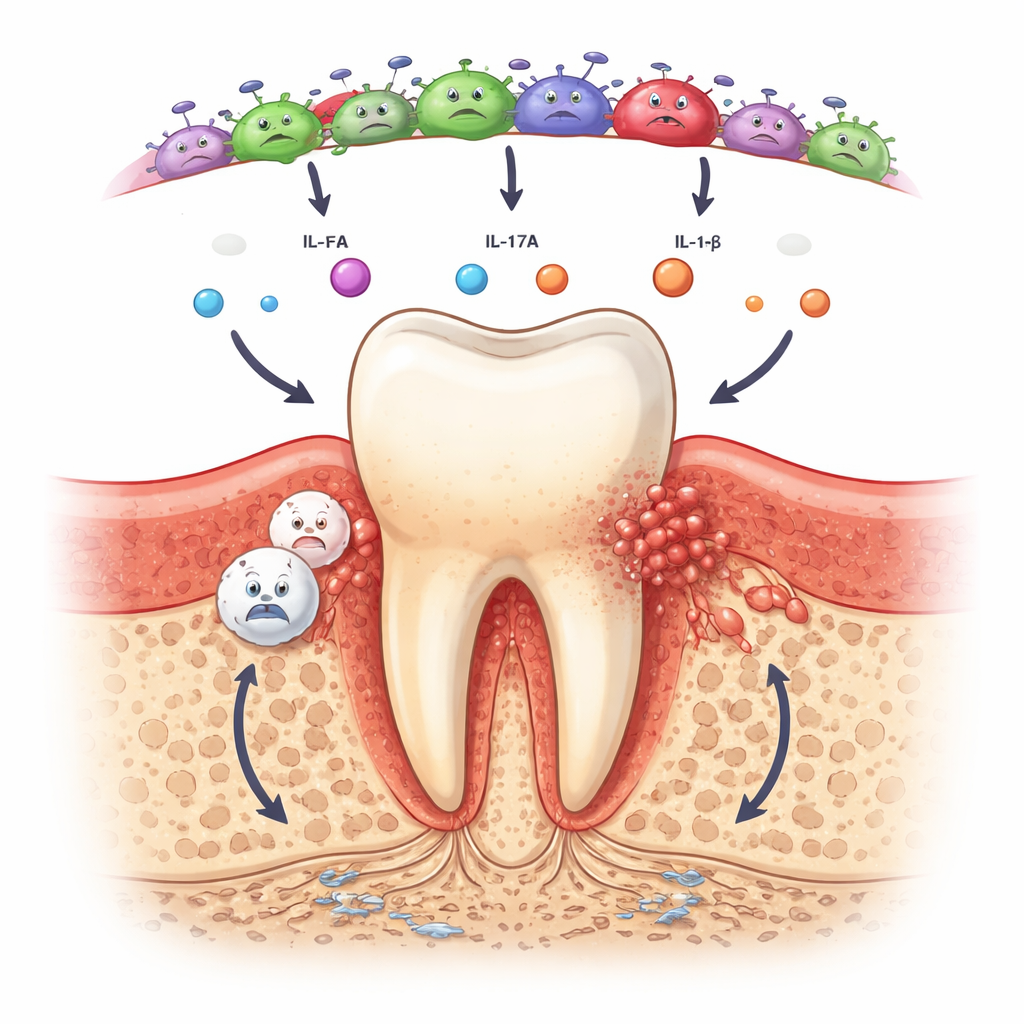
Tidiga tecken på en högriskprofil
Genom att kombinera statistik och maskininlärning identifierade teamet bakteriegrupper som bäst skiljde friska från sjuka platser. Två stammar av Tannerella forsythia och flera Fretibacterium‑arter framstod som särskilt informativa, medan en Rothia‑art signalerade friskare tandkött. En intressant observation kom från gingivitgruppen: nivåer av IL‑8 i saliv följde tätt med förekomsten av en bakteriegenus kallad Megasphaera. Denna koppling syntes inte i friska munnar eller vid fullt utvecklad parodontit, vilket antyder att Megasphaera tillsammans med IL‑8 kan fungera som en indikator i tidigt skede medan skadan fortfarande är begränsad och potentiellt reversibel. Dock var storleken på urvalet modest, och författarna betonar att sådana mönster måste testas i större, långsiktiga studier innan de kan vägleda vård.
Vad detta betyder för patienter
För personer oroade över sitt tandkött är huvudbudskapet att kroppen skickar tidiga biokemiska signaler om problem, men dessa syns mer i lokal saliv och tandköttsflora än i cirkulerande immunceller när sjukdomen fortfarande är måttlig. Rutintester i blod för CD5‑positiva B‑celler kommer sannolikt inte att upptäcka tidig parodontit. Istället kan den mest lovande metoden vara en kombinerad saliv‑ och mikrobiompanel som följer flera cytokiner — särskilt IL‑8 och IL‑17A — tillsammans med nyckelbakterier som Tannerella, Fretibacterium och Megasphaera. Om detta valideras kan ett sådant enkelt munbaserat test hjälpa tandläkare att snabbare identifiera högriskpatienter, anpassa rengöringar och behandlingar och möjligen förebygga både tandförlust och några av de bredare hälsoproblem som är kopplade till kronisk tandköttsinflammation.
Citering: Gottschalk, E.C., Chabanovska, O., Vasudevan, P. et al. Potential biomarkers for early periodontal inflammation: investigating CD5+ B cells, salivary cytokines and oral microbiome. Sci Rep 16, 7192 (2026). https://doi.org/10.1038/s41598-026-37044-6
Nyckelord: tandköttssjukdom, oral mikrobiom, salivariska biomarkörer, parodontit, inflammation