Clear Sky Science · sv
Maskininlärningsbaserad prediktion av blödningsomvandling efter trombektomi med kvantitativ DSA
Varför detta spelar roll för strokepatienter
När någon drabbas av en allvarlig stroke kan läkare ibland avlägsna blodproppen i hjärnans huvudartär med ett litet instrument i en procedur som kallas mekanisk trombektomi. Detta har förändrat strokebehandlingen, men många patienter får ändå dåliga utfall eftersom vissa utvecklar ny blödning i hjärnan. Studien bakom denna artikel ställer en enkel men avgörande fråga: kan vi använda information som redan samlas in i operationssalen, tillsammans med modern maskininlärning, för att förutsäga vilka patienter som mest sannolikt kommer att blöda och behöva extra skydd?
Att se bortom ”artären öppen eller stängd”
I dag bedöms framgång efter trombektomi vanligtvis utifrån om den blockerade artären ser öppen ut igen på angiografi, en slags realtidsröntgenfilm av blodkärl. Men denna grova bedömning avslöjar inte vad som händer i hjärnans små nedströmskärl, där skada och blödning faktiskt uppstår. Några patienter med perfekt utseende stora kärlåterupptagning utvecklar ändå allvarlig hjärnblödning, en komplikation som kallas blödningsomvandling. Författarna antog att mer detaljerade mätningar av blodflödet i dessa små kärl, hämtade från samma angiogram, kan innehålla dolda ledtrådar om vem som är i riskzonen.
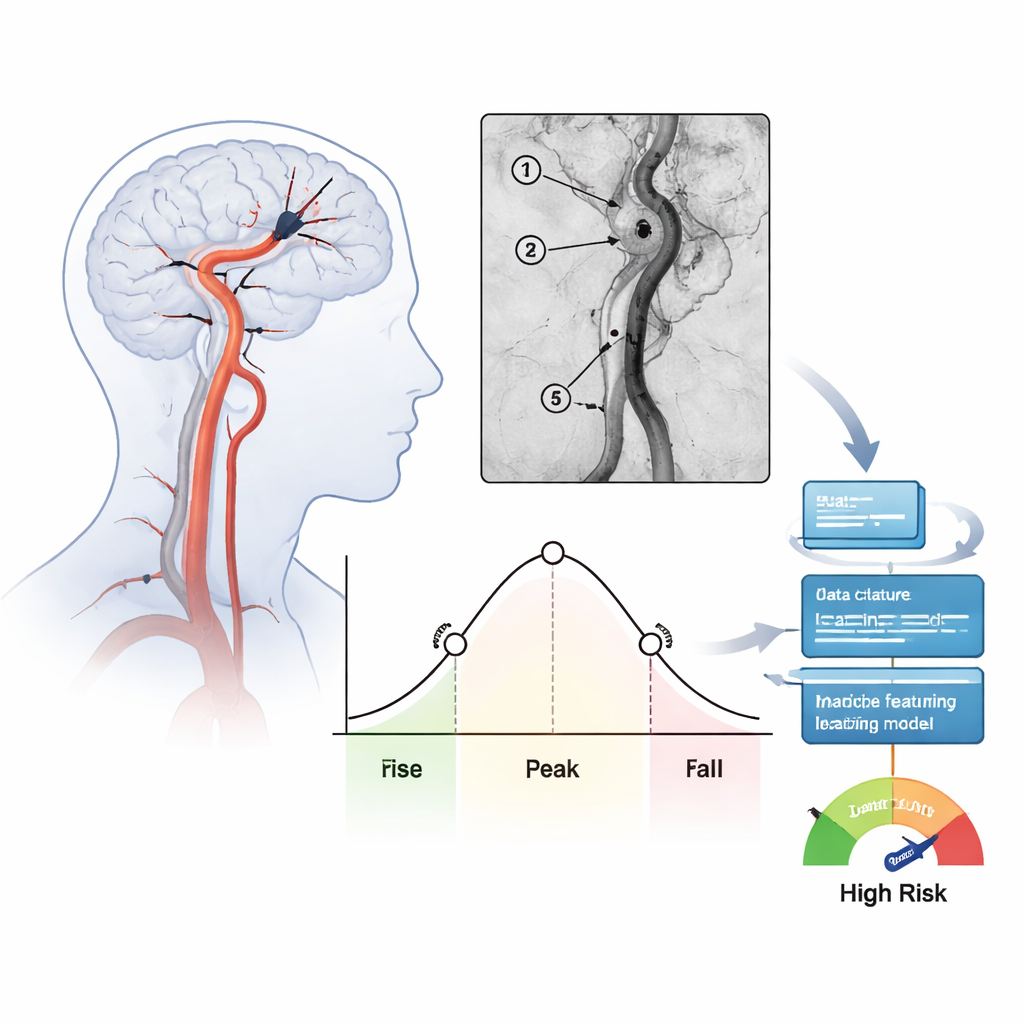
Att förvandla angiogramfilmer till siffror
Forskarteamet studerade 171 personer som behandlats för svåra framre strokefenomen under ett år på ett enda sjukhus. Efter att läkare avlägsnat proppen och återställt flödet spelade de in standardvyer av angiografin och analyserade hur det injicerade kontrastmedlet fyllde och spolades ut i flera nyckelställen längs den behandlade artären. För varje region beräknade de tidsmått som hur lång tid blodet behövde för att passera (mean transit time) och hur bred huvudtoppen av kontrasten var (full width at half maximum). Dessa siffror sammanfattar om blodet rör sig långsamt och jämnt eller skjuter igenom snabbt i en snäv puls. Totalt extraherades 39 sådana flödesegenskaper för varje patient och kontrollerades för konsistens mellan oberoende bedömare.
Att lära datorn känna igen riskmönster
Forskarna använde sedan en uppsättning vanliga maskininlärningsmetoder för att se om dessa flödesegenskaper, ensamma eller i kombination med grundläggande kliniska data som ålder och strokesvårighetsgrad, kunde skilja patienter som senare utvecklade hjärnblödning från dem som inte gjorde det. För att undvika överanpassning använde de först fem olika tekniker för funktionsurval för att plocka ut de mest informativa mätningarna, och de delade upp data upprepade gånger i tränings- och testgrupper med korsvalidering. Bland många testade kombinationer presterade en relativt enkel modell—logistisk regression, finjusterad med ett “Elastic Net”-filter för funktionsval—bäst. När modellen förlitade sig enbart på angiografi-härledda flödesmått separerade den i genomsnitt patienter med och utan blödning med ett area under ROC-kurvan på cirka 0,81. När kliniska faktorer lades till steg prestandan till ungefär 0,86, vilket tyder på att modellen kan bli ett starkt beslutsstöd.
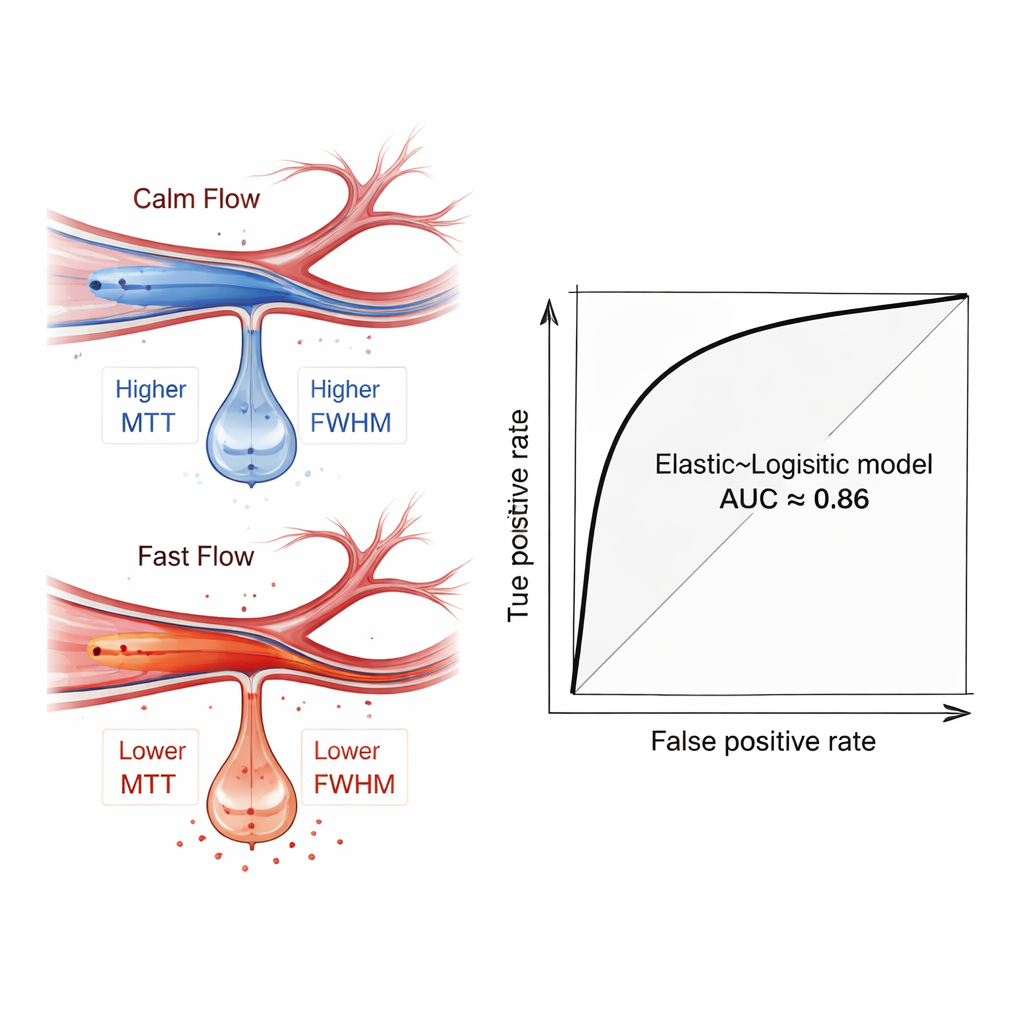
Vad blodflödessignalerna avslöjade
När författarna granskade de tränade modellerna använde de en tolkbarhetsteknik kallad SHAP för att se vilka funktioner som spelade störst roll. Mått som fångade hur lång och hur utspridd flödespulsen var—särskilt i en mer avlägsen gren av media-arterien—stod ut som viktiga prediktorer. Patienter som senare blödde tenderade att visa snabbare, mer fokuserat flöde i dessa distala kärl, vilket återspeglades av lägre transittider och smalare toppar. Detta mönster är ett hemodynamiskt fingeravtryck av ”hyperperfusjon”, ett tillstånd där skör hjärnvävnad, plötsligt översköljd av höghastighetsblod efter att ha varit undernärd, är mer benägen att läcka och blöda. Viktigt är att denna signal framträdde även när enkla gruppjämförelser inte visade dramatiska statistiska skillnader, vilket understryker värdet av multifunktionell, maskinbaserad analys.
Hur detta kan förändra vården vid sängkanten
Eftersom metoden använder bilder som redan tas under trombektomin krävs inga extra skanningar, kontrast eller strålning. När intresseområdena väl ritas upp—ett steg som idag tar ett par minuter—kan datorn automatiskt beräkna flödesmåtten och generera en personlig uppskattning av blödningsrisken. I princip kan detta hjälpa läkare att anpassa blodtrycksmål, avgöra hur aggressivt blodförtunnande läkemedel ska användas och planera tidigare CT-skanningar för patienter som flaggas som hög risk. Författarna varnar för att deras studie är retrospektiv och från ett enskilt center, så större, multicenterstudier behövs innan verktyget kan styra rutinvård. Ändå erbjuder det ett tydligt konceptbevis: genom att omvandla strokeangiogram till rika numeriska data och låta maskininlärning sålla bland dem kan vi gå bortom frågan ”Är artären öppen?” till ”Är hjärnans mikrocirkulation säker?”—en förskjutning som i slutändan kan rädda fler patienter från farlig blödning efter behandling.
Citering: Li, H., Pang, C., Guo, X. et al. Machine learning-enabled prediction of hemorrhagic transformation post-thrombectomy using quantitative DSA. Sci Rep 16, 6008 (2026). https://doi.org/10.1038/s41598-026-37036-6
Nyckelord: stroke, mekanisk trombektomi, hjärnblödning, maskininlärning, angiografi