Clear Sky Science · sv
En konstruerad M13-fag–rGO elektro-kemisk biosensor för snabb detektion av virusprotein i komplexa matriser
Varför snabba virustester fortfarande spelar roll
COVID-19-pandemin visade hur avgörande det är att snabbt kunna upptäcka virus, inte bara hos patienter utan också i miljöer som avloppsvatten och livsmedelsbearbetningslinjer. Dagens labbtester är kraftfulla men kan vara långsamma, dyra och beroende av bräckliga biologiska komponenter som är svåra att transportera och förvara. Denna studie presenterar en ny typ av liten elektronisk sensor som använder konstruerade virus och ett ark av avancerat kolmaterial för att detektera ett nyckelprotein från SARS-CoV-2 på under en sekund, även i smutsiga verkliga prover som blodserum, mjölk och avloppsvatten.
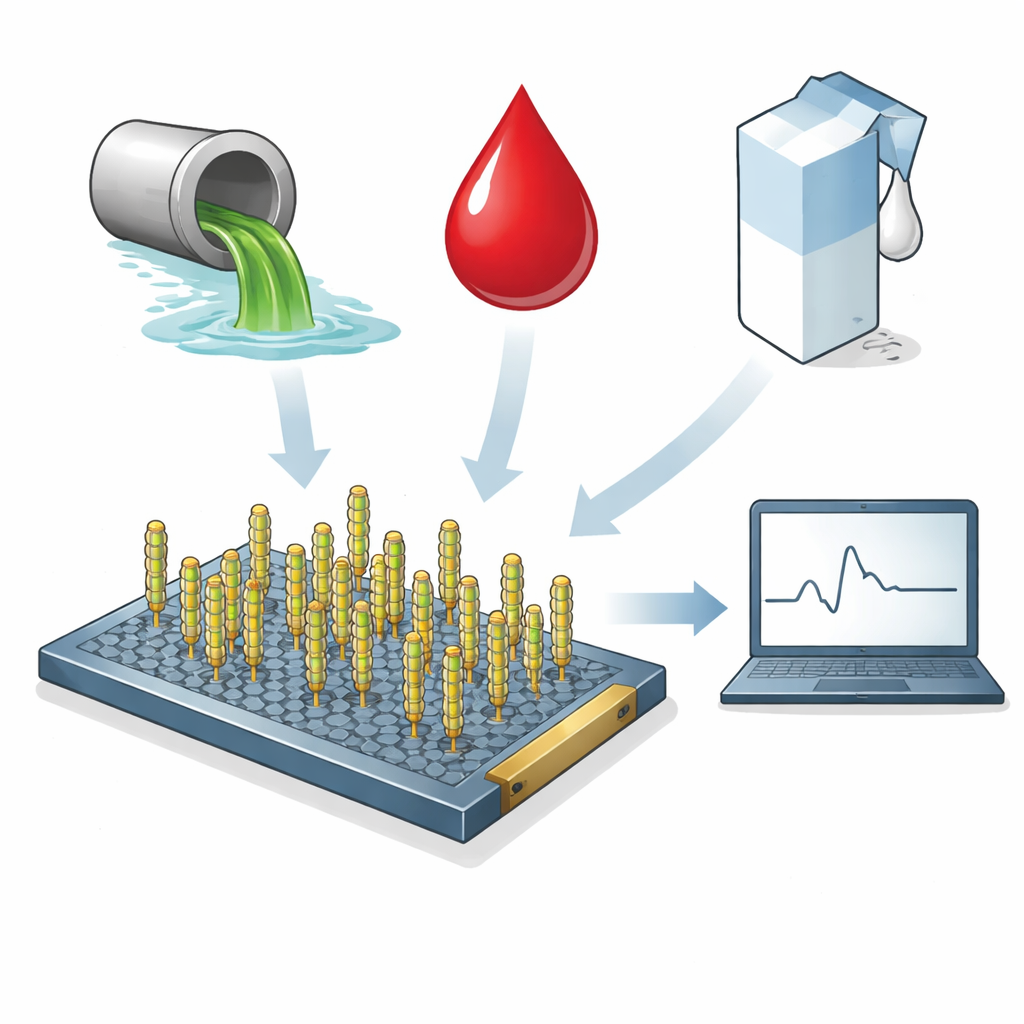
Att förvandla ett ofarligt virus till en smart detektor
I enhetens kärna finns M13, ett ofarligt virus som normalt infekterar bakterier. Dess långa, stavformade kropp är täckt av många identiska kapsidproteiner som forskare kan omprogrammera genetiskt. Forskargruppen infogade en kort, specialkonstruerad peptid på ett av dessa proteiner så att M13-partiklarna skulle känna igen och fästa vid S1-fragmentet av koronavirusets spikeprotein. En andra version av viruset, som bar en slumpad peptid, användes som kontroll för att visa att responsen beror på verklig igenkänning snarare än slumpmässig vidhäftning.
Bygger på ett atomtjockt kolark
För att göra detta programmerbara virus till en sensor fäste forskarna det vid en tunn film av reducerat grafenoxid, en mycket ledande form av kol framställd genom kemisk bearbetning av grafit. Efter att ha spridit grafenoxid på små glaschips och värmt dem för att omvandla dem till reducerat grafenoxid, tillsatte de en länkarmolekyl som både fäster vid kolytan och binder till aminogrupper på viruset. Detta skapade ett tätt lager av M13-partiklar förankrade vid den ledande ytan. Elektronmikroskopi och atomkraftmikroskopi bekräftade att varje tillverkningssteg förändrade ytan på förväntat sätt, och elektriska mätningar visade att tillsats av länken och därefter viruset stadigt ökade resistansen — ett tecken på att ytan framgångsrikt belagts.
Läser virusbindning som en elektrisk puls
Till skillnad från många biosensorer som behöver tillsatta kemikalier eller rörliga delar fungerar denna plattform som ett enkelt motstånd under en mycket liten konstant spänning. När S1-proteinet landar på den virustäcka ytan och binder till den visade peptiden ändrar det något hur laddningar rör sig genom grafenlagret. Detta visar sig som en kortspik i elektrisk ström som uppträder ungefär 300 millisekunder efter att en provdroppe placerats på chippet och sedan avtar när systemet stabiliseras. Genom att ställa in den applicerade spänningen fann teamet en optimal punkt kring minus 0,8 millivolt, där signalen från verklig S1-bindning var stark medan bakgrundsbrus och respons på orelaterade proteiner, såsom bovint serumalbumin, förblev låg.
Fungerar i röriga verkliga prover
Forskarna utmanade sedan sensorn med de typer av komplexa blandningar som ofta slår ut känsliga labbreagenser. De testade enheten i buffert, kommunalt avloppsvatten, fosterbovinserum (en modell för blod) och pastöriserad mjölk, med och utan tillsatt S1-protein. Med en statistiskt definierad gräns för positivt resultat detekterade sensorn extremt låga proteinhalter i enkel buffert — ned till ungefär 10⁻⁴ pikogram per milliliter — vilket är jämförbart med eller bättre än många antikroppsbaserade system. I avloppsvatten flaggade enheten pålitligt högre S1-nivåer, medan den i serum och mjölk konsekvent upptäckte även lägre koncentrationer, allt inom en bråkdel av en sekund. Viktigt är att en kontrollsensor byggd med det slumpade viruset visade liten respons på S1, vilket bekräftar att signalen beror på den konstruerade bindningssekvensen. En parallell sensor som använde en konventionell antikropp på samma grafenplattform uppvisade liknande prestanda, vilket tyder på att virusbaserade system kan matcha antikroppars känslighet samtidigt som de potentiellt är billigare och enklare att producera.

Vad detta kan innebära för vardagstestning
Antikroppar, ryggraden i många diagnostiska metoder, är dyra att framställa, känsliga för värme och kräver ofta kallförvaring från fabrik till klinik. M13-virus kan däremot odlas i bakterier som en enkel kultur, tolerera tuffare förhållanden och kan omprogrammeras genom att ändra deras genetiska kod. Genom att förena denna robusthet och flexibilitet med en snabb, lågströms elektronisk avläsning på grafen, skisserar studien en väg mot bärbara, kostnadseffektiva enheter som kan anpassas för att upptäcka många olika sjukdomsmarkörer eller föroreningar genom att helt enkelt byta den visade peptiden. Arbetet är fortfarande i ett proof-of-concept-stadium och har ännu inte testats i mänskliga kliniska prover, men det pekar mot en framtid där handhållna sensorer skulle kunna skanna efter virusproteiner och andra biomarkörer i kliniker, avlopp eller till och med livsmedelsprodukter inom sekunder, utan den logistiska bördan från traditionella antikroppsbaserade tester.
Citering: Alshehhi, H.Y., Tizani, L., Palanisamy, S. et al. An engineered M13 phage–rGO electrochemical biosensor for rapid detection of viral protein in complex matrices. Sci Rep 16, 9279 (2026). https://doi.org/10.1038/s41598-026-37008-w
Nyckelord: biosensor, grafen, bakteriofag, SARS-CoV-2, elektrokemisk detektion