Clear Sky Science · sv
Ampliconsekvensering med Oxford Nanopore-teknik som ett diagnostiskt alternativ för små idisslar-lentivirus hos får
Dolda infektioner i vardagliga får
Får världen över bär tyst på virus som kan försvaga deras hälsa, förkorta deras liv och kosta lantbrukare pengar — ofta utan tydliga symtom under åratal. Denna studie undersöker ett nytt sätt att upptäcka dessa dolda infektioner med hjälp av en bärbar DNA-sekvenseringsteknik, och erbjuder ett potentiellt genombrott i hur vi skyddar djurens välfärd, gårdens inkomster och till och med livsmedelssäkerhet.
En långsam, kostsam sjukdom som är svår att upptäcka
Arbetet fokuserar på små idisslar-lentivirus (SRLV), en grupp virus som infekterar får och getter. Hos får orsakar de Maedi-Visna-sjukdomen, en långvarig infektion som kan leda till andningsproblem, artrit, hjärnsjukdom och kronisk juverinflammation. Många infekterade djur visar aldrig tydliga tecken, men viruset minskar ändå mjölkproduktionen, ökar lammens dödlighet och leder till för tidig avlivning. I vissa europeiska mjölkbesättningar, bland annat i Spanien och Grekland, kan ungefär hälften av djuren vara infekterade, vilket gör detta till en av de mest betydelsefulla fårsjukdomarna i intensivt drivna besättningar.
Varför dagens tester missar många infekterade djur
Idag förlitar sig gårdar främst på blodprov som letar efter antikroppar (ELISA) eller på standard-DNA-tester (qPCR) för att avgöra vilka djur som är infekterade och bör tas ur besättningen. Men SRLV muterar och rekombinerar snabbt och skapar många snarlika virusvarianter. Vissa varianter känns dåligt igen av antikroppstester, och vissa infekterade får utvecklar aldrig starka antikroppssvar alls. qPCR, som riktar in sig på korta och mycket specifika DNA-sekvenser, kan också misslyckas om de målsökta regionerna förändras. Som följd testar många verkligt infekterade djur negativt och blir kvar i besättningen, där de tyst sprider viruset.
Använda realtidsläsning av DNA för att hitta viruset
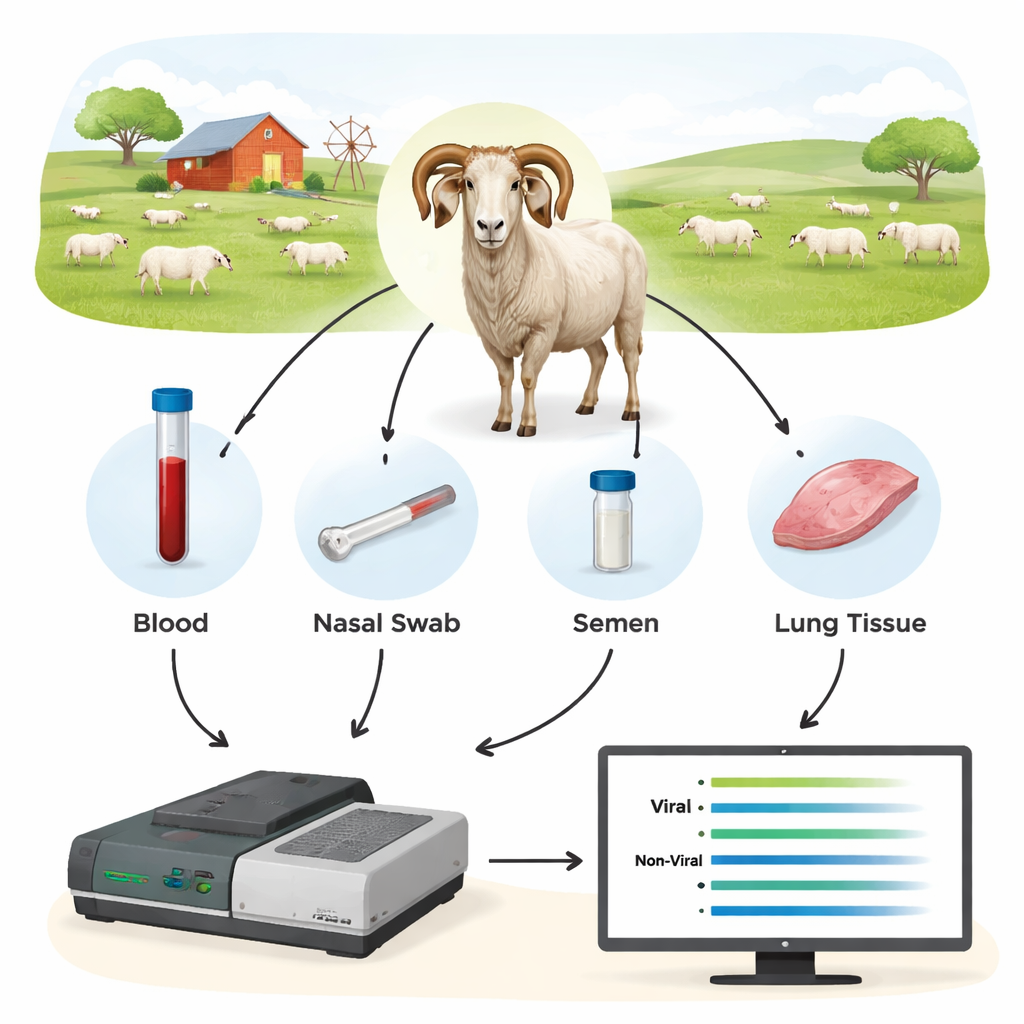
Forskarna testade en tredjegenerationens DNA-metod kallad Oxford Nanopore-sekvensering som ett nytt slags diagnostiskt verktyg. Istället för att söka efter en enda, liten bit av virus-DNA amplifierade de först längre sträckor av viktiga virusgener från djurens prover och sekvenserade sedan dessa bitar i realtid på en Nanopore-enhet. De samlade blod, nässvabbar, sperma samt celler från blod och lungor från 44 baggar och ytterligare får, många av vilka redan testats med konventionella metoder. Genom att fokusera på virusregioner som är relativt bevarade men ändå tillräckligt långa för att avslöja exakt stam, kunde teamet både upptäcka infektion och identifiera vilka virustyper som förekom.
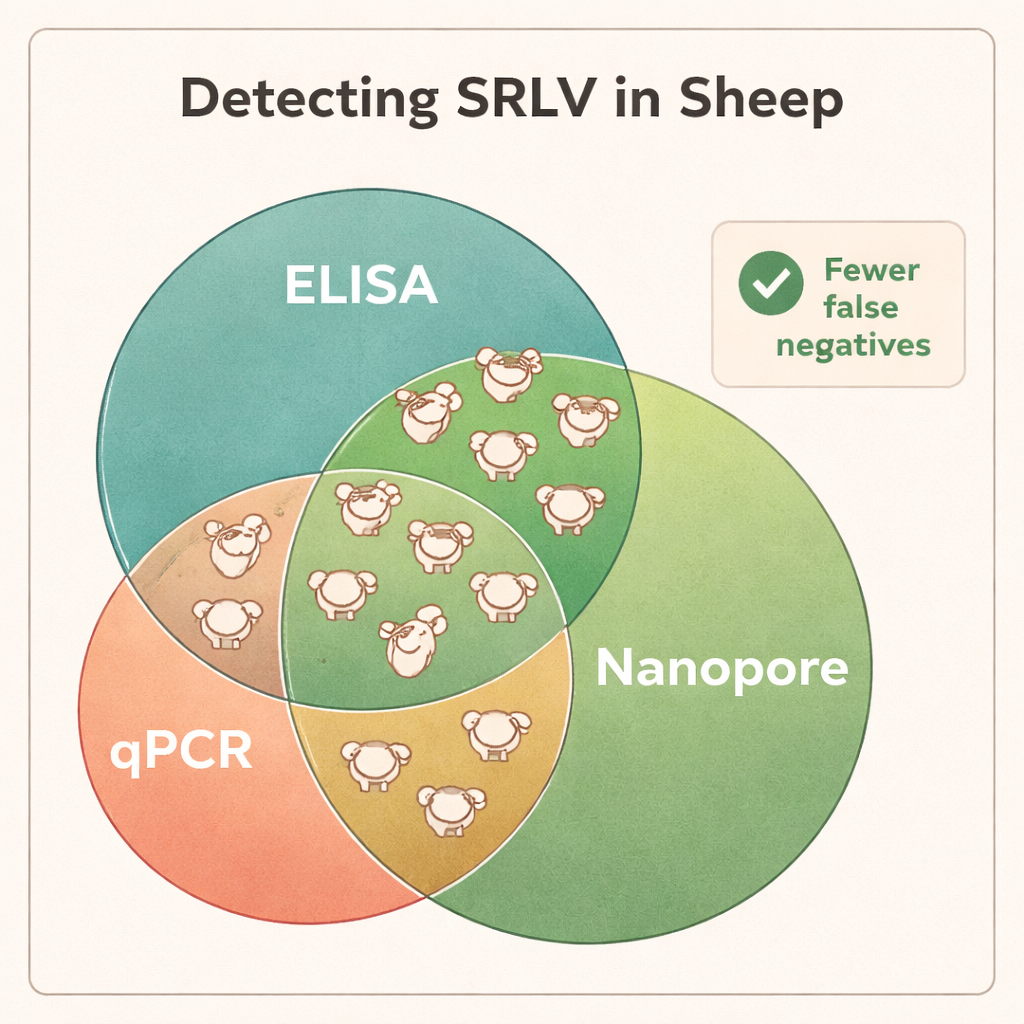
Blod fungerar bäst — och hittar det andra tester missar
Sekvensering visade att DNA från helblod var det mest tillförlitliga materialet för att upptäcka SRLV, även om viruset huvudsakligen lever i en liten delmängd av vita blodkroppar. Lungvävnad från kraftigt infekterade djur gav mycket höga mängder virus-DNA, men sådana prover finns endast tillgängliga efter slakt. I motsats erbjöd nässvabbar, sperma och renade vita blodkroppar för lite virusmaterial för konsekvent diagnostik. När forskarna jämförde Nanopore-resultaten med standardtester som ELISA och qPCR var skillnaderna påtagliga: Nanopore-sekvensering bekräftade infektion hos alla ELISA-positiva baggar men avslöjade också att många ELISA-negativa djur faktiskt var infekterade. I olika besättningar visade sig ungefär 40–45 % av djur märkta som “negativa” med ELISA bära viruset, och qPCR missade en ännu större andel. Sekvensdata avslöjade också saminfektioner med olika SRLV-typer i vissa baggar — information som traditionella tester har svårt att ge.
Från enkla ja/nej-svar till djupare insikter
Eftersom Nanopore läser de faktiska virussekvenserna kan metoden ge mer än en enkel ja- eller nej-diagnos. Teamet använde data för att jämföra virusstammar, bygga släktskaps-träd för de virus som cirkulerade i deras besättningar och studera subtila skillnader i virusproteiner som kan förklara varför vissa djur undgår upptäckt av standard ELISA-kit. De visade att vissa versioner av ett nyckelvirusprotein, som kommersiella antikroppstester riktar sig mot, skiljer sig markant mellan antikroppspositiva och antikroppsnegativa djur. Med tiden skulle sådan information kunna bidra till att förfina både serologiska tester och avelsprogram som syftar till att välja djur som är naturligt mer motståndskraftiga mot infektion.
Vad detta betyder för lantbrukare och djurhälsa
För icke-specialister är huvudbudskapet enkelt: genom att läsa längre delar av virusets DNA direkt kan Nanopore-sekvensering upptäcka fler infekterade får, tidigare och mer exakt än nuvarande rutinmetoder. Den anger också exakt vilka virusstammar som finns i en besättning. Även om detta tillvägagångssätt ännu är mer komplext och kostsamt än ett enstaka blodprov, blir tekniken snabbare, billigare och mer bärbar. Om den integreras i kontrollprogram kan den kraftigt minska antalet “dolda” bärare, förbättra utformningen av vacciner och tester samt stödja avel för mer motståndskraftiga djur — vilket gör fårhållning mer hållbar och human.
Citering: Serrano, M., González, C., Roy, R. et al. Amplicon sequencing with Oxford nanopore technologies as a diagnostic alternative for small ruminant lentiviruses in sheep. Sci Rep 16, 6212 (2026). https://doi.org/10.1038/s41598-026-36989-y
Nyckelord: fårhälsa, lentivirus, nanoporsekvensering, veterinärdiagnostik, Maedi-Visna