Clear Sky Science · sv
En proinflammatorisk neutrofilundergrupp driver tarmens ischemisk–reperfusionsskada via ATF4‑medierad endoplasmatiskt retikel‑stressväg
När blodflöde skadar tarmen
Kirurger och intensivvårdsläkare har länge förbryllats av ett farligt paradox: när blodtillförseln till tarmen avbryts och sedan återställs kan själva återställandet av flödet allvarligt skada tarmens ytskikt. Denna process, kallad intestinal ischemisk–reperfusionsskada, kan leda till livshotande komplikationer såsom sepsis och multipelt organsvikt. Den sammanfattade studien här visar att inte alla immunceller som strömmar till platsen är likadana—en särskilt aggressiv undergrupp av vita blodkroppar spelar en avgörande roll i att förvandla en livräddande reaktion till en skadlig sådan.
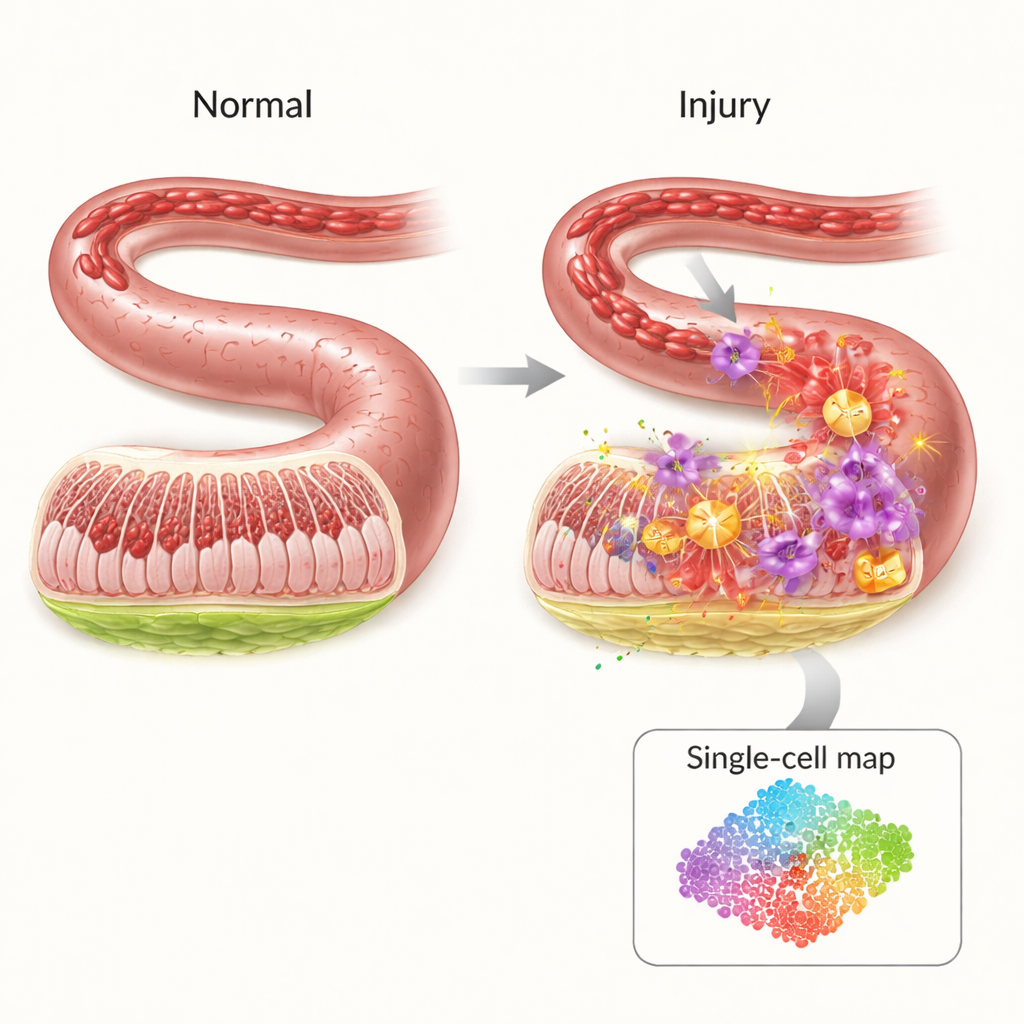
Tarmens sköra skyddsvägg
Insidan av tarmen är täckt av en tunn men högorganiserad barriär som håller bakterier och toxiner kvar i tarmen samtidigt som näringsämnen släpps igenom. När blodflödet avbryts—till exempel vid chock, större operation eller svår trauma—utsätts denna barriär för syrebrist. Överraskande nog uppstår det mesta av skadan inte under syrebristen i sig utan när cirkulationen återvänder. Den plötsliga tillströmningen av syre och immunceller utlöst en storm av inflammatoriska signaler och reaktiva molekyler som kan skapa hål i tarmväggen och låta smittämnen läcka ut i blodomloppet. Trots den kliniska betydelsen finns i dag få riktade behandlingar för att förebygga denna kaskad.
Zooma in på enskilda celler
För att ta reda på vem som gör vad under denna kris använde forskarna single‑cell RNA‑sekvensering, en teknik som läser vilka gener som är aktiva i tusentals enskilda celler samtidigt. I en musmodell för intestinal ischemisk–reperfusion jämförde de skadade tarmar med friska och kartlade 19 större celltyper. De fann att vissa immunceller—särskilt neutrofiler och inflammatoriska monocyter—ökade dramatiskt efter skadan, medan skyddande celler såsom T‑celler, B‑celler och natural killer‑celler minskade. Kommunikationsnätverken mellan celltyper skiftade också, med neutrofiler som framträdande nav som sände och mottog många inflammatoriska signaler, vilket pekar på dem som nyckeldrivkrafter i skadan.
En skadlig undergrupp av första responders
Neutrofiler är kroppens snabbaste första responders och rusar genom blodomloppet för att ta hand om infektioner och rensa upp skräp. Men denna studie visar att inom neutrofilpopulationen finns en särskilt aggressiv subgrupp som står för mycket av den kollaterala skadan i tarmen. När forskarna tog bort neutrofiler hos möss innan de inducerade ischemisk–reperfusion fick djuren mindre tarmförkortning, lägre nivåer av skademarkörer i blodet, bättre vävnadsbild under mikroskopet och tätare tätande proteiner i tarmens epitel. I samodlingsförsök skadade neutrofiler tagna från skadade möss direkt tarmcellerna, minskade deras överlevnad, ökade celldöd och störde viktiga ”blixtlås”-proteiner som håller tarmbarriären intakt.
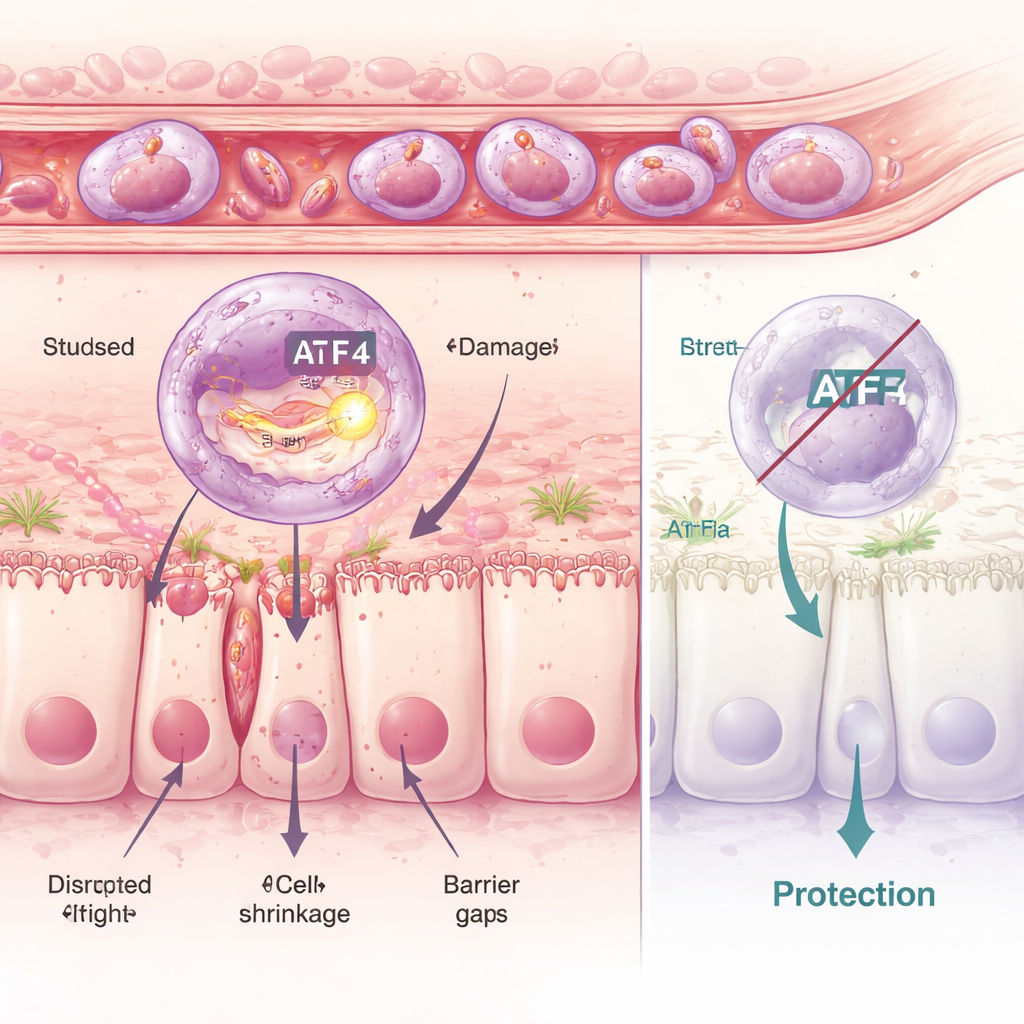
Stress inne i cellerna: när kvalitetskontrollen går fel
Genom att gå djupare undersökte forskarna neutrofiler en och en och identifierade sex distinkta undergrupper. En, kallad C5‑klustret, stack ut med sin starka inflammatoriska profil och för att den aktiverade ett molekylärt stressprogram inne i en struktur som kallas det endoplasmatiska retiklet, cellens proteinvikningsverkstad. En nyckelregulator för detta program är ett protein som heter ATF4. I de skadliga C5‑cellerna var ATF4 och dess målgener högt aktiva. Genom att använda läkemedel som antingen ökar eller dämpar denna interna stressrespons visade teamet att mer stress gav mer tarmsskada, medan blockering av den bevarade tarmbarriären. Möss genetiskt konstruerade att sakna ATF4 var till stor del skyddade: även när stressframkallande läkemedel gavs kunde deras neutrofiler inte längre fullfölja sitt skadliga program, och tarmepitelet förblev betydligt mer intakt.
Vad detta innebär för framtida behandlingar
Tillsammans målar dessa fynd upp en tydlig bild för icke-specialister: bland svärmen av immunceller som översvämmar tarmen när blodflödet återvänder agerar en specifik, stressförberedd undergrupp av neutrofiler som en överentusiastisk saneringsstyrka som river ner byggnaden tillsammans med skräpet. Deras destruktiva kraft beror på en inbyggd stressväg kontrollerad av ATF4 inne i cellerna. Att dämpa denna väg—utan att utplåna alla neutrofiler—kan erbjuda ett sätt att skydda tarmen vid högriskhändelser som större operationer, allvarlig infektion eller trauma. Även om mer arbete krävs för att bekräfta dessa resultat hos människor och för att hitta säkra, precisa läkemedel, öppnar studien en lovande väg mot terapier som håller tarmbarriären intakt när patienterna behöver det som mest.
Citering: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
Nyckelord: tarmbarriär, ischemi reperfusion, neutrofiler, endoplasmatiskt retikel‑stress, ATF4