Clear Sky Science · sv
Metadynamik avslöjar luteolinmedierad konformationsstabilisering mot avapritinib‑resistent PDGFRα D842V/G680R GIST
Varför detta är viktigt för cancerbehandling
Målinriktade cancerläkemedel kan fungera anmärkningsvärt bra—tills tumörer utvecklar sätt att undkomma dem. Denna artikel undersöker hur en vanlig växtförening, luteolin, kan hjälpa till att återställa effekten hos ett viktigt läkemedel som används mot vissa gastrointestinala stromacellstumörer (GIST), en typ av cancer i matsmältningskanalen. Genom avancerade datorsimuleringar visar forskarna hur luteolin skulle kunna stabilisera ett missformat protein i cancerceller så att det befintliga läkemedlet åter kan binda, vilket antyder ett nytt sätt att bekämpa läkemedelsresistens utan att uppfinna behandlingen på nytt. 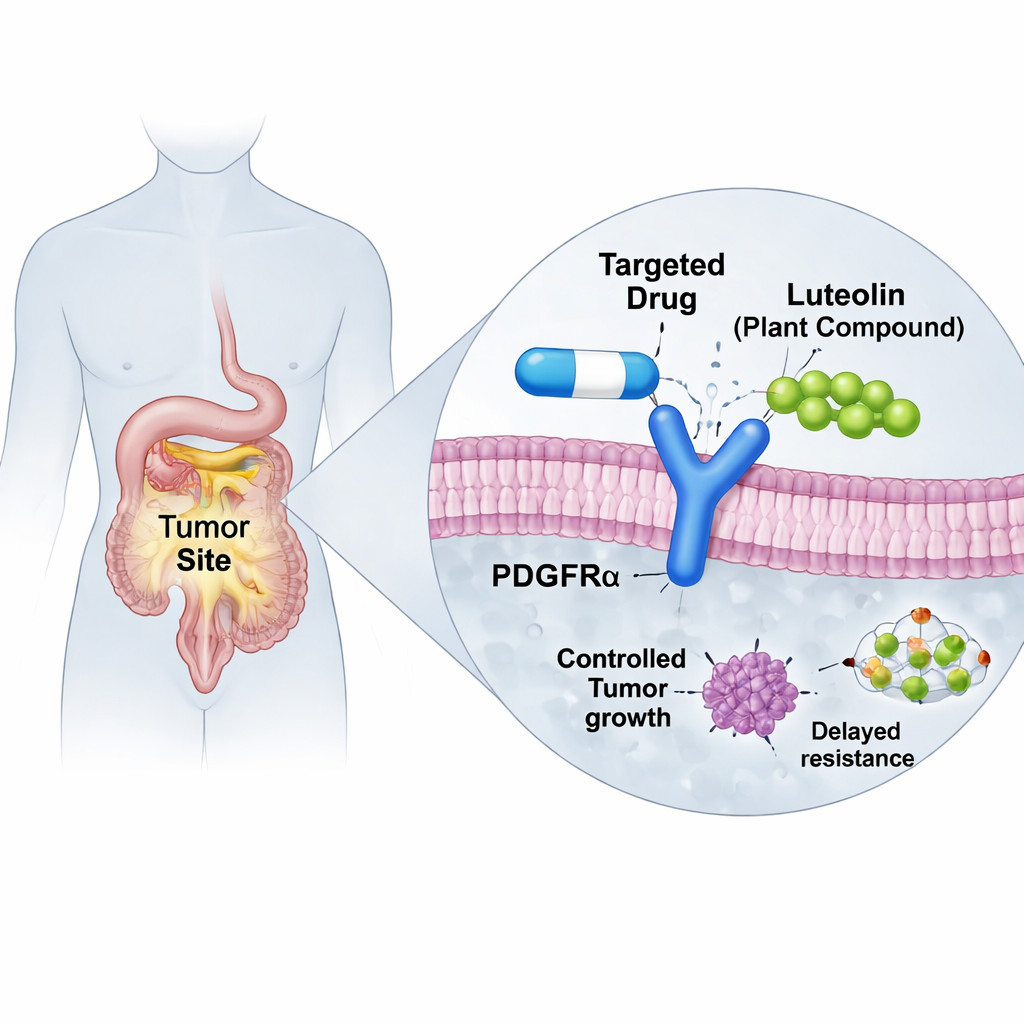
Problemet med tumörer som lär sig undvika läkemedel
GISTs växer ofta på grund av felaktiga ”på‑strömbrytare” i cellsurfaceproteiner kända som KIT eller PDGFRα, som driver konstant tillväxtsignalering. Moderna tabletter kallade tyrosinkinasinhibitorer är utformade för att stänga av dessa strömbrytare och har förbättrat prognosen för många patienter. Men en vanlig mutation i PDGFRα, kallad D842V, gör det äldre läkemedlet imatinib i stort sett verkningslöst. Ett nyare läkemedel, avapritinib, utvecklades specifikt för att bemästra denna envisa mutant och har visat slående framgång i kliniska studier. Tyvärr kan tumörer ändå anpassa sig. Vissa patienter utvecklar ytterligare förändringar i PDGFRα, såsom en sekundär G680R‑mutation, som fysiskt hindrar avapritinib från att sitta bekvämt i sitt bindningsfack, så att läkemedlet lossnar och resistens uppstår.
En växtmolekyl med fascinerande form
Naturprodukterna är en rik källa till läkemedelsidéer, och flavonoider—färgade föreningar som finns i många frukter, grönsaker och medicinalväxter—är kända för att interagera med tillväxtreglerande proteiner inne i celler. Luteolin, en sådan flavonoid som förekommer i en medelhavsväxt kallad Retama monosperma, har redan studerats för sina anticancerösa och antiinflammatoriska egenskaper och verkar säker vid nivåer som kan uppnås genom orala tillskott. Baserat på tidigare screeningarbete misstänkte författarna att luteolin kanske fäster vid PDGFRα på en plats nära, men inte överlappande med, det vanliga läkemedelsbindningsstället. Om detta stämmer kan luteolin fungera som ett subtilt stag och knuffa proteinet till en form som åter välkomnar avapritinib.
Att simulera ett molekylärt partnerskap
För att testa idén in silico byggde teamet detaljerade tredimensionella datormodeller av det resistente PDGFRα‑proteinet som bar både D842V‑ och G680R‑mutationerna. De simulerade hur avapritinib uppträdde på egen hand och hur det uppträdde när luteolin fanns närvarande i närheten, och följde atomära rörelser över hundratals nanosekunder—miliarder av en sekund i verklig tid. När endast avapritinib var bundet drev läkemedlet gradvis ut ur sitt fack eftersom den skrymmande G680R‑förändringen tryckte bort det, tills det helt lossnade från proteinet. I kontrast, när luteolin också var bundet vid ett separat ”allostert” ställe intill en nyckelhelix, stannade avapritinib till stor del kvar på plats. Proteinet som helhet flexade mindre, viktiga strukturella segment höll formen, och betydande kontakter mellan läkemedlet och proteinet bestod mycket längre. 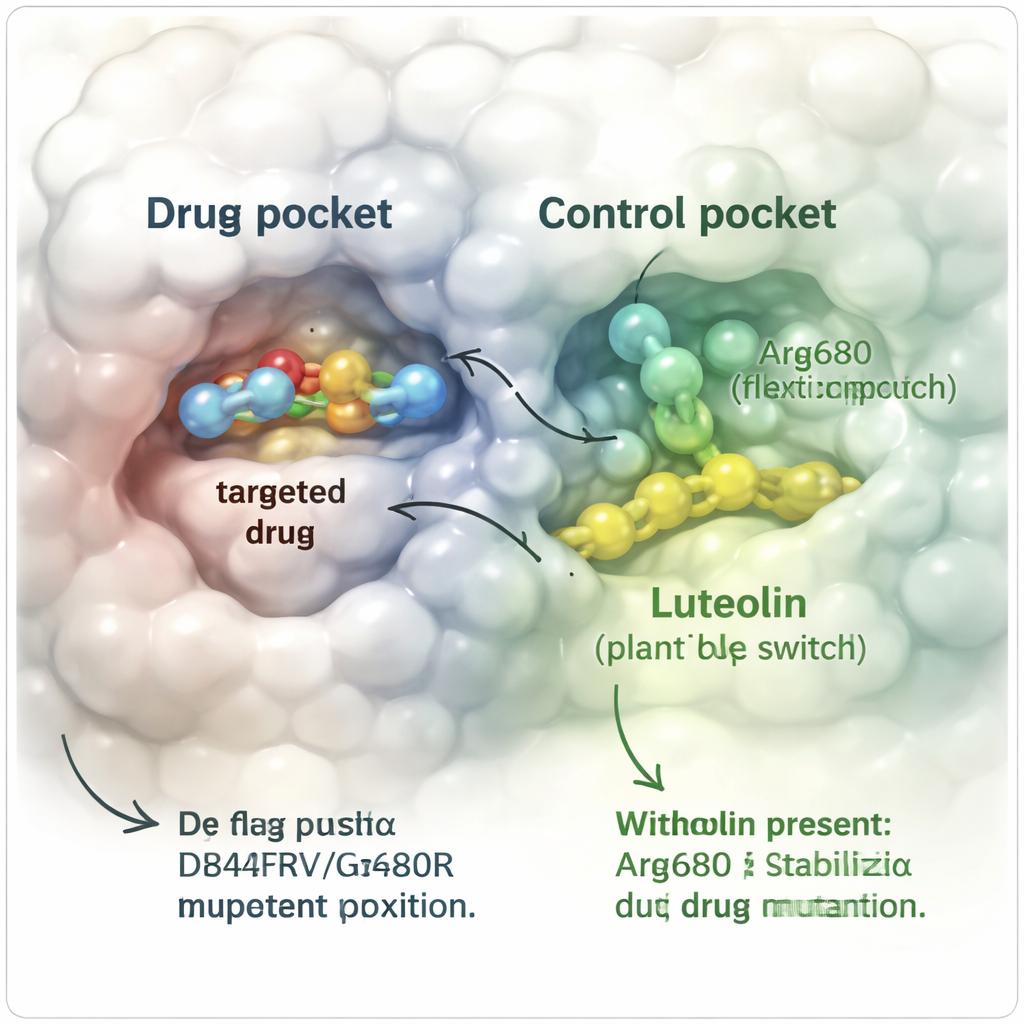
Att fixera en vildsint molekylär strömbrytare
Standardsimuleringar missar fortfarande sällsynta men viktiga formförändringar, så forskarna använde en förstärkt metod kallad metadynamik för att mer fullständigt utforska hur proteinet kan vridas och böjas. De fokuserade på beteendet hos den förändrade aminosyran Arg680, som fungerar som en liten flexibel arm nära läkemedelsfacket. Utan luteolin provade denna arm många positioner och läkemedlet gled lätt bort, med relativt låga energibarriärer för att undkomma. Med luteolin på plats hölls Arg680 i en specifik orientering som inte längre stred mot läkemedlet. Energifyllan förändrades: systemet föredrog nu konformationer där avapritinib förblev bundet, och den energetiska ”kullen” läkemedlet skulle behöva klättra för att undkomma blev flera kilokalorier högre, vilket gjorde dissociation mycket mindre sannolik.
Vad detta kan betyda för patienter
Kort sagt antyder studien att luteolin kan fungera som en molekylär stödbandage som stabiliserar ett förvridet cancerprotein så att ett befintligt målinriktat läkemedel kan greppa det igen. Istället för att designa ett helt nytt läkemedel för varje resistensmutation kan man para det nuvarande läkemedlet med en noga utvald hjälpförening för att återställa dess effektivitet. Arbetet bygger på kraftfulla men rent datorbaserade metoder, så laboratorie‑ och djurstudier behövs fortfarande för att bekräfta om luteolin, eller en relaterad molekyl optimerad för bättre läkemedelsegenskaper, verkligen förstärker avapritinib i levande system. Ändå kan idén att använda små allosteriska hjälpämnen för att återstabilisera resistenta cancermål öppna en ny väg för att förlänga livet för dagens precisionsbehandlingar.
Citering: El Khattabi, K., Akachar, J., Lemriss, S. et al. Metadynamics reveals luteolin-mediated conformational stabilization against avapritinib-resistant PDGFRα D842V/G680R GIST. Sci Rep 16, 6534 (2026). https://doi.org/10.1038/s41598-026-36898-0
Nyckelord: läkemedelsresistens, gastrointestinal stromacellstumör, tyrosinkinasinhibitorer, luteolin, allosterisk modulering