Clear Sky Science · sv
Experimentell och teoretisk utvärdering av geometriberoende inbindning av doksorubicin till ceriumoxid-nanopartiklar via modellering av van der Waals-interaktioner
Varför formen på små läkemedelsbärare spelar roll
Cancerläkemedel som doksorubicin är kraftfulla men kan skada frisk vävnad. En strategi för att göra dem säkrare är att fästa dem på nanopartiklar som transporterar medicinen direkt till tumörer. Denna studie ställer en förbluffande enkel fråga med stora konsekvenser: påverkar nanopartikelns form—om den ser ut som en boll, en stav eller ett skikt—hur mycket läkemedel den kan bära och hur väl den fungerar?
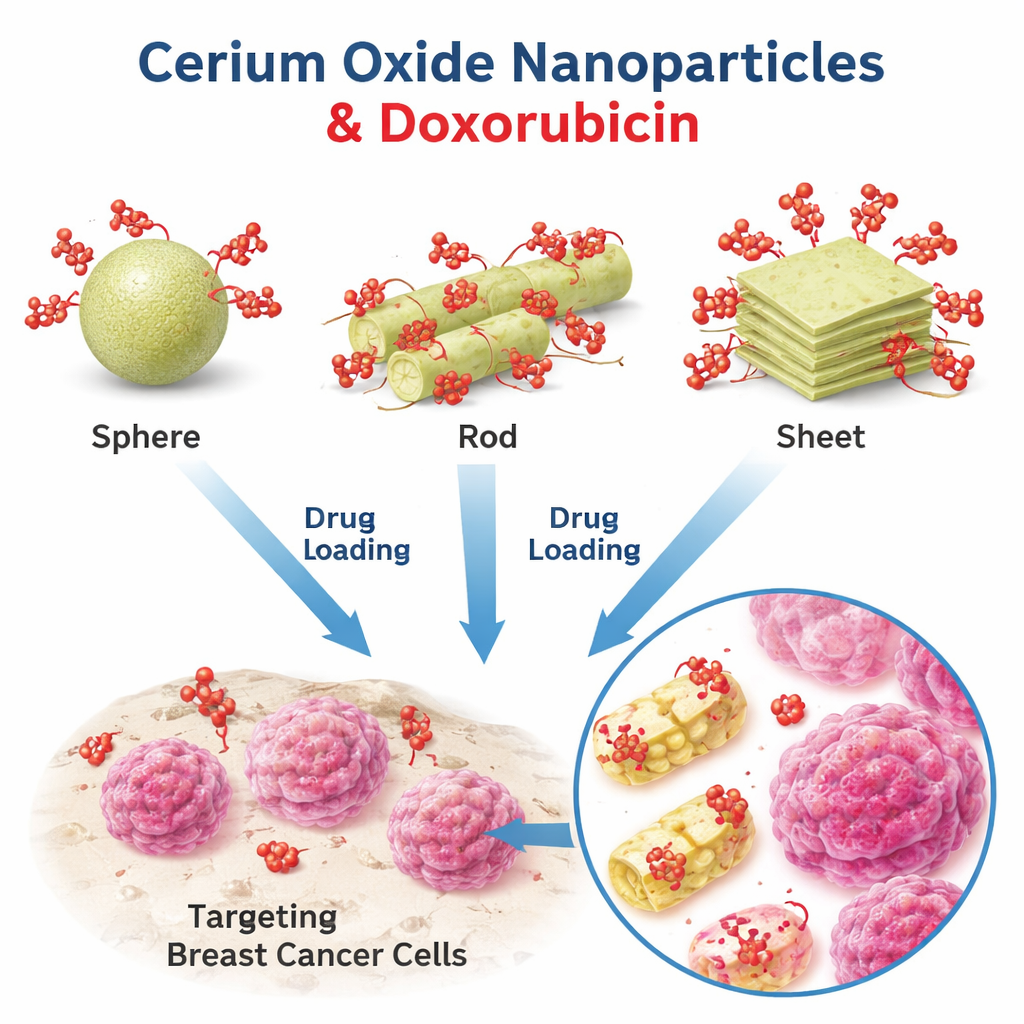
Tre små former, ett cancerläkemedel
Forskarna fokuserade på nanopartiklar av ceriumoxid, ett material som redan är känt för sina antioxidativa, antibakteriella och sårläkande egenskaper, och undersökte dess potential som bärare för doksorubicin, ett ofta använt cytostatikum. De framställde tre distinkta former av ceriumoxid: nästan perfekta sfärer, stavliknande cylindrar och tunna flakelika skivor. Med hjälp av elektronmikroskopi och ljusspridningsmätningar bekräftade de partiklarnas storlek och form, där sfärerna bildade kompakta pärlor, cylindrarna syntes som smala stavar och skivorna som breda, platta lager. Detta kontrollerade uppsättning former gjorde det möjligt att undersöka hur enbart geometrin förändrar läkemedelsbeteendet, samtidigt som materialet i sig var oförändrat.
Mätning av hur mycket läkemedel varje form kan hålla
För att avgöra hur effektivt varje form kunde bära doksorubicin blandade teamet nanopartiklarna med en läkemedelslösning och mätte därefter hur mycket läkemedel som blev kvar i vätskan. Mindre kvarvarande läkemedel betydde att mer hade laddats på partiklarna. Med hjälp av precisa ljusbaserade metoder (UV–vis och fluorescensspektroskopi) fann de att sfäriska nanopartiklar fångade mest doksorubicin, med cirka 86 % av läkemedlet bundet till eller inuti sfärerna. Cylindrar följde med cirka 79 % och skivor hamnade på ungefär 67 %. När dessa läkemedelsladdade partiklar testades mot en aggressiv bröstcancercellinje var den sfärbaserade formuleringen återigen mest effektiv för att döda cancerceller, följd av cylindrarna och därefter skivorna. Intressant nog frigjorde sfärerna också läkemedlet långsammast över tid, vilket antyder att hög laddning kombinerat med långsam frisättning kan stärka läkemedlets effekt inne i cellerna.
Sätta matematiken i arbete i nanovärlden
Parallellt med laboratoriearbetet byggde forskarna en analytisk modell—en förenklad matematisk mikroskopisk bild—för att beräkna hur starkt ett enskilt, ungefär sfäriskt doksorubicinmolekyl bör fästa vid varje nanopartikelgeometri. De koncentrerade sig på van der Waals-krafter, de svaga men allomfattande attraktiva krafterna som får molekyler att hålla ihop. Genom att behandla läkemedlet som en liten sfär nära en sfärisk, cylindrisk eller skivlik ceriumoxidyta härledde de exakta formler för interaktionsenergin när läkemedlet närmade sig eller rörde sig bort. Dessa beräkningar gjorde det möjligt att förutsäga vilken form som borde ge mest stabil bindning, både när läkemedlet är inbäddat i partikeln och när det sitter på ytan, utan att köra omfattande datorsimuleringar.
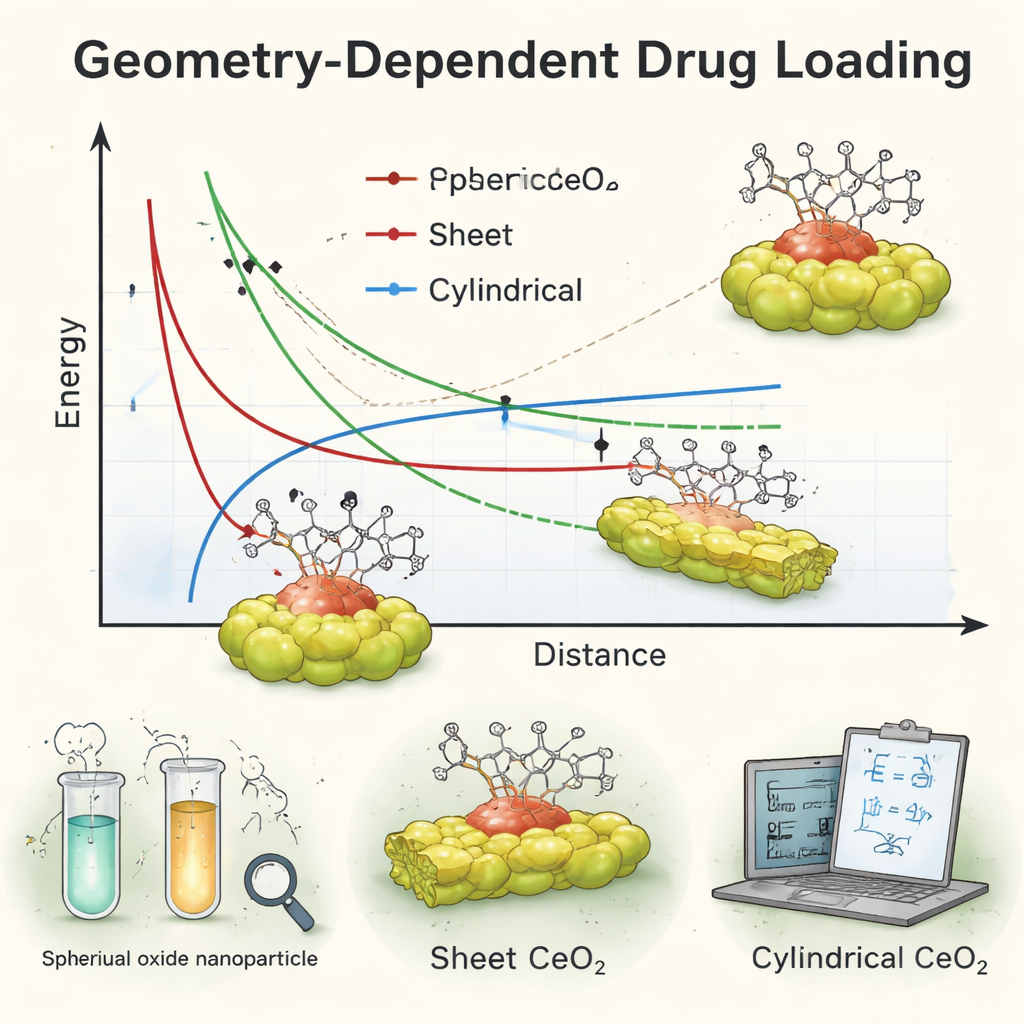
Var teorin stämmer—och var den fallerar
När teamet jämförde sina ekvationer med de experimentella uppgifterna fann de en slående delvis överensstämmelse. Matematiken antydde att sfäriska och skivliknande nanopartiklar borde hålla doksorubicin med mycket liknande bindningsstyrkor, vilket stämde väl överens med den generellt höga inbindning som observerades för dessa två former. Dessutom visade sig sfärerna, när läkemedlet antogs vara fångat inuti partiklarna, vara något mer stabila än de andra formerna, vilket återklang med sfärernas starka prestanda i labbet. Men det fanns en gåta: modellen förutsade relativt svagare bindning för cylindrar, medan experimenten visade att stavformade partiklar ändå laddade läkemedlet ganska effektivt—nästan lika väl som sfärerna. Denna mismatch, särskilt för den cylindriska formen, avslöjade att en enkel modell som behandlar omgivningen som tomt rum och medelvärdesbildar ytdetaljer inte helt kan fånga det verkliga beteendet hos läkemedel–nanopartikel-system badande i vätska och interagerande med celler.
Vad detta betyder för framtida cancerbehandlingar
För icke-specialister är budskapet tvådelat. För det första är nanopartikelns form inte en kosmetisk detalj; den påverkar direkt hur mycket cancerläkemedel den kan bära, hur snabbt den frigör läkemedlet och hur starkt den kan angripa tumörceller. Sfäriska ceriumoxidpartiklar i denna studie framstod som särskilt lovande bärare för doksorubicin, genom att kombinera hög inbindning, stark dödning av cancerceller och långsam läckage av läkemedel. För det andra visar studien gränserna för även eleganta matematiska modeller när de förenklar den röriga verkligheten i biologin. För att designa verkligt tillförlitliga nanomediciner kommer framtida arbete att behöva förena detaljerade experiment med mer sofistikerade teorier som inkluderar den vattenrika miljön, komplexa partikelytor och partikelklustring. Tillsammans kan dessa framsteg leda till smartare nanopartikeldesigner som levererar kraftfulla läkemedel på ett säkrare och mer effektivt sätt.
Citering: Sripaturad, P., Keo, S., Wongpan, A. et al. Experimental and theoretical evaluation of geometry-dependent doxorubicin loading onto cerium oxide nanoparticles via van der Waals interaction modeling. Sci Rep 16, 6169 (2026). https://doi.org/10.1038/s41598-026-36893-5
Nyckelord: nanomedicin, ceriumoxid-nanopartiklar, doksorubicinleverans, nanopartikelgeometri, bröstcancerterapi