Clear Sky Science · sv
Syntes och antitumorutvärdering av nya tioimidazol‑derivat med en trimetoxyfenyl‑moj
Nya kemiska verktyg i kampen mot cancer
Cytostatika skadar ofta friska celler liksom tumörer, vilket leder till svåra biverkningar. Denna studie undersöker en ny familj laboratorietillverkade molekyler som syftar till att slå hårdare mot cancerceller än mot normalt vävnad. Genom att smart förena två kemiska byggstenar som redan är kända för att fungera väl i läkemedel skapade forskarna föreningar som uppvisar stark, målinriktad död av cancerceller i provrörs- och 3D‑tumörmodeller, samtidigt som friska celler förblir i stort sett opåverkade.
Att bygga smartare cancer‑dödande molekyler
Gruppen fokuserade på två ”privilegerade” kemiska strukturer som återfinns i många framgångsrika läkemedel. Den ena är imidazol, en liten ring som passar väl in i många biologiska mål. Den andra är en trimetoxyfenyl (TMP)‑grupp, ett mönster av tre syre‑innehållande sidokedjor på en aromatisk ring som är centralt i flera antitumörläkemedel som stör celldelning. Genom att infoga en svavelatom i imidazol‑kärnan (skapande av en tioimidazol) och koppla den till en TMP‑grupp hoppades kemisterna kunna finjustera hur molekylerna rör sig i kroppen och hur tätt de binder till cancerrelaterade proteiner. Med en stegvis syntesväg byggde de ett bibliotek av närbesläktade föreningar, var och en subtilt modifierad för att undersöka vilka egenskaper som är viktigast för antitumoral aktivitet. 
Testning av cancerceller samtidigt som frisk vävnad skonas
De nya molekylerna testades på fyra humana cancercellinjer — osteosarkom (ben), cervix-, kolon‑ och lungcancer — samt på icke‑cancerösa lungfibroblaster. Många av föreningarna saktade ner eller stoppade cancercellstillväxten, men en särskild, benämnd 13b, utmärkte sig. Den dödade ben‑ och cervixcancerceller vid mycket låga koncentrationer, samtidigt som den inte visade mätbar toxicitet mot normala fibroblaster även vid doser som var mer än 60 gånger högre. Flera andra föreningar var måttligt potenta men mindre selektiva, vilket understryker hur små strukturella förändringar — såsom att lägga till en kloratom eller en nitrogrupp i specifika positioner — kan vrida balansen mellan bred toxicitet och cancerfokuserad verkan.
Hur ledande föreningen får cancerceller att självdö
För att förstå vad 13b faktiskt gör inne i cellerna letade forskarna efter kännetecken för programmerad celldöd, det vill säga apoptos. Cancerceller behandlade med 13b blev positiva för Annexin V och aktiverade enzymerna kaspas‑3 och ‑7, klassiska markörer på att en cell pressats in i ett ordnat självmordsprogram snarare än att helt enkelt spricka. Mikroskopi visade intensiva fläckar av γH2AX, en signal för brutna DNA‑strängar, i kärnorna hos behandlade celler. Med tiden började cellernas interna skelett omorganiseras och brytas ner, särskilt i cervixcancerceller som rundade upp sig och lossnade — visuella tecken på att apoptos var väl igång. Tillsammans visar dessa fynd att 13b skadar cancercellernas DNA och sedan driver cellerna ned en kontrollerad dödsväg.
Från platta celllager till 3D‑mini‑tumörer
De flesta laboratorietester odlar cancerceller i tunna lager, vilket inte fullt ut efterliknar den täta, lagerlika strukturen i verkliga tumörer. För att hantera detta odlade teamet cellerna som tredimensionella sfäroider — små, bollformade kluster som bättre liknar en tumörs arkitektur och de utmaningar som läkemedelsgenomträngning innebär. När dessa sfäroider behandlades med 13b krympte de i en dosberoende takt. Bensfäroider var särskilt känsliga och blev små, lösa och fragmenterade vid högre läkemedelsnivåer. Fluorescerande färgning visade vågor av apoptos som rörde sig från sfäroidens utsida inåt när koncentrationen ökade, vilket bevisar att 13b kan penetrera och döda celler genom hela dessa kompakta strukturer. 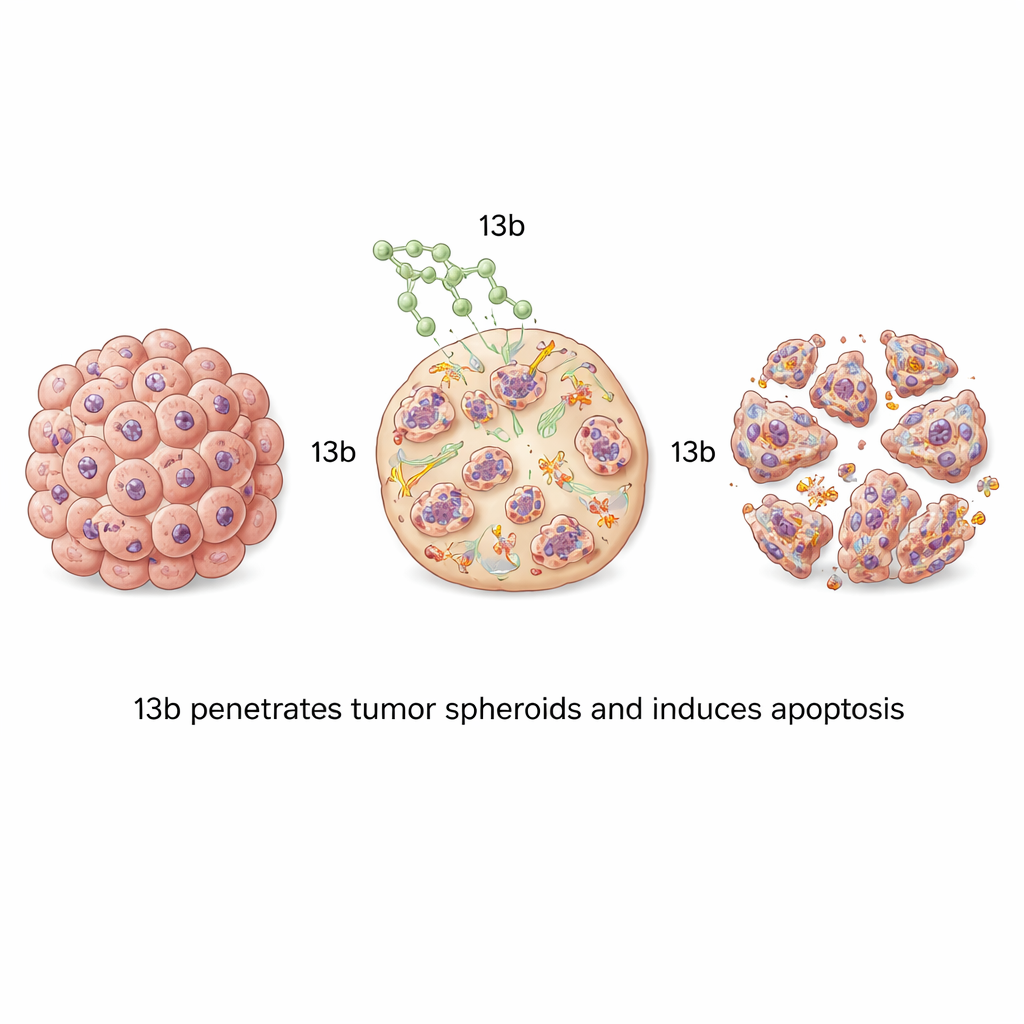
Varför detta arbete är viktigt för framtida cancerbehandlingar
För icke‑specialisten är huvudbudskapet att forskarna har skapat en ny klass små molekyler som kombinerar de bästa egenskaperna från två väletablerade läkemedelskomponenter i en hybriddesign. Deras ledande förening, 13b, kan känna igen och effektivt förstöra cancerceller samtidigt som den i hög grad skonar friska celler i laboratorietester, och den förblir effektiv även i mer realistiska 3D‑tumörmodeller. Även om mycket återstår — såsom att bestämma dess exakta molekylära mål, förbättra lösligheten och testa i djurmodeller — visar denna studie att kombinationen av tioimidazol‑ och TMP‑ramverk är en lovande strategi för att skapa mer selektiva och kraftfulla antikancermedel.
Citering: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
Nyckelord: antikancerläkemedel, imidazol‑derivat, trimetoxyfenyl, apoptos, 3D tumörsfäroid