Clear Sky Science · sv
Utvärdering av cytotoxicitet, sårhelande och antiinflammatoriska effekter av netarsudil på humana hornhinnans epitelceller
Varför en ögondropps "sweet spot" spelar roll
Glaukomögondroppar kan rädda synen genom att sänka trycket inne i ögat, men långvarig användning lämnar ofta patienter med sveda, rodnad och torrhet. Denna studie granskar en modern glaukomläkemedel, netarsudil (säljs som Rhopressa), och ställer en enkel men avgörande fråga: vid vilken punkt börjar ett hjälpsamt läkemedel skada ögats klara yta? Genom att testa olika utspädningar av den kommersiella ögondroppen på humana hornhinnesceller i laboratoriet identifierar forskarna en smal "sweet spot" där läkemedlet verkar främja läkning och dämpa inflammation, och högre doser där det blir giftigt.
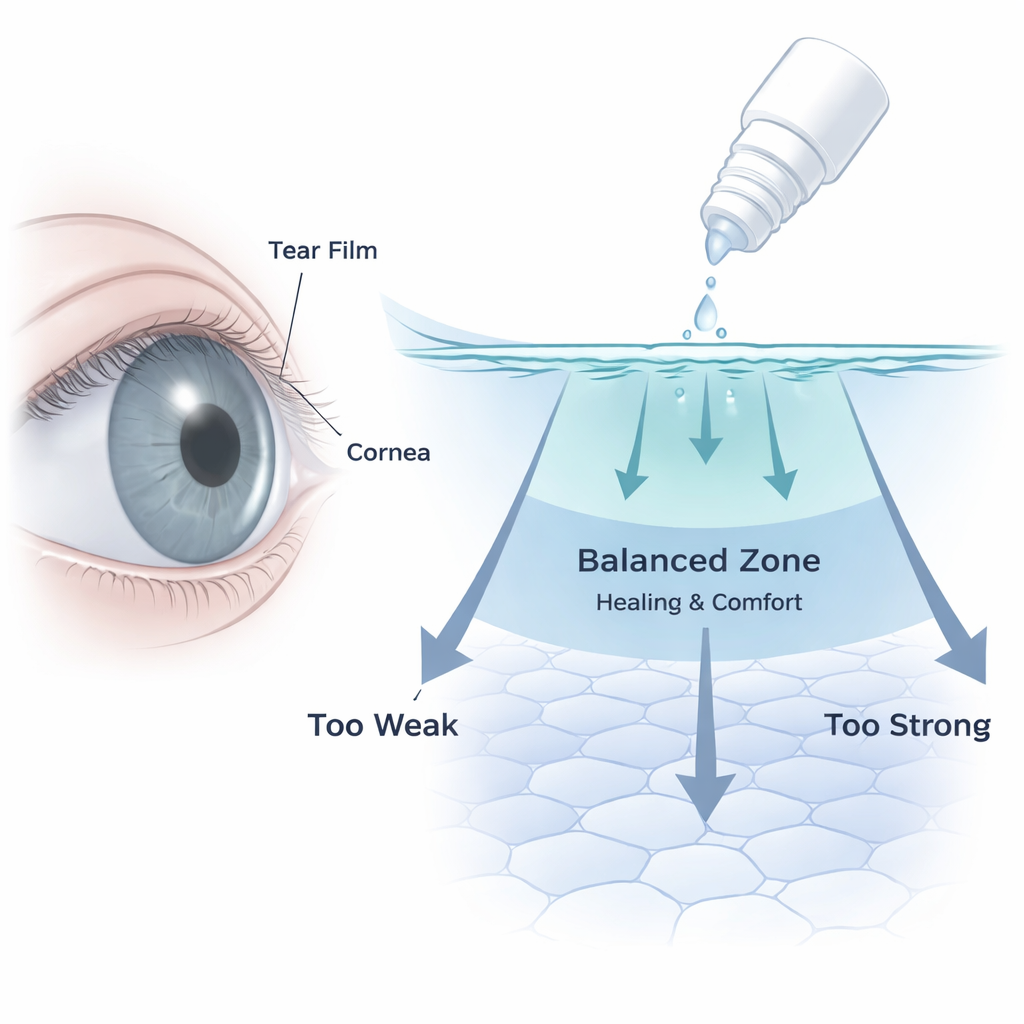
Problemet med hjälpsamma men hårda ögondroppar
Glaukom skadar långsamt synnerven och är en ledande orsak till irreversibel blindhet globalt. Det vanliga sättet att bromsa sjukdomen är att sänka ögontrycket med dagliga ögondroppar. Men dessa läkemedel utsätter ögats framsida under år, och många patienter utvecklar ögonytsjukdom: torra, irriterade ögon med suddig eller fluktuerande syn. Orsakerna är flera—aktiva läkemedelsmolekyler, konserveringsmedel som bensalkoniumklorid och formuleringar som är för sura eller salta jämfört med naturliga tårar. Netarsudil tillhör en nyare klass läkemedel kallad ROCK-hämmare, som verkar genom att relaxera interna dräneringsvävnader snarare än att ändra vätskproduktion. Eftersom samma ROCK-signalväg också styr hur hornhinnesceller behåller form, fäster vid varandra, rör sig och svarar på skada, har det funnits oro—och vissa kliniska fallrapporter—för att netarsudil kan störa hornhinnans yta på sätt vi ännu inte helt förstår.
Test av netarsudil på ögats frontlinjeceller
Teamet använde en etablerad human hornhinnans epitelcellinje—den typ av celler som bildar ögats klara yttersta lager—och exponerade dem för utspädda versioner av den faktiska netarsudilflaskan som patienterna får. De kontrollerade grundläggande fysikaliska egenskaper först: dropplösningen hade ett surt pH på 5,5 (tårar ligger närmare neutralt, omkring 7,0–7,5) och något lägre saltkoncentration än naturliga tårar, men en övergripande salthalt (osmolaritet) som ändå var nära det fysiologiska spannet. De skapade sedan en serie arbetslösningar genom att blanda den kommersiella droppen med odlingsmedium till slutliga styrkor på 0,1%, 0,5%, 1% och 2% i volym, och jämförde dem med en läkemedelsfri kontroll. Över dessa utspädningar och tider från 30 minuter till 24 timmar mätte de om cellerna överlevde, om deras membran läckte, hur deras form och fina struktur förändrades i mikroskopet, och hur snabbt de kunde sluta ett artificiellt "skrapsår".
En smal gräns mellan läkning och skada
Resultaten visade ett tydligt, tvåfasigt mönster. Mycket låga koncentrationer (0,1%) orsakade endast mild stress, medan en medelnivåutspädning (0,5%) framträdde som en subletal "optimal zon." På denna nivå förblev den totala cellöverlevnaden hög, cellagret hölls relativt intakt, och skrapsår i cellskiktet slöt sig snabbare än i obehandlade kontroller, vilket tyder på bättre reparation. I kontrast minskade starkare exponeringar vid 1% och 2% kraftigt cellöverlevnaden och ökade utsläpp av ett enzym (LDH) som signalerar membranskada, särskilt efter 12–24 timmar. Under både standardmikroskop och elektronmikroskop blev celler vid dessa högre utspädningar rundade, förlorade sina fina ytförlängningar, utvecklade stora inre blåsor (vakuoler) och visade klumpat DNA—kännetecken för celler på väg mot celldöd. Med andra ord, när den effektiva koncentrationen steg blev samma läkemedel som kunde stödja läkning vid en nivå tydligt skadligt bortom en kritisk tröskel.
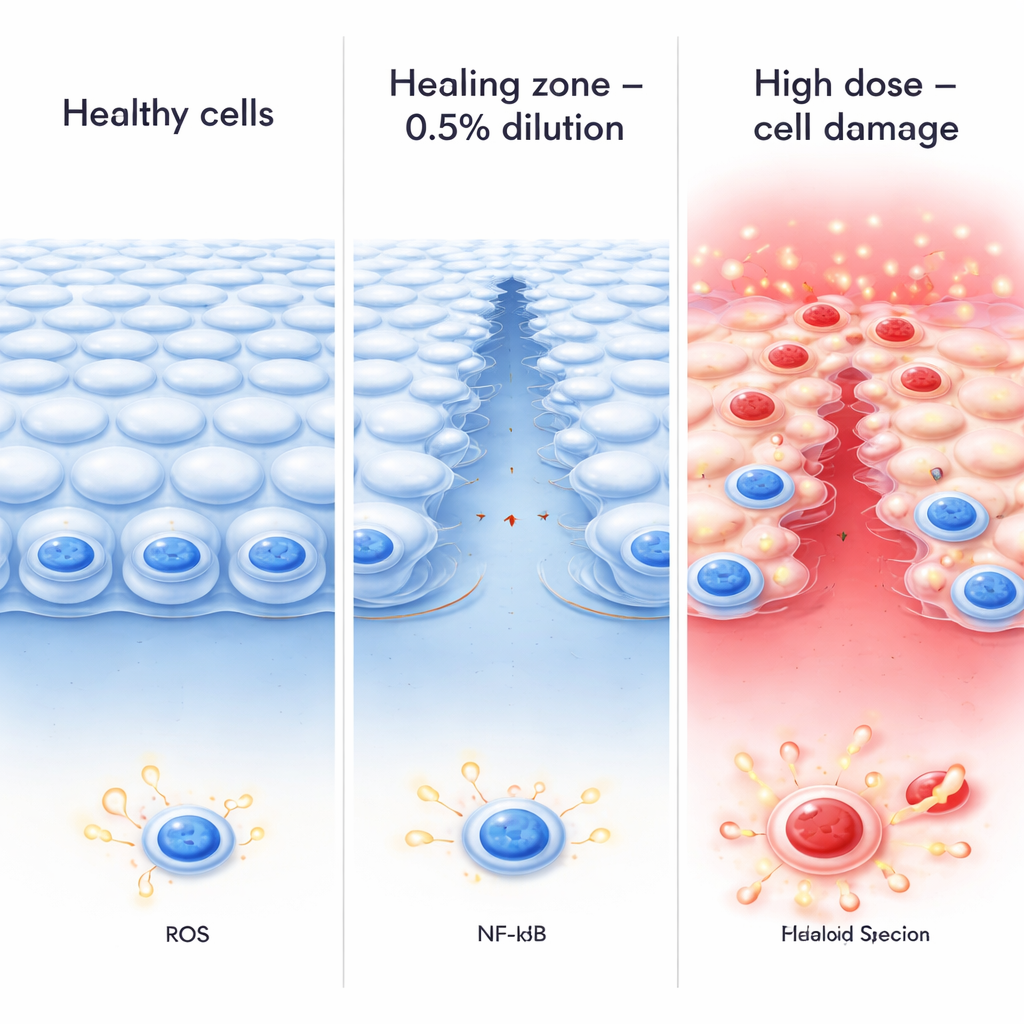
Dämpning av inflammation på en stressad ögonyta
Forskarna undersökte också hur netarsudil beter sig när ögats yta redan är inflammerad. De härmade bakteriell skada genom att tillsätta lipopolysackarid (LPS), en molekyl som utlöser ett immunsvar, och observerade hur hornhinnescellerna klarade sig med eller utan 0,5%-utspädningen. LPS ensam sänkte cellöverlevnaden, ökade produktionen av reaktiva syreradikaler (skadliga syrebaserade kemikalier) och drev en viktig inflammatorisk regulator kallad NF-κB in i cellkärnan, där den aktiverar inflammatoriska gener. När celler medbehandlades med LPS och 0,5% netarsudil överlevde de bättre, producerade mindre reaktiva syrearter och visade reducerad kärntranslokation av NF-κB. Detta tyder på att netarsudil, åtminstone inom detta mellanspann, kan dämpa inflammatorisk signalering snarare än att förstärka den.
Vad detta betyder för personer som använder glaukomdroppar
För en lekmannaläsare är slutsatsen att samma netarsudilögondropp kan driva hornhinnesceller mot läkning eller mot skada, beroende på hur mycket som faktiskt når dem och hur länge. I en kontrollerad odlingsskål påskyndade en 0,5%-utspädning av den kommersiella formuleringen sårslutning och mildrade inflammatoriska svar, medan högre utspädningar av samma produkt dödade celler och störde deras struktur. Riktiga ögon är mer komplexa: blinkning, tåromsättning och naturliga försvar späder ut och rensar droppar snabbt, och produkten innehåller konserveringsmedel och andra ingredienser som också kan spela roll. Ändå ger dessa fynd ögonläkare och läkemedelsutvecklare en mekanistisk ledtråd: det finns ett smalt terapeutiskt fönster där ROCK-hämning kan stödja en friskare hornhinnayta, och att gå förbi det riskerar att tippa balansen mot toxicitet. Framtida arbete som kopplar dessa laboratorietrösklar till verklig dosering och tårfilmsdynamik kan hjälpa till att förfina formuleringar och behandlingsscheman som skyddar både syn och vardagskomfort för personer med glaukom.
Citering: Han, K.E., Ahn, J.H., Kim, SJ. et al. Evaluation of cytotoxicity, wound healing, and anti-inflammatory effects of netarsudil on human corneal epithelial cells. Sci Rep 16, 6164 (2026). https://doi.org/10.1038/s41598-026-36860-0
Nyckelord: glaukomögondroppar, netarsudil, hornhinnans epitel, ögonytsjukdom, ROCK-hämmare