Clear Sky Science · sv
Farmakokinetik, patologi och effekt av SARS-CoV-2:s huvudproteashämmare VPC285785 i en murin modell för coronavirusinfektion
Varför vi fortfarande behöver bättre COVID‑piller
De första antivirala pillren mot COVID‑19, såsom Paxlovid, var ett viktigt genombrott under pandemin. Men de är inte perfekta: de måste tas mycket tidigt, kräver flera tabletter per dag och kan ge farliga interaktioner med andra läkemedel. Denna studie undersöker nya läkandekandidater utformade för att blockera coronaviruset på mer än ett sätt, fungera bra som enkla tabletter att ta peroralt och orsaka färre läkemedels‑interaktioner, med hjälp av en musmodell för coronavirusinfektion.
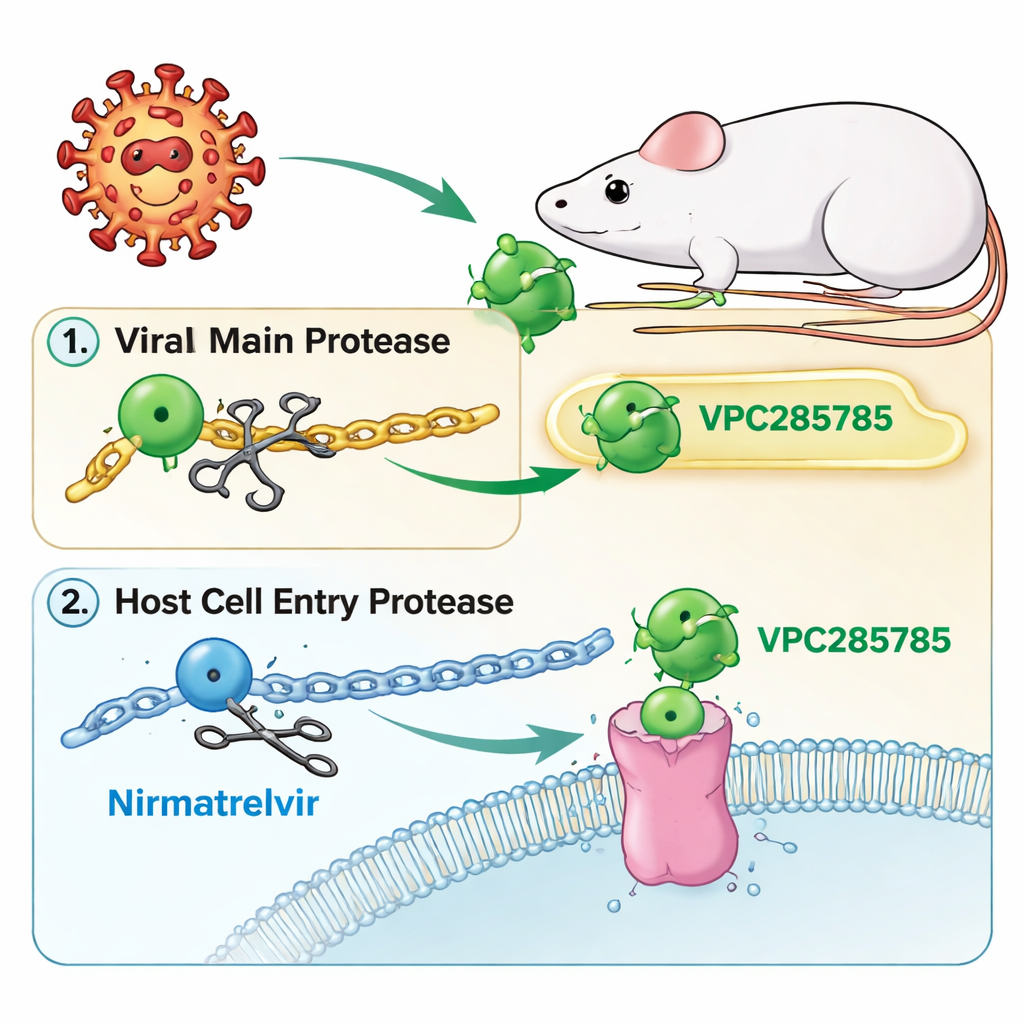
En ny vinkel på COVID‑19:s proteasmål
Likt Paxlovid riktar sig de nya föreningarna — kallade VPC285785 och VPC285786 — mot virusets ”huvudproteas”, en molekylär sax som klipper långa virusproteiner till fungerande delar. Om dessa saxar blockeras kan viruset inte färdigställa sin uppbyggnad och stannar av. Forskarna designade också molekylerna för att slå mot ett andra protein i våra egna celler, cathepsin L, som hjälper vissa coronavirus att ta sig in. Genom att rikta in sig både på det virala proteaset och en värdcellens inträdeshjälpare hoppades teamet skapa ett tvåfaldigt verkande piller som kan vara svårare för viruset att undkomma och som inte skulle behöva en booster‑medicin.
Byggda för uthållighet, inte för booster
Paxlovid kombinerar nirmatrelvir med ett annat läkemedel, ritonavir, vars uppgift inte är att bekämpa viruset utan att bromsa nedbrytningen av nirmatrelvir i levern. Ritonavir stör dock många enzymer som bearbetar vanliga mediciner, vilket leder till komplexa och ibland farliga interaktioner. VPC285785 och VPC285786 har kemiskt justerats för att stå emot nedbrytning på egen hand, med drag som fluoratomer och ringstyvning som gör dem mindre attraktiva för leverns enzymer. I laboratorietester med humana och murina leversystem visade båda nya föreningarna sig vara åtminstone lika stabila som nirmatrelvir, och VPC285786 var i vissa avseenden ännu mer tålig, utan något ritonavir närvarande.
Hur läkemedlen beter sig och förflyttar sig i möss
Teamet undersökte sedan hur föreningarna färdas i musens kropp, genom att mäta hur snabbt de försvinner från blodet och hur väl de tas upp peroralt. Efter injektion dröjde VPC285785 och VPC285786 kvar i blodomloppet ungefär lika länge som nirmatrelvir och nådde en högre total exponering. När de gavs peroralt skilde sig deras banor dock åt: VPC285785 uppnådde måttlig men användbar absorption (ungefär 15 % av den intagna dosen nådde cirkulationen), medan VPC285786 knappt tog sig in i blodet (cirka 3 %). Eftersom tabletter måste passera tarmväggen för att vara praktiska behandlingar gick endast VPC285785 vidare till infektionsförsöken.
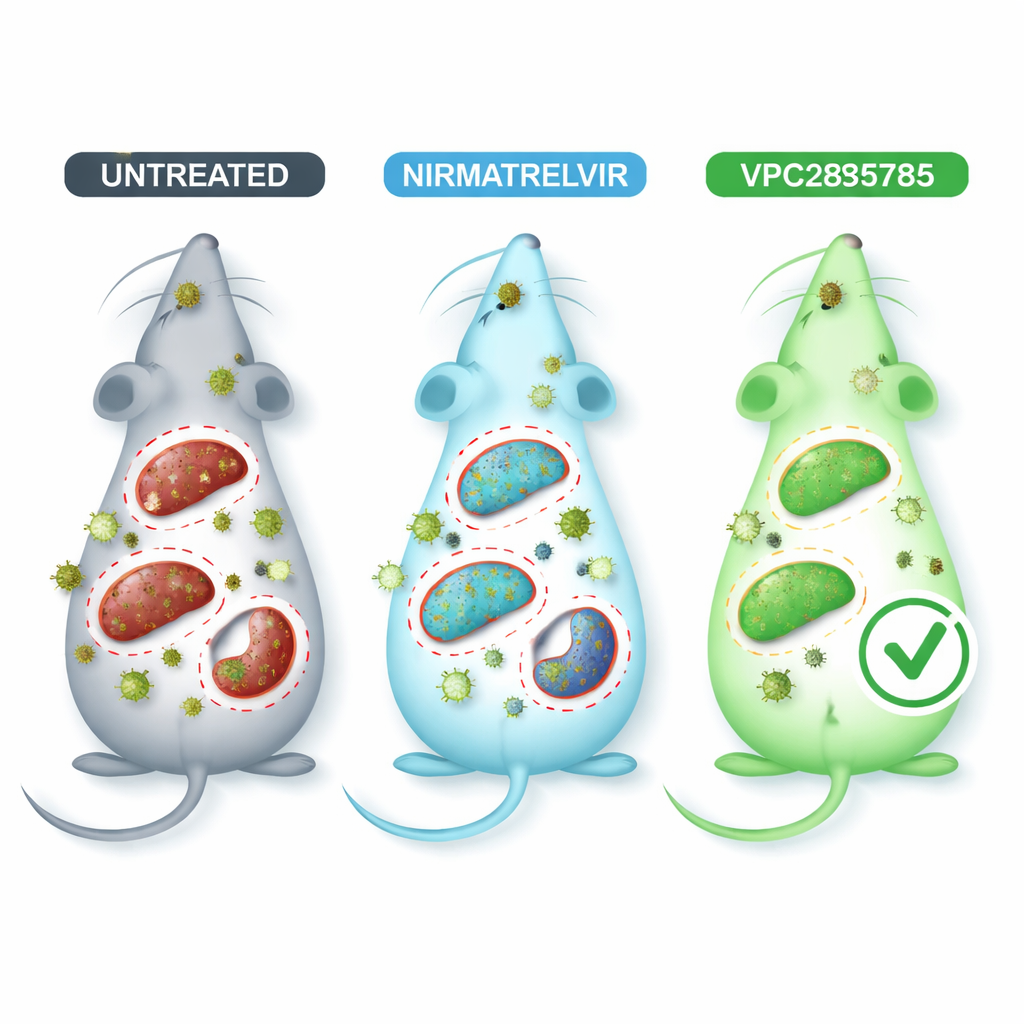
Tester av det nya pillret i infekterade möss
För att efterlikna coronavirus‑sjukdom i en säkrare miljö använde forskarna ett muscoronavirus kallat MHV‑A59, som invaderar flera organ och orsakar lungs‑ och leverskador som på många sätt liknar mänsklig infektion. Infekterade möss behandlades peroralt med VPC285785, med nirmatrelvir som jämförelse, eller med ett inaktivt fordon. Blodprov visade att infektionen påfrestade levern och njurarna, men djur som gavs VPC285785 eller nirmatrelvir tenderade att ha friskare leverenzym‑ och njurmarkörer än obehandlade möss. Mest anmärkningsvärt sänkte VPC285785 kraftigt mängden viralt genetiskt material i levern, hjärnan och mjälten, medan nirmatrelvir gav en tydlig minskning endast i hjärnan. I lungor, hjärta och njurar gav ingen av behandlingarna stor skillnad under de testade förhållandena.
Vad detta kan betyda för framtida COVID‑behandlingar
Även om VPC285785 är mindre potent mot det virala proteaset i ett provrör än nirmatrelvir presterar det väl i levande djur, genom att signifikant minska virusnivåer i flera viktiga organ samtidigt som organfunktionen bevaras — allt utan en ritonavir‑booster. Dess systerförening, VPC285786, visar att ännu starkare dubbelt mål riktat mot både virusproteas och cathepsin L är möjligt, men dess dåliga absorption måste åtgärdas. Sammanfattningsvis tyder resultaten på att nästa generations COVID‑piller kan utformas som enkla, peroralt tillgängliga läkemedel som slår mot både virus‑ och värdmål, ger färre farliga interaktioner med andra mediciner och ändå levererar starkt skydd i livsviktiga vävnader.
Citering: Smith, J.R., Toro, A., Sabater, A. et al. Pharmacokinetics, pathology and efficacy of SARS-CoV-2 main protease inhibitor VPC285785 in a murine model of coronavirus infection. Sci Rep 16, 6905 (2026). https://doi.org/10.1038/s41598-026-36842-2
Nyckelord: SARS-CoV-2 antivirala medel, inhibitorer av huvudproteas, Paxlovid‑alternativ, musmodell för coronavirus, oral COVID‑behandling