Clear Sky Science · sv
YTHDC1 modulerar det maligna fenotypen hos retinoblastom via SQSTM1-medierad autophagi
Varför detta spelar roll för barnens ögoncancer
Retinoblastom är den vanligaste ögoncancern hos små barn. Läkare kan ofta bota den om den upptäcks tidigt, men när tumören börjar invadera vävnader runt ögat eller sprida sig mot hjärnan blir det mycket svårare att rädda både barnets liv och syn. Denna studie undersöker en molekylär "broms" inne i tumörcellerna — två molekyler kallade YTHDC1 och SQSTM1 — som verkar bidra till att hålla retinoblastom mindre aggressiv. Att förstå hur denna broms fungerar kan öppna nya vägar för mildare, mer riktade behandlingar.
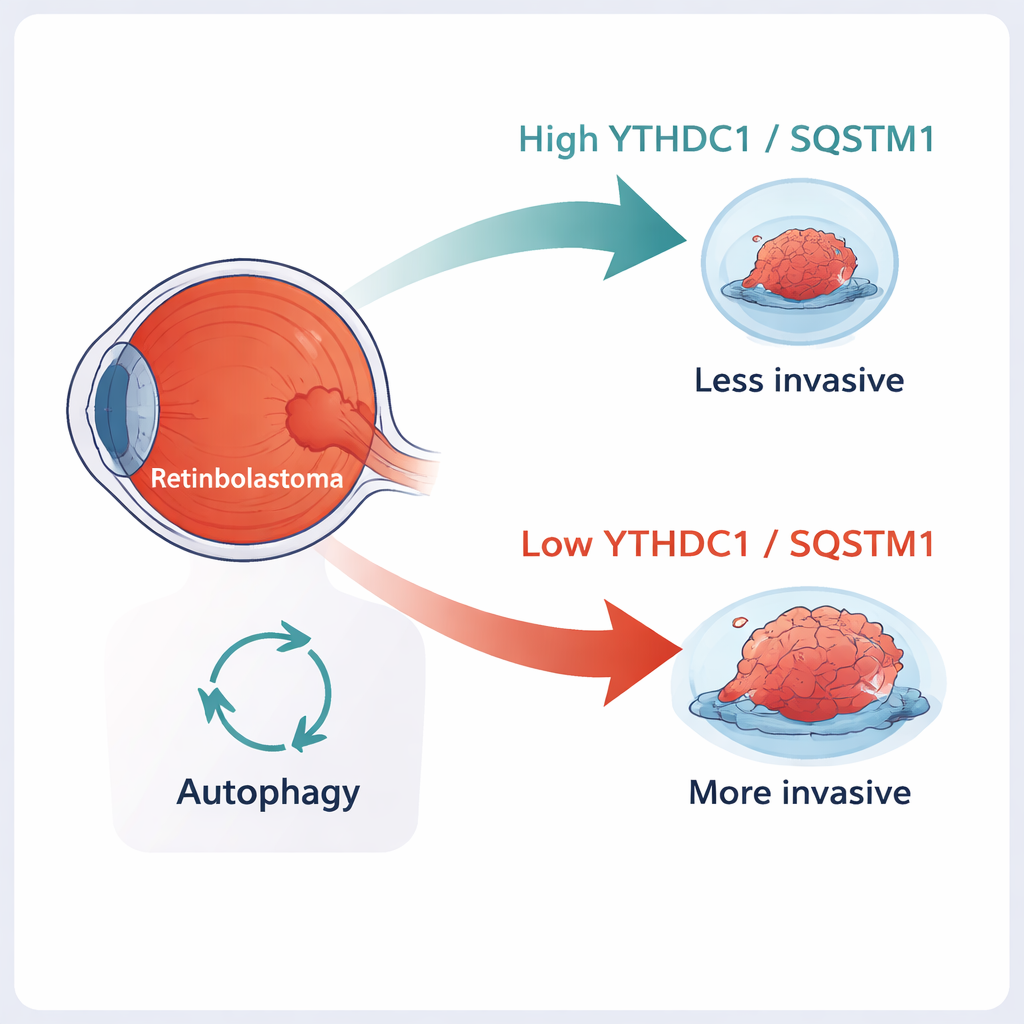
En närmare titt på barndomens ögtumörer
Retinoblastom uppstår från ögats ljuskänsliga lager, näthinnan, vanligtvis hos barn under fem år. Klassiskt börjar sjukdomen när båda kopiorna av ett skyddande gen, RB1, förloras. Men förlust av RB1 förklarar inte fullt ut varför vissa tumörer förblir begränsade till ögat medan andra gräver sig in i närliggande vävnader eller sprider sig längs synnerven. Forskare har i allt större utsträckning insett att kemiska märken som placeras på RNA — de tillfälliga budskapen som berättar vilka proteiner cellen ska tillverka — kan påverka hur cancer beter sig. En av de vanligaste märkningarna, kallad m6A, kan förändra hur stabila dessa budskap är och hur länge de kvarstår i cellen.
Upptäckten av en saknad molekylär broms
Författarna började med att jämföra genaktiviteten i tumörer som stannade inne i ögat med sådana som redan blivit invasiva. Genom att använda en offentlig RNA-sekvenseringsdataset från retinoblastomprover identifierade de tusentals gener vars aktivitet skilde sig mellan de två grupperna och koncentrerade sig sedan på viktiga m6A-"regulatorer." Dessa inkluderar enzymer som lägger till eller tar bort m6A samt "läsar"-proteiner som tolkar märkningen. Bland tio stora regulatorer fann de att en läsare, YTHDC1, konsekvent var lägre i invasiva tumörer. När de undersökte prover från 50 barn och utförde laboratorietester på tumörvävnad bekräftade de att nivåerna av YTHDC1 — både dess RNA och protein — var reducerade i mer aggressiva cancerformer.
YTHDC1 på prov
För att se vad YTHDC1 faktiskt gör manipulerade teamet dess nivåer i två mänskliga retinoblastomcellinjer. När de sänkte YTHDC1 med genetiska verktyg delade sig cellerna snabbare och kunde i högre grad ta sig genom konstgjorda membran som efterliknar vävnadsbarriärer — tecken på en mer invasiv tumör. I möss bildade celler utan YTHDC1 större, tyngre tumörer. Motsatsen gällde också: att tvinga fram extra YTHDC1 hos cellerna bromsade deras tillväxt och minskade deras förmåga att migrera och invadera. Dessa experiment tyder på att YTHDC1 fungerar som en tumörsuppressor och hjälper till att hålla tillbaka retinoblastoms farligaste egenskaper.
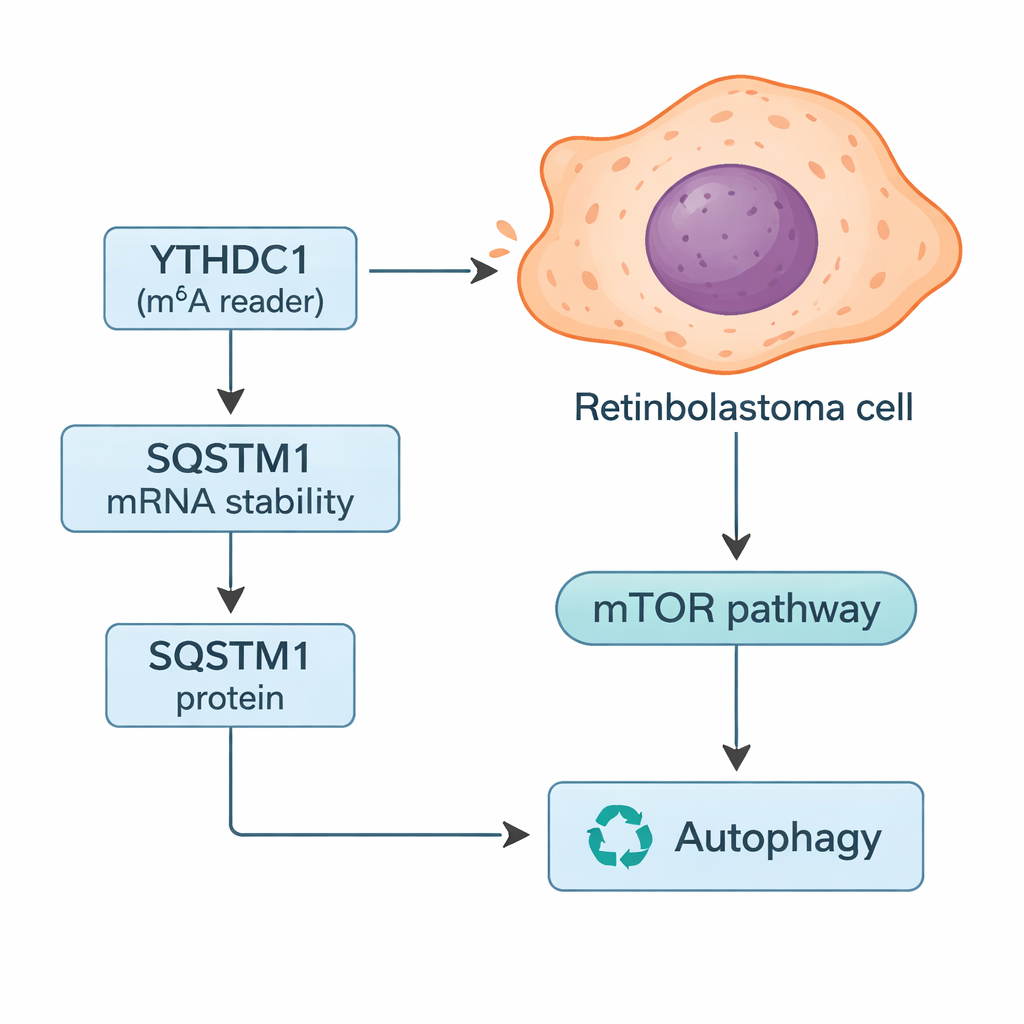
Hur YTHDC1 styr cellens återvinningssystem
Vid en djupare genomgång sökte forskarna efter specifika gener vars budskap kan kontrolleras av YTHDC1. Genom att kombinera databassökningar med sina tumördata fokuserade de på SQSTM1, ett protein bättre känt som p62. SQSTM1 hjälper till att reglera autofagi, cellens återvinningssystem som bryter ner skadade komponenter och kan ge bränsle när resurser är knappa. Studien visade att YTHDC1 fysiskt binder till SQSTM1:s RNA och stabiliserar det, vilket tillåter mer SQSTM1-protein att bildas. När YTHDC1 minskade föll SQSTM1-nivåerna och dess RNA bröts ner snabbare. Att tysta SQSTM1 ensam gjorde att retinoblastomceller växte och invaderade mer, och det utplånade delvis de skyddande effekter som sågs när YTHDC1 överuttrycktes, vilket placerar SQSTM1 som en viktig mellanstation i denna väg.
Autofagi, energi och tumöraggressivitet
Eftersom SQSTM1 är centralt för autofagi testade teamet hur förändringar i YTHDC1 och SQSTM1 påverkar detta återvinningsförlopp. Med en kombination av fluorescerande markörer och proteinmätningar fann de att minskad nivå av antingen YTHDC1 eller SQSTM1 ökade autofagiskt "flöde" — mer cellulärt material fördes in i och genom återvinningssystemet. De observerade också förändringar i mTOR-vägen, en viktig näringskännande brytare som normalt håller autofagin i schack. Med mindre SQSTM1 sjönk mTOR-aktiviteten, vilket stämmer med ökad autofagi. I invasivt retinoblastom föreslår författarna att reducerad YTHDC1 leder till svagare SQSTM1-signaler, dämpad mTOR-aktivitet och ökad autofagi som hjälper tumörceller att överleva stress och sprida sig.
Vad detta betyder för framtida behandlingar
För en icke-specialist är huvudbudskapet att denna studie identifierar en händelsekedja inne i retinoblastomceller — YTHDC1 som kontrollerar SQSTM1, vilket i sin tur formar cellens återvinningsmaskineri — som påverkar hur aggressiv cancern blir. När denna kedja försvagas växer tumörer snabbare och invaderar mer. Även om mycket arbete återstår innan dessa rön kan nå kliniken, erbjuder vägen nya idéer för terapi: återställa YTHDC1-funktionen, stabilisera SQSTM1 eller finjustera autofagi och mTOR-aktivitet skulle en dag kunna komplettera befintliga cytostatikabehandlingar. För barn som drabbas av denna ögoncancer kan sådana riktade strategier hjälpa till att begränsa tumörspridning samtidigt som mer syn bevaras och behandlingsbiverkningar minskas.
Citering: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
Nyckelord: retinoblastom, YTHDC1, SQSTM1, autofagi, mTOR-väg