Clear Sky Science · sv
Irisin reglerar lipidmetabolism och ferroptos i ovariecancerceller genom att modulera ALOX5–5‑HETE–PD‑L1‑axeln
Varför denna växtmolekyl är viktig för äggstockscancer
Äggstockscancer är en av de dödligaste cancerformerna hos kvinnor eftersom den ofta upptäcks sent och ofta återkommer efter behandling. Denna studie undersöker om en naturlig förening kallad tectorigenin, som finns i växten Belamcanda chinensis, kan bromsa äggstockscancer genom att beröva tumörceller vissa fetter och tvinga dem in i en särskild form av järn‑driven celldöd. Den undersöker också hur denna förening kan försvaga den ”osynlighetskappa” som tumörer använder för att dölja sig för immunsystemet.
En dold bränslekälla inne i tumörceller
Liksom många andra cancerformer omprogrammerar äggstockstumörer hur de hanterar fetter. Istället för att enbart använda fetter som energi lagrar cancerceller dem som byggstenar för nya membran och som buffertar mot skada. I odlade äggstockscancerceller ledde tillskott av enkelomättade fettsyror till en ansamling av fria fettsyror, triglycerider och kolesterol—viktiga former av lagrat fett. Detta överskott av fett gjorde att cellerna växte och invaderade lättare och hjälpte dem att motstå en destruktiv process kallad ferroptos, där järn och oxiderade fetter samverkar för att få cellmembran att brista. Med andra ord gav abnorm lipidmetabolism cancern en tillväxtfördel och ett överlevnadsskydd.
Att tvinga cancerceller mot självförstörelse
Forskarna testade därefter tectorigenin på både normala äggstocksceller och flera äggstockscancercellinjer. Vid doser upp till 200 mikrogram per liter skadade föreningen inte normala celler men hämmade tydligt cancercellernas tillväxt, minskade deras förmåga att invadera genom ett membran och ökade deras grad av programmerad celldöd. När cancerceller förbehandlades med ett ferroptosblockerande läkemedel blev de mer aggressiva. Tillsats av tectorigenin återställde dessa effekter: fettlagren minskade, nivåerna av järn‑ och oxidationsrelaterade skademarkörer ökade och fler celler dog. I musemodeller med mänskliga äggstockstumörer krympte tumörerna vid injektioner av tectorigenin, fettinnehållet i tumörvävnad minskade och kemiska tecken på ferroptos ökade — vilket åter antyder att föreningen driver cancerceller mot denna järnberoende dödsväg.
En nyckelregulator som kopplar ihop fetter och immunflykt
För att ta reda på hur tectorigenin verkar på molekylär nivå kombinerade teamet stordata‑analys med datorbaserad modellering av läkemedels–protein‑interaktioner. De fokuserade på ett enzym kallat ALOX5, som omvandlar en vanlig fettsyra till en signalsubstans kallad 5‑HETE. I äggstockscancerceller och tumörprover var ALOX5‑nivåerna mycket högre än i normal vävnad. Datorisk dockning och molekylära dynamik‑simulationer visade att tectorigenin kan binda stabilt till ALOX5 och fungera som en intern broms. När forskarna konstgjort ökade ALOX5 i cancerceller ökade fettlagren, markörer för ferroptos minskade och cellerna blev mer invasiva. Behandling med tectorigenin upphävde dessa förändringar. Nedreglering av ALOX5 gav motsatt effekt—mindre fett, mer ferroptos och svagare tillväxt—vilket tydligt placerar detta enzym i centrum för föreningens effekt.
Hur tumörer förlorar sitt skydd mot immunsystemet
Studien kopplade också denna lipidväg till ett viktigt immuncheckpunktmolekyl kallad PD‑L1, som tumörer använder för att stänga av angripande immunceller. ALOX5:s produkt 5‑HETE ökade PD‑L1‑nivåerna och stärkte detta skydd. När ALOX5 tystades minskade både 5‑HETE och PD‑L1; när 5‑HETE återintroducerades ökade PD‑L1 igen och cancercellerna återfick en del av sitt skydd mot ferroptos. Tectorigenin minskade ALOX5, sänkte 5‑HETE och i förlängningen reducerade PD‑L1 i cellkulturer och i mus‑tumörer. Detta tyder på att genom att rikta in sig på ett enda metabolismenzym kan föreningen både störa tumörernas fettbaserade försvar och försvaga deras förmåga att gömma sig från immunsvar.
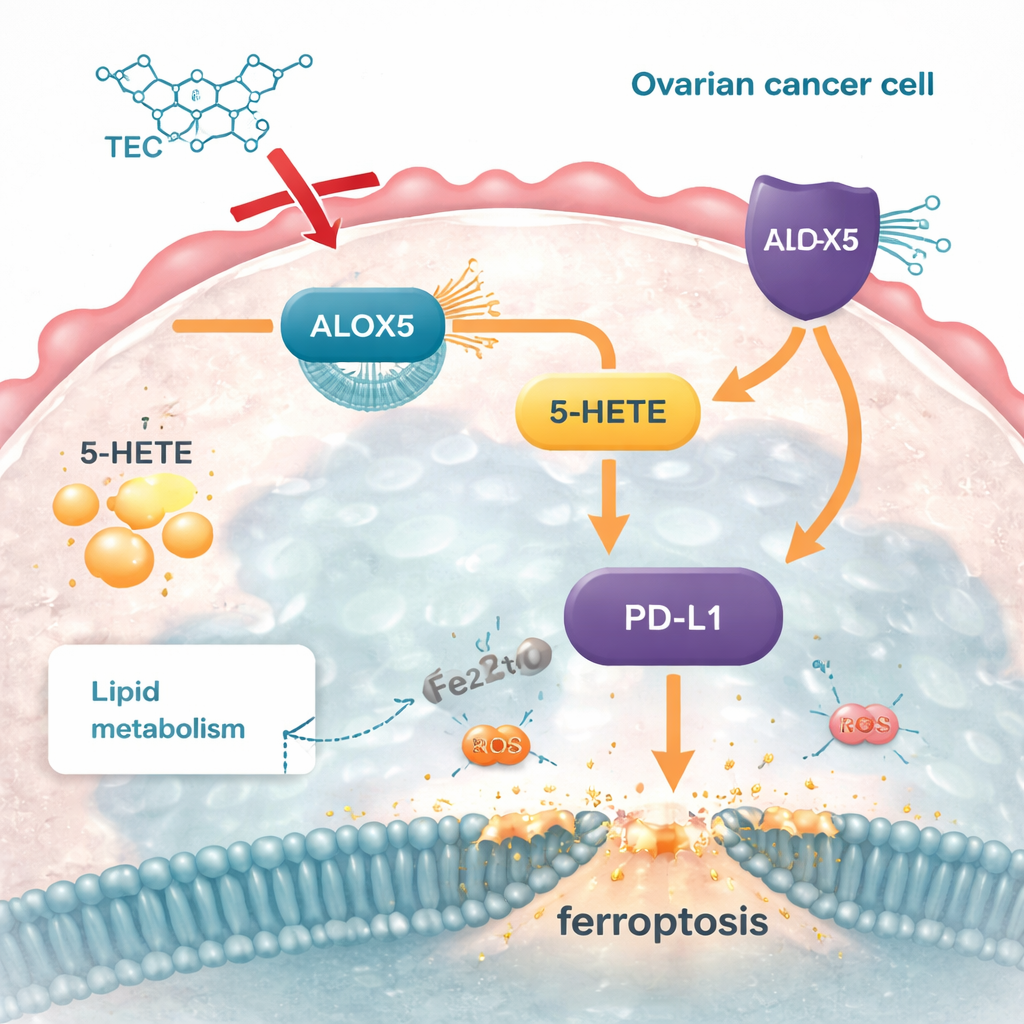
Vad detta kan innebära för framtida behandlingar
Kort sagt visar detta arbete att tectorigenin fungerar som ett precist verktyg som stör en cancercells fett‑hantering. Genom att blockera ALOX5 stoppar det produktionen av 5‑HETE, minskar överskottet av fettlager, gör cellerna sårbara för järn‑driven skada och avlägsnar en del av deras immunkamouflage. Även om dessa fynd härrör från cell‑ och musstudier — och mycket återstår att pröva på människor — pekar de mot en lovande strategi: att rikta in sig på ALOX5–5‑HETE–PD‑L1‑axeln för att både svälta äggstockstumörer och göra dem lättare för kroppens egna försvar, eller framtida immunoterapier, att eliminera.
Citering: Cai, H., Huang, C. & Zhang, Z. Irisin regulates lipid metabolism and ferroptosis in ovarian cancer cells by modulating the ALOX5-5-HETE-PD-L1 axis. Sci Rep 16, 7223 (2026). https://doi.org/10.1038/s41598-026-36816-4
Nyckelord: äggstockscancer, lipidmetabolism, ferroptos, ALOX5, naturlig ämnesbehandling