Clear Sky Science · sv
Utveckling och validering av en PSMA-positiv trippelnegativ bröstcancermusmodell för prekliniska riktade radionuklidbehandlingar
Varför denna forskning är viktig
Trippelnegativ bröstcancer är en av de svåraste formerna av bröstcancer att behandla. Den sprider sig ofta snabbt, erbjuder färre riktade behandlingsalternativ för patienterna och återkommer ofta efter standardbehandlingar. Samtidigt har en ny klass av ”smarta” radioaktiva läkemedel som binder till en specifik molekyl kallad PSMA förändrat vården vid avancerad prostatacancer. Denna studie ställer en enkel men potent fråga: kan vi bygga en realistisk laboratoriemodell av trippelnegativ bröstcancer som bär samma PSMA-mål, så att vi rättvist kan pröva om dessa smarta radioaktiva läkemedel också kan hjälpa patienter med denna aggressiva bröstcancer?
Från prostatamål till bröstcancerns utmaning
PSMA, förkortning för prostate-specific membrane antigen, är en liten struktur som sitter på ytan av vissa celler. Den är rikligt förekommande i många prostatacancer och kan kännas igen av radioaktiva läkemedel som både avslöjar tumörer på skanningar och levererar strålning direkt till dem. Forskare har nyligen upptäckt att PSMA också förekommer, i varierande grad, i blodkärl och celler i flera andra tumörer, inklusive trippelnegativ bröstcancer. I dessa icke-prostattumörer är PSMA dock ofta fläckvis och svagare, vilket gör det svårt att veta om PSMA-riktade terapier kommer att fungera. Innan nya behandlingar prövas på patienter behöver forskarna djurmodeller som troget efterliknar detta PSMA-mönster i brösttumörer—något som visat sig vara förvånansvärt svårt att åstadkomma.
Test av många tumörmodeller som vägrade samarbeta
Forskargruppen undersökte först ett brett spektrum av befintliga musmodeller för trippelnegativ bröstcancer, med både mus- och humana cancercellinjer inplanterade på olika platser och under varierande förhållanden. De ändrade antalet injicerade cancerceller, tillsatte stödjande geler för att främja blodkärlsbildning och blandade till och med in humana blodkärlsceller i hopp om att höja PSMA-nivåerna. För varje modell mätte de hur tillförlitligt tumörer etablerade sig och växte, granskade tumörsnitt i mikroskop och använde en PSMA-sökande PET-tracer för att se om tumörerna lystes upp i helkroppsskanningar. Trots robust tumörtillväxt och rikliga nätverk av blodkärl visade ingen av dessa 23 modeller märkbar PSMA-närvaro, varken vid vävnadsfärgning eller på PET-avbildning. Tumörerna såg aktiva och välförsörjda ut, men den specifika PSMA-"dockningsplats" forskarna behövde var i praktiken frånvarande.
Konstruera en tumör som visar rätt mål
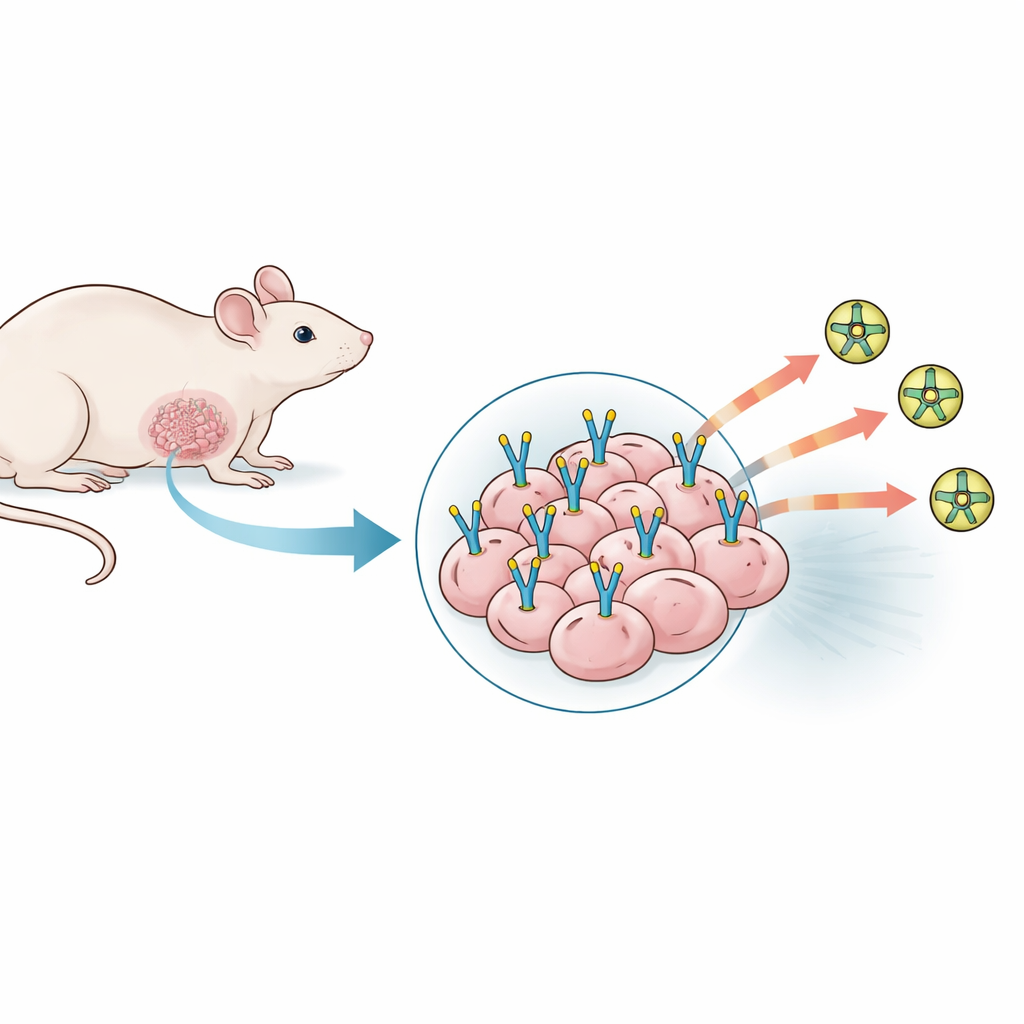
Inför detta hinder valde forskarna en mer direkt väg. De genetiskt modifierade en allmänt använd human trippelnegativ bröstcancercellinje, MDA-MB-231, för att tvinga fram uttryck av PSMA på ytan. Dessa förändrade celler implanterades sedan i spenfettet hos immundefekta möss, en plats som bättre efterliknar den naturliga bröstmiljön. Forskarna skapade två versioner av modellen: en där alla tumörceller uttryckte PSMA, och en annan "blandad" tumör som innehöll lika delar PSMA-positiva och vanliga cancerceller, för att efterlikna de fläckvisa mönster som ses hos patienter. Båda modellerna bildade tumörer lika tillförlitligt och växte i liknande hastighet som tumörer från omodifierade celler, vilket visar att tillsatsen av PSMA inte fick cancern i sig att bete sig onormalt.
Se det nya målet på skanningar och i mikroskopet
När den PSMA-sökande PET-tracern injicerades i dessa möss lyste de konstruerade tumörerna starkt på skanningarna, med tumörupptag ungefär tio gånger högre än i lever eller muskel. Denna starka och selektiva signal bekräftade att PSMA nu fanns i riklig mängd på cancercellerna och kunde nås av ett cirkulerande läkemedel. Mikroskopisk analys av tumörvävnad stämde överens: PSMA-färgning var hög men ojämn, med fläckar av starkare och svagare uttryck som liknade det heterogena mönster som observeras i humana trippelnegativa bröstcancer. Viktigt var att det tillsatta PSMA:t var begränsat till tumörcellerna, inte de omgivande blodkärlen, vilket höll modellen inriktad på cellmålade terapier. Områden med död vävnad inne i större tumörer tog inte upp tracern, vilket stämmer med kliniska observationer.
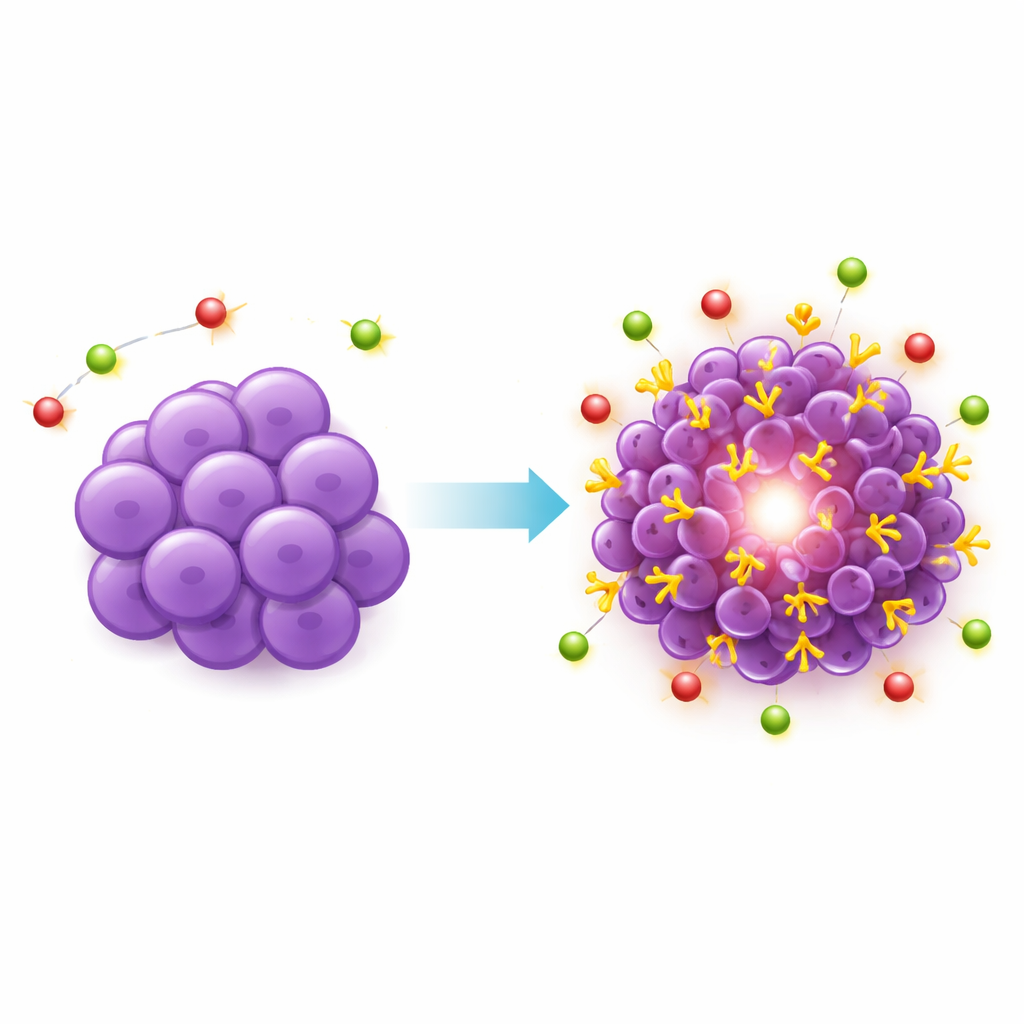
Vad detta betyder för framtida behandlingar
Genom att systematiskt visa att standardmodeller för bröstcancer inte pålitligt uttrycker PSMA och sedan konstruera en ny modell som gör det, ger detta arbete en avgörande testbädd för nästa generations riktade strålningsbehandlingar. Den PSMA-positiva trippelnegativa bröstcancermodellen är stabil, växer förutsägbart och visar en realistisk blandning av områden med högt och lågt PSMA-uttryck, vilket gör den väl lämpad för att utvärdera hur PSMA-riktade läkemedel beter sig innan de prövas på patienter. Även om denna modell inte kan fånga alla aspekter av mänsklig sjukdom—såsom påverkan av ett fullgott fungerande immunsystem—erbjuder den ett kraftfullt verktyg för att utforska om framgångarna med PSMA-baserade terapier vid prostatacancer en dag kan utsträckas till personer med denna särskilt aggressiva form av bröstcancer.
Citering: Chaussin, B., Sanchez, L., Levesque, S. et al. Development and validation of a PSMA-positive triple-negative breast cancer mouse model for preclinical targeted radionuclide therapies. Sci Rep 16, 9348 (2026). https://doi.org/10.1038/s41598-026-36724-7
Nyckelord: trippelnegativ bröstcancer, PSMA, riktad radionuklidterapi, preklinisk musmodell, PET-avbildning