Clear Sky Science · sv
Kan evolutionär terapi tillämpas vid icke‑småcellig lungcancer?
Att tänka om cancerbehandling som en evolutionär tävling
Cancerbehandling skildras ofta som en enkel strid: ge så starka läkemedel som möjligt och försök utplåna varje sista cancercell. Men vid snabba, aggressiva cancerformer som avancerad icke‑småcellig lungcancer (NSCLC) slår denna "maximala attack" ofta fel. Tumörer krymper inledningsvis, men växer nästan alltid tillbaka — nu dominerade av läkemedelsresistenta celler. Denna studie ställer en provocerande fråga: vad om läkare, istället för att försöka utplåna tumören, behandlade den som ett föränderligt ekosystem och använde doseringsscheman som medvetet låter vissa läkemedelskänsliga celler överleva för att hålla de resistenta cellerna i schack?
Varför standardbehandling med höga doser kan påskynda resistens
I dagens praxis får patienter med metastaserad NSCLC och vissa genetiska förändringar ofta dagliga tabletter kallade tyrosinkinashämmare (TKI), som erlotinib. Dessa läkemedel kan dramatiskt minska tumörer till en början, men nästan alla patienter får så småningom återfall eftersom resistenta cancerceller överlever och tar över. När läkare driver dosen till det maximalt tolererbara dödar de främst de känsliga cellerna som svarar väl på läkemedlet. Resistent celler, som kan överleva även höga doser, möter plötsligt mindre konkurrens om utrymme och näring. Resultatet är en evolutionär "seger" för de tuffaste cancercellerna, och tumören återkommer slutligen, nu mycket svårare att behandla. 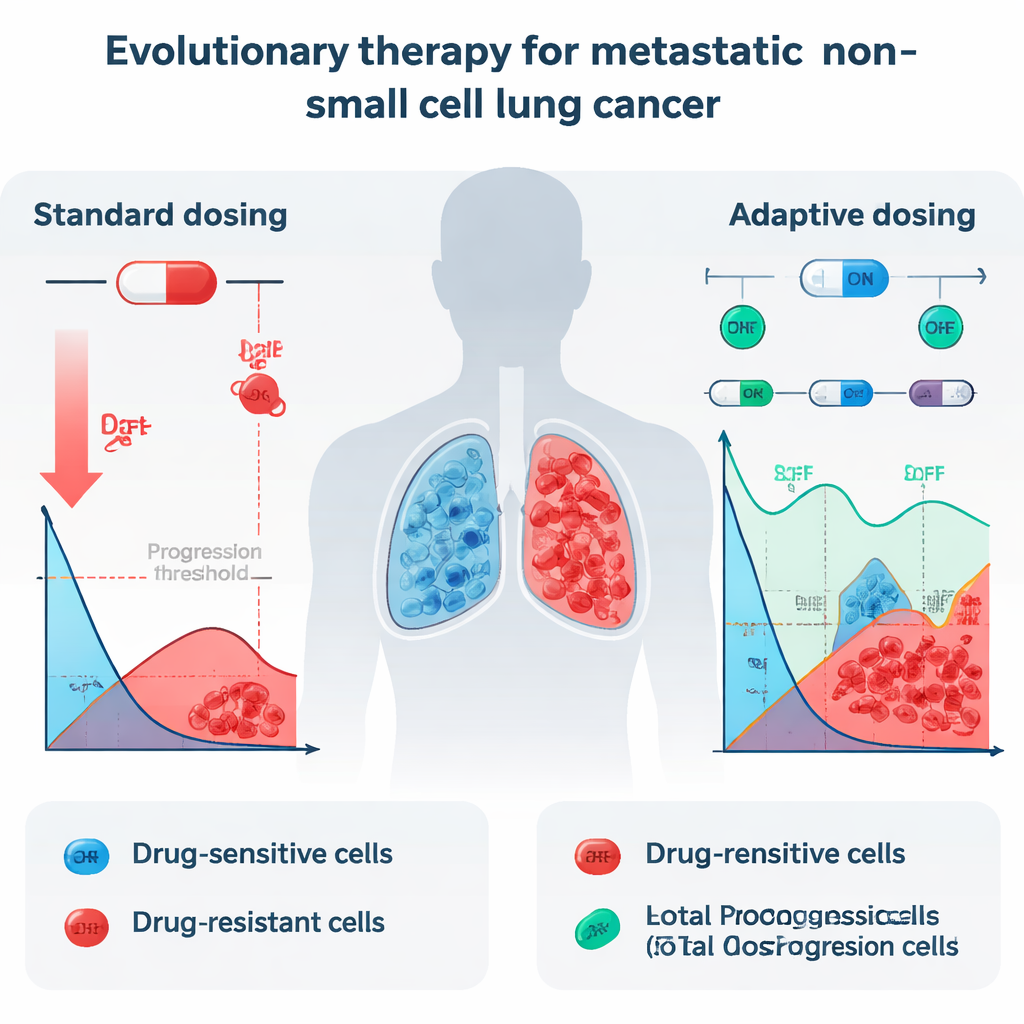
Att använda matematik för att testa en ny doseringsstrategi på verkliga patienter
Forskarna undersökte om en annan strategi, kallad evolutionär terapi, kunde fungera vid stadium IV NSCLC. Evolutionär terapi syftar inte till att utrota tumören helt. I stället försöker den kontrollera tumören genom att upprätthålla en stabil blandning av känsliga och resistenta celler, så att de känsliga cellerna "tränger ut" de resistenta. Teamet lånade ett specifikt av‑och‑på‑doseringsprotokoll som redan visat lovande resultat vid prostatacancer och frågade: skulle denna typ av strategi teoretiskt kunna vara effektiv även för lungcancer? För att besvara detta analyserade de detaljerade tumörstorleksmätningar från 13 NSCLC‑patienter behandlade med erlotinib i en klinisk prövning, omvandlade skannarna till total tumörvolym över tid och matade dessa data in i en svit av matematiska modeller.
Att hitta modellen som verkligen fångar upp resistens
Forskarna testade 26 olika modeller för tumörtillväxt, alla med en uppdelning av cancerceller i två grupper: läkemedelskänsliga och läkemedelsresistenta. Dessa modeller skilde sig åt i hur de beskrev tillväxtbegränsningar, hur de två celltyperna konkurrerar med varandra, hur läkemedlet hanteras i kroppen och hur behandlingen dödar celler. Många enklare modeller passade patientdata hyfsat väl när tumörer bara krympte. Men när tumörerna följde en mer realistisk "U‑formad" bana — krympande vid behandling och sedan återväxande när resistens uppstod — misslyckades de flesta modeller. Bäst överensstämmelse gav en typ kallad Gompertziansk modell som innehöll två avgörande idéer: för det första kan tumörer inte växa utan gräns (de påverkas av trängsel), och för det andra konkurrerar känsliga och resistenta celler asymmetriskt, så framgången för den ena typen beror på hur många av den andra typen som finns.
Simulering av adaptiv terapi jämfört med standardvård
När de identifierat de bäst passande modellerna använde teamet dem för att simulera två behandlingsstrategier för varje patient: vanligtvis konstant maximal dos och ett adaptivt protokoll inspirerat av Zhang och kollegor. I den adaptiva metoden ges erlotinib tills tumören minskat till hälften av sin ursprungliga storlek, därefter pausas läkemedlet för att tillåta att känsliga celler återvuxer; behandlingen återupptas när tumören åter når sin startstorlek, och cykeln upprepas. Över alla välfungerande modeller som inkluderade konkurrens mellan celltyper fördröjde denna adaptiva strategi konsekvent tiden tills tumören översteg 110 % av sin ursprungliga storlek — en vanlig gräns för progression. I den bäst passande Gompertzianska modellen med konkurrens ökade medianen för tid till progression från cirka 24,8 månader under standarddosering till 42,3 månader under den adaptiva protokollet, en förbättring på ungefär ett och ett halvt år. 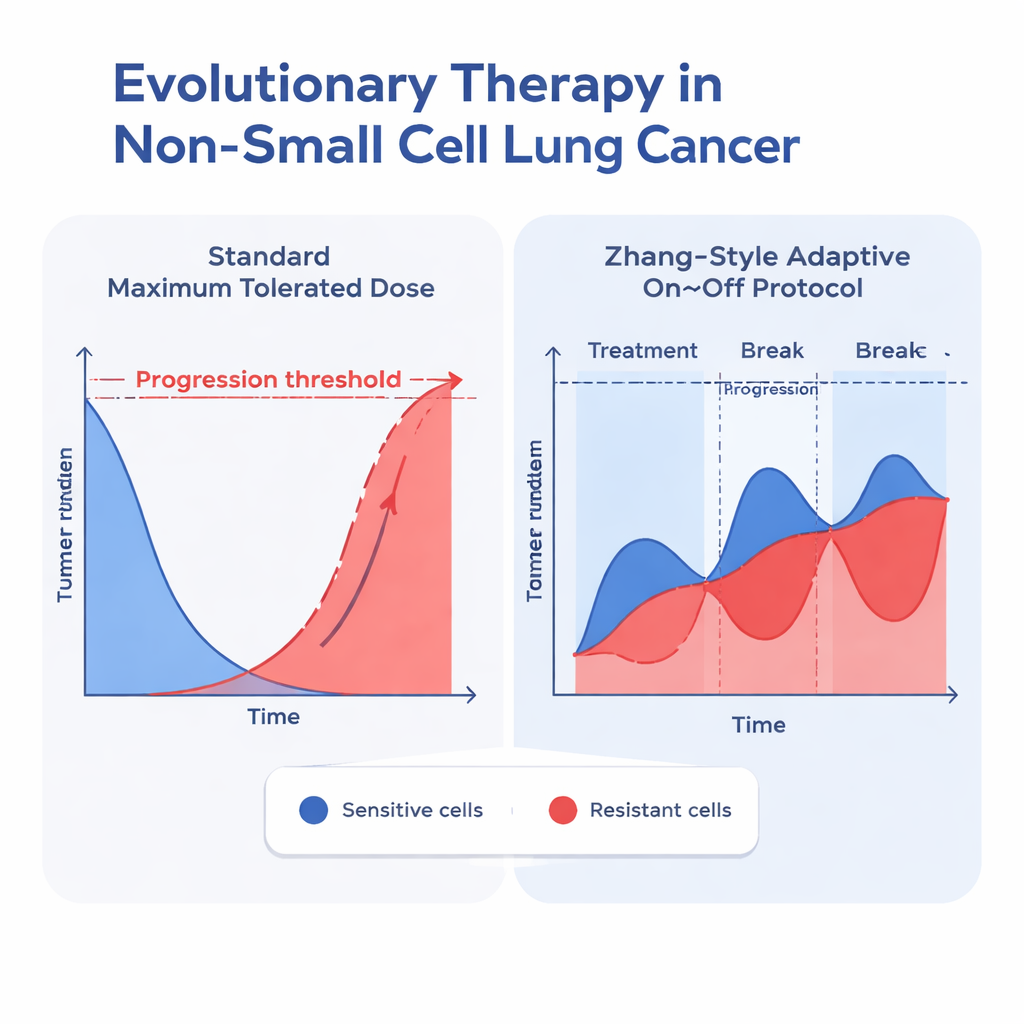
Vad detta kan innebära för framtida patienter
Detta arbete ändrar ännu inte hur läkare behandlar NSCLC‑patienter i dag, men det erbjuder ett kraftfullt konceptbevis. Genom att förankra sina modeller i verkliga patientdata och kräva att modellerna reproducerar inte bara tidig krympning utan också återväxt driven av resistens visar författarna att evolutionär terapi teoretiskt är möjlig även vid en snabbväxande och dödlig cancer. Deras resultat tyder på att noggrant timade behandlingsuppehåll skulle kunna förlänga kontrollen av sjukdomen genom att använda läkemedelskänsliga celler som allierade snarare än kollaterala offer. För att förvandla denna idé till praktik krävs dock mer data, bättre biomarkörer som blodtester som följer tumör‑DNA, och rigorösa kliniska prövningar. Ändå är budskapet till allmänheten tydligt: ibland är det smartaste sättet att bekämpa cancer inte att slå så hårt som möjligt, utan att styra dess evolution så att den förblir en hanterbar, långsammare fiende.
Citering: Jansén-Storbacka, L.R., Honasoge, K.S., Molnárová, E. et al. Can evolutionary therapy be applied in non-small cell lung cancer?. Sci Rep 16, 7442 (2026). https://doi.org/10.1038/s41598-026-36712-x
Nyckelord: evolutionär terapi, icke‑småcellig lungcancer, läkemedelsresistens, adaptiv dosering, matematisk onkologi