Clear Sky Science · sv
Klinisk validering av lätta CNN-arkitekturer för pålitlig flerkategori-klassificering av lungcancer med histopatologiska avbildningstekniker
Varför denna forskning är viktig för patienter och läkare
Lungcancer är ofta dödlig eftersom den upptäcks sent eller felklassificeras, vilket kan fördröja rätt behandling. Denna studie undersöker hur små, effektiva datorprogram—snarare än stora, strömkrävande modeller—på ett tillförlitligt sätt kan känna igen olika typer av lungcancer från mikroskopbilder av vävnad. Om sådana lätta verktyg fungerar väl kan de användas på sjukhus över hela världen, även där datorkapaciteten är begränsad, för att stödja patologer i att göra snabbare och mer konsekventa diagnoser.
En närmare titt på cancer med digitala mikroskop
När en misstänkt lungnodul tas bort eller biopsieras undersöker patologer tunt skivade, färgade vävnadsprov under mikroskop för att avgöra om det är ofarligt eller tillhör en av flera cancertyper. I detta arbete fokuserar författarna på tre huvudkategorier: benign lungvävnad, lungadenocarcinom och lungskivepitelkarsinom. Dessa undertyper är viktiga eftersom de svarar olika på behandlingar. Teamet använder digitala ögonblicksbilder av dessa preparat—histopatologiska bilder—och undersöker om kompakta neurala nätverk kan lära sig de subtila visuella mönstren som skiljer varje klass åt, från cellformer till vävnadsarkitektur, lika pålitligt som mycket större modeller.
Bygga mindre men smartare digitala klassificerare
De flesta toppmoderna bildigenkänningssystem är extremt stora och kräver dyra grafiska processorer, vilket gör dem svåra att driftsätta i många kliniker. Forskarna designar istället fyra «lite»-bildanalysmodeller, kallade Lite-V0, Lite-V1, Lite-V2 och Lite-V4, var och en en strömlinjeformad version av ett konvolutionellt neuralt nätverk (CNN). Alla fyra följer samma grundrecept: de extraherar gradvis visuella drag genom ett lager av enkla byggstenar, sammanfattar bilden och ger en av de tre lungvävnadsetiketterna. Det som skiljer versionerna åt är hur många block som används och hur breda de är—i praktiken hur mycket kapacitet modellen har att lära sig komplexa mönster. Denna kontrollerade design låter teamet studera hur mycket komplexitet som verkligen behövs för pålitlig cancerklassificering.
Träning, testning och val av den mest rättvisa modellen
För att lära upp och testa dessa modeller sammanställer författarna en balanserad samling på 15 000 lungvävnadsbilder, noggrant uppdelade i tränings-, validerings- och testgrupper med lika många från varje klass. Innan träning ändras bildstorlek, normaliseras och förstärks försiktigt med speglingar, små rotationer och zoomningar för att efterlikna hur preparat kan se ut under olika förhållanden. Avgörande är att teamet inte bedömer modeller enbart utifrån rå noggrannhet, eftersom den metriska kan dölja svag prestanda för en klass. Istället använder de ett «macro-F1»-mått, vilket tvingar modellen att prestera väl för alla tre vävnadstyper, inte bara de enklaste. En specialanpassad träningsprocedur övervakar kontinuerligt detta balanserade mått och stoppar automatiskt träningen när förbättringarna planar ut, och sparar bästa versionen av varje modell för jämförelse. 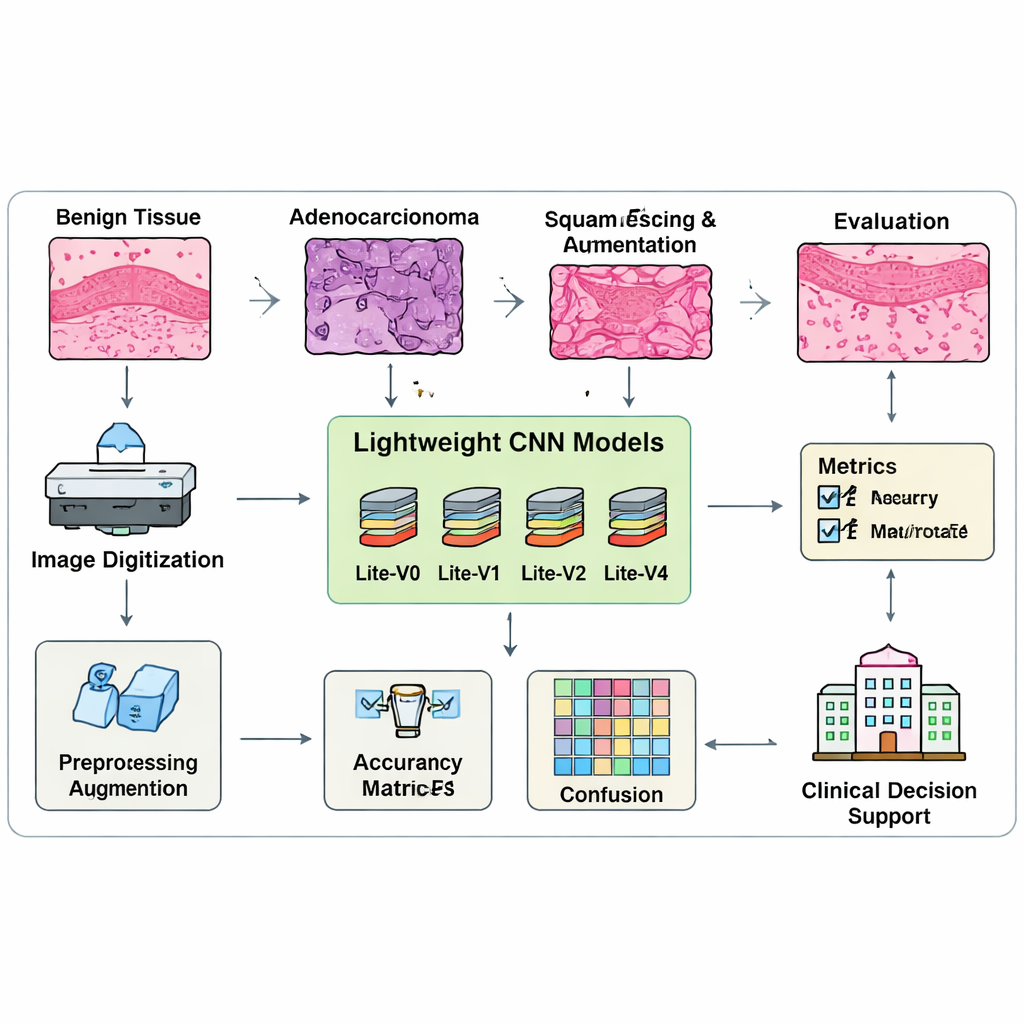
Vad den bästa lätta modellen verkligen kan göra
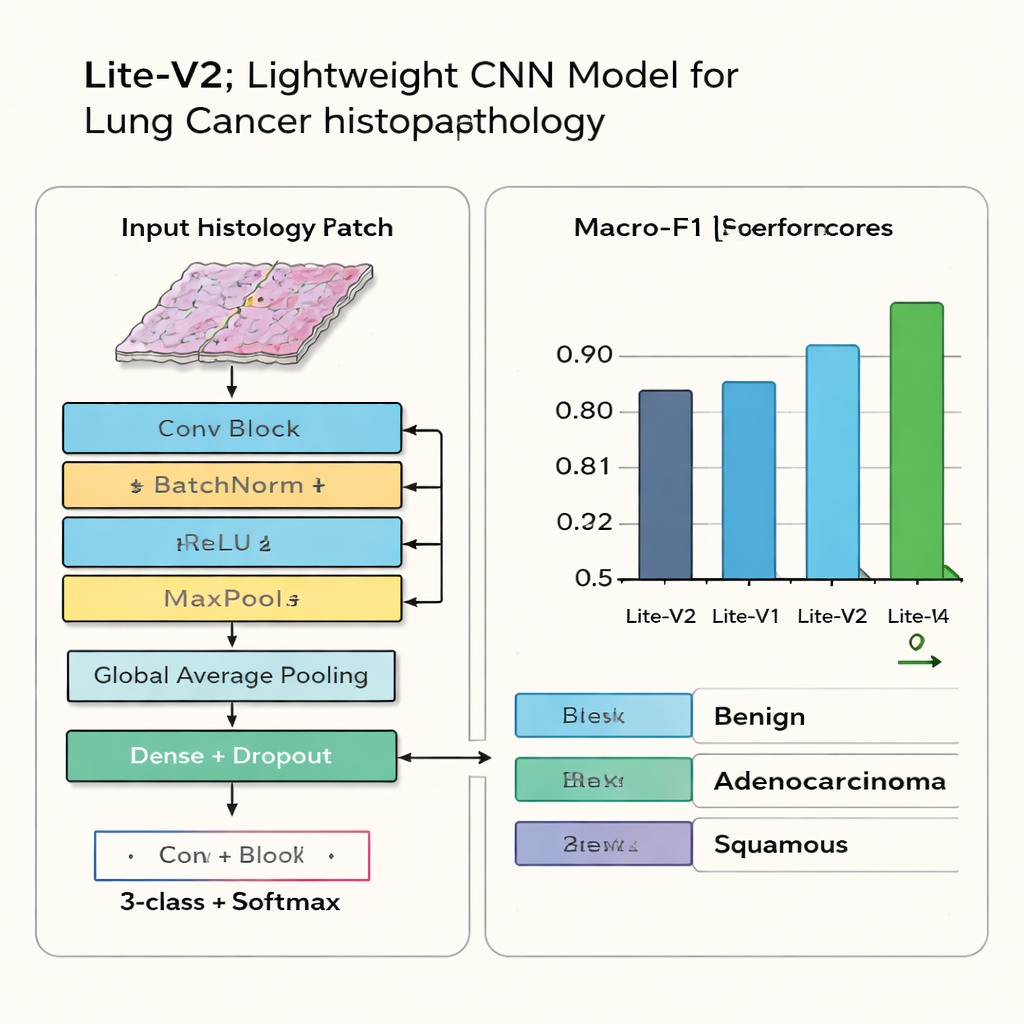
När dammet lagt sig står en variant—Lite-V2—ut. Den är varken det minsta nätverket eller det största, utan hamnar i mitten och uppnår den bästa balansen mellan noggrannhet och effektivitet. På osedda testbilder klassificerar Lite-V2 korrekt benign vävnad, adenocarcinom och skivepitelkarsinom med hög och jämnt fördelad prestanda, och når en macro-F1-poäng på ungefär 0,96. Förväxlingsmatriser visar att den sällan blandar ihop de tre kategorierna, medan djupare varianter börjar "överanpassa", minnas träningsdata men tappa tillförlitlighet på nya fall. Författarna kör dessutom om Lite-V2 flera gånger med olika slumpmässiga startpunkter och använder ett statistiskt test för att bekräfta att dess fördel över de andra varianterna inte beror på slump.
Från forskningskod till verkligt stöd
Bortom prestationssiffror betonar studien praktisk implementering. Eftersom Lite-V2 och dess syskon är kompakta kan de köras på modest sjukhushårdvara eller till och med på edge-enheter utan att behöva skicka känsliga bilder till molnet. Författarna publicerar ett reproducerbart ramverk som loggar varje experimentell detalj, från datapreparering till träningskurvor och felmönster, så att andra team kan verifiera eller bygga vidare på arbetet. För patienter och kliniker är huvudbudskapet att genomtänkt designade lätta AI-modeller kan hjälpa till att föra pålitlig klassificering av lungcancer närmare vardaglig patologipraktik, och stödja snabbare, mer konsekventa beslut—även i kliniker som saknar toppmodern datorkraft.
Citering: Raza, A., Hanif, F. & Mohammed, H.A. Clinical validation of lightweight CNN architectures for reliable multi-class classification of lung cancer using histopathological imaging techniques. Sci Rep 16, 6512 (2026). https://doi.org/10.1038/s41598-026-36652-6
Nyckelord: lungcancer, histopatologi, konvolutionella neurala nätverk, medicinsk bildbehandling AI, datorstödd diagnos