Clear Sky Science · sv
Kombinerade effekter av nitrat och antimikrobiella föreningar på in vitro subgingivala biofilmer
Varför ditt tandkött och tarmmedicin hänger ihop
Blödande tandkött och tandköttssjukdom skylls ofta på ”dåliga” bakterier. För att bekämpa dem använder tandläkare ofta starka munsköljmedel och antibiotika. Denna studie ställer en större fråga: vad händer om några av dessa behandlingar i tysthet skadar de hjälpsamma bakterierna vi behöver, medan ett enkelt näringsämne som finns i bladgrönsaker faktiskt skjuter våra munmikrober i riktning mot hälsa?
Tandköttssjukdom som ett gemenskapsproblem
Periodontit är en långvarig infektion runt tänderna som förstör de vävnader som håller dem på plats och är kopplad till hjärtsjukdom, diabetes och till och med hjärnrelaterade tillstånd. Istället för att orsakas av en enda mikrob uppstår den när hela munbakterie‑samhället skiftar till ett skadligt tillstånd, kallat dysbios. Modern behandling lutar fortfarande tungt mot bredverkande läkemedel: antibiotika som amoxicillin och metronidazol, och antiseptiska sköljningar som klorhexidin. Dessa produkter kan döda problematiska mikrober—men de kan också utplåna vänliga bakterier och kan främja läkemedelsresistens.
Närmare titt på biofilmer från verkliga patienter
För att se vad dessa behandlingar faktiskt gör med tandköttsbakterier samlade forskarna plack från djupa fickor runt tänderna hos 12 personer med periodontit. I laboratoriet odlade de dessa prover som tunna bakterielager, eller biofilmer, i åtta timmar under åtta olika förhållanden: ingen behandling, nitrat ensam, varje läkemedel ensam, och varje läkemedel kombinerat med nitrat. Nitrat, en naturlig förening rik i spenat, sallad och rödbeta, kan omvandlas av vissa munbakterier till kväveoxid, en gas som hjälper blodkärl att slappna av och kan bromsa tillväxten av sjukdomsrelaterade mikrober. Teamet mätte hur mycket biofilm som bildades, hur väl den omvandlade nitrat och vilka bakteriearter som frodades under varje behandling.
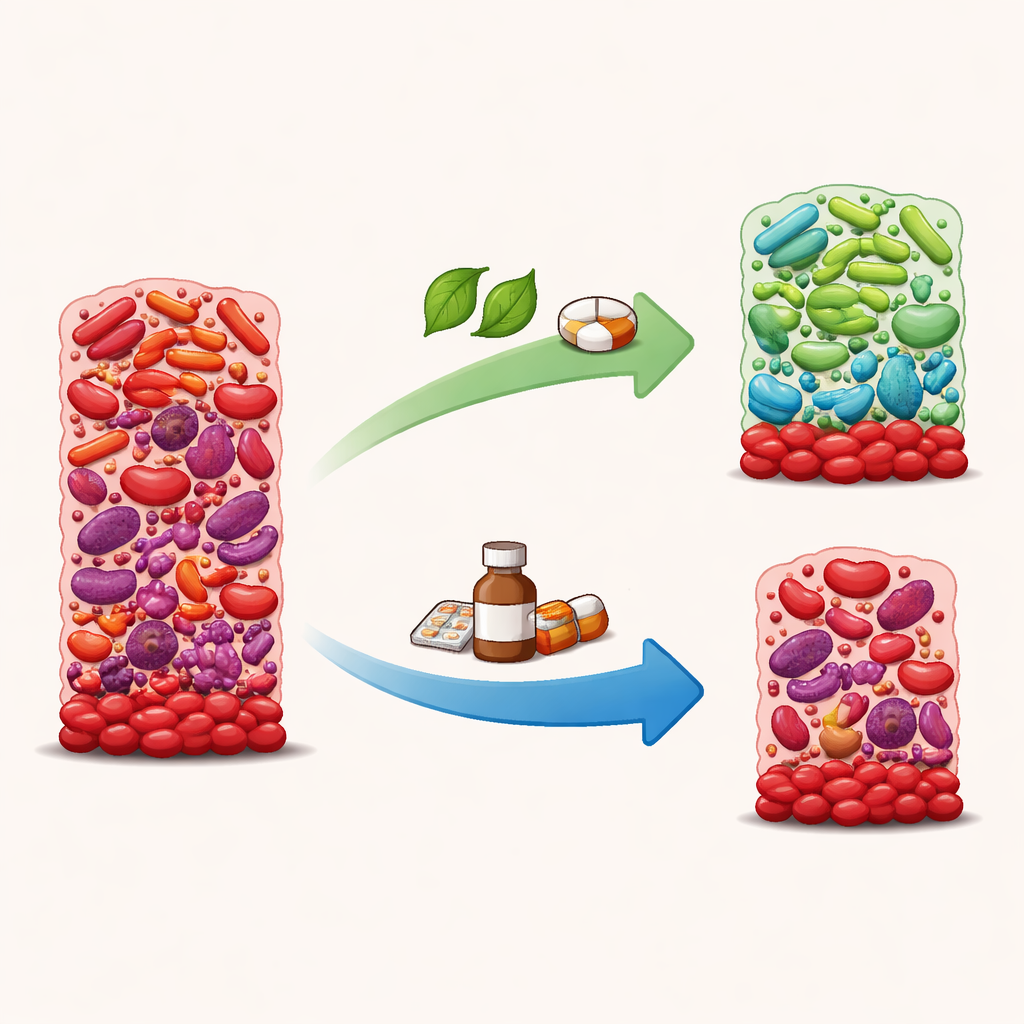
Läkemedel som krymper tillväxten men kan försämra balansen
Låga doser klorhexidin och amoxicillin halverade ungefär biofilmtillväxten och minskade kraftigt bakteriernas förmåga att bearbeta nitrat. Men detta var inte en selektiv ”bra städning”. DNA‑sekvensering visade att under dessa förhållanden tenderade hälsoassocierade bakterier som Rothia, Gemella och Kingella att minska, medan flera arter kopplade till tandköttssjukdom—inklusive Fusobacterium, Treponema och Eubacterium—antingen stod kvar eller blev mer framträdande. Ett index som poängsätter hur ”sjukt” ett samhälle ser ut i mikroskopet var högre med klorhexidin och amoxicillin än med nitrat, vilket tyder på att dessa läkemedel kan driva biofilmen mot ett mer skadligt, obalanserat tillstånd även när de dämpar den övergripande tillväxten.
Bladgrönt som bränsle och ett mildare antibiotikum
Nitrat berättade en annan historia. När placket odlades med nitrat ensam ökade bakterier som specialiserar sig på att omvandla nitrat till användbara produkter, såsom Neisseria och vissa Aggregatibacter‑arter. Dysbiospoängen sjönk jämfört med klorhexidin‑ eller amoxicillin‑förhållanden, vilket pekar mot ett hälsosammare samhälle. Metronidazol, vid en nivå lik den som faktiskt når tandköttsfickorna hos patienter, minskade inte starkt tillväxten eller nitratanvändningen på egen hand. Men när det kombinerades med nitrat verkade det vinkla balansen på ett hjälpsamt sätt: sjukdomsassocierade arter som Fusobacterium och Treponema minskade, medan nitrat‑användande Neisseria och Kingella ökade. Denna kombination verkade beskära de värsta förövarna utan att ta bort viktiga funktioner.
Vad detta betyder för vardaglig vård
För personer med tandköttssjukdom antyder dessa fynd att ”starkast” inte alltid är ”bäst” när det gäller antimikrobiella medel. I denna labbmodell saktade lågdoserade klorhexidin och amoxicillin ner bakterietillväxten men försvagade också en naturlig, nitratbaserad väg som stödjer både oral och kroppslig hälsa, och de var kopplade till mer sjukdomsliknande mikrobiella mönster. Nitrat, särskilt i kombination med metronidazol, gynnade bakterier förknippade med friskare tandkött och bevarade nitratmetabolismen. Även om verkliga munnar är mer komplexa än laboratoriefat, stöder detta arbete idén om skonsammare, mikrobiom‑vänliga strategier—såsom nitrat‑rika dieter och noggrant valda antibiotika—för att hantera tandköttssjukdom utan att underminera de bakterier som hjälper oss att må bra.
Citering: Moran, S.P., Nadal-Ruiz, M., Mira, A. et al. Combined effects of nitrate and antimicrobial compounds on in vitro subgingival biofilms. Sci Rep 16, 6686 (2026). https://doi.org/10.1038/s41598-026-36588-x
Nyckelord: tandköttssjukdom, munmikrobiom, nitrat, munskölj, antibiotika