Clear Sky Science · sv
Diagnos av Alzheimers sjukdom med hög noggrannhet via Petri-nätsmodellering av signalvägar
Varför tidig upptäckt av hjärnsjukdomar betyder något för oss alla
Alzheimers sjukdom urholkar långsamt minnet och förmågan att klara sig själv, ofta långt innan tydliga symptom syns. Dagens diagnostiska verktyg, som hjärnavbildning och kognitiva tester, kan vara dyra, svåra att få tillgång till och har låg känslighet i de tidigaste skedena. Denna studie introducerar ett nytt sätt att läsa kroppens molekylära ”kopplingar” med hjälp av blod- eller hjärnprover och ett matematiskt ramverk kallat Petri-nät. Målet är enkelt men djupt: att med mycket hög noggrannhet avgöra om en persons genaktivitetsmönster liknar en frisk individ eller en person med Alzheimers sjukdom—helst tidigt nog för att kunna påverka sjukdomsförloppet.
Att läsa sjukdom i kroppens signal"kretsar"
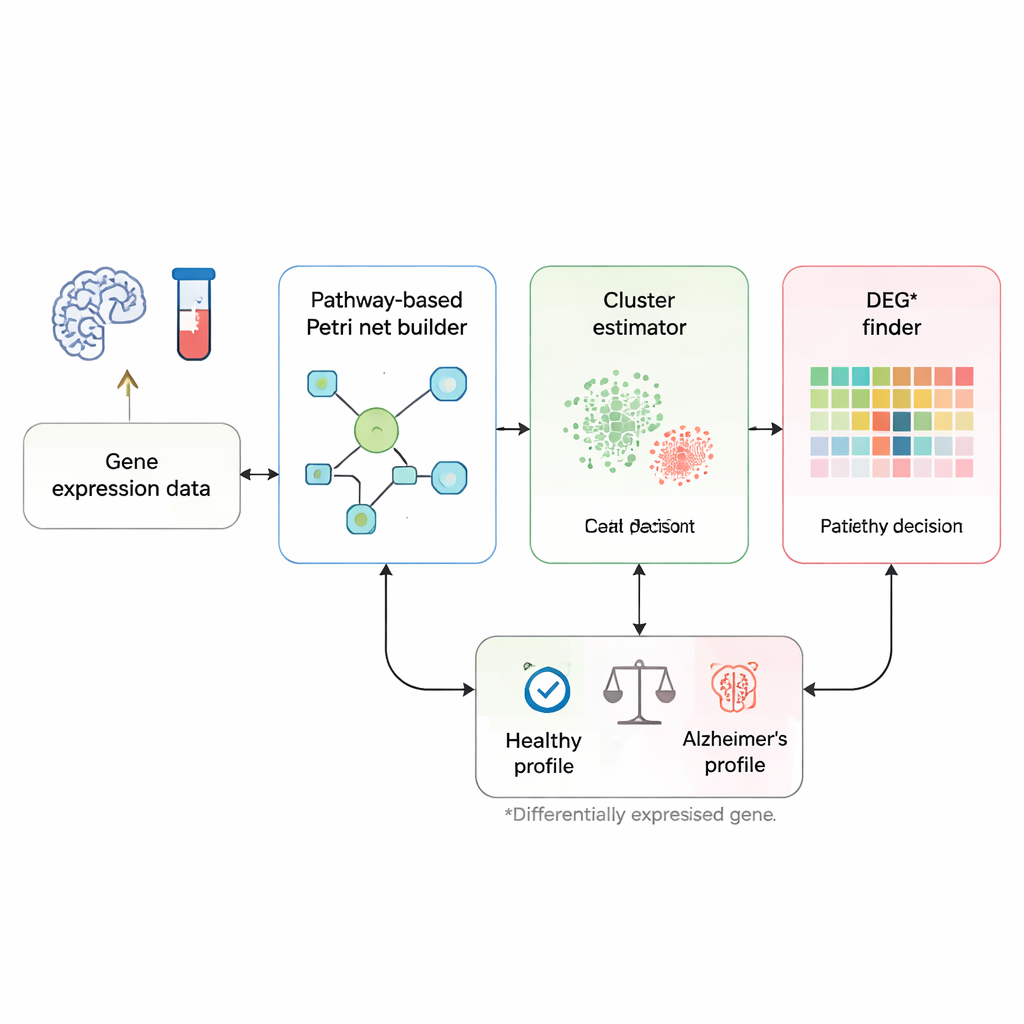
I stället för att betrakta varje gen som en isolerad markör fokuserar forskarna på hur gener kommunicerar med varandra längs kända biologiska signalvägar kopplade till Alzheimers sjukdom. De börjar med en kuraterad vägkarta från KEGG-databasen, som listar gener och de aktiverande eller hämmande relationerna mellan dem. Denna väg omvandlas till ett Petri-nät—en sorts flödesschema där cirklar står för gener, rektanglar för interaktioner och små token för signaler som rör sig genom nätverket. När en token färdas från ena änden av vägen till särskilda ”sjukdoms”-noder representerar det en kedja av gengenomförda händelser som kan leda till neurons död och demens.
Från ett blodprov till ett ja-eller-nej-svar
Metoden börjar med genuttrycksprofiler: mätningar som visar hur aktiva tusentals gener är i en persons blod eller hjärnvävnad. Först jämför en specialanpassad ”klusteruppskattare” ett nytt prov med tidigare märkta friska och patientprover, med fokus på gener som redan är kända för att skilja mellan dessa grupper. För varje sådan gen identifierar verktyget vilka träningsprover som har mest liknande uttrycksnivåer och använder en form av grannskapsröstning för att ge det nya provet en inledande etikett som sannolikt friskt eller sannolikt sjukt. Detta steg bildar två arbetsgrupper, eller kluster, av prover: ett som representerar typiska friska mönster och ett som representerar typiska Alzheimers-mönster.
Hitta de mest talande generna för varje person
Därefter följer ett mer personligt steg. För en given person undersöker metoden gen för gen för att se var deras uttrycksnivåer verkligen sticker ut. För varje gen jämförs personens värde med intervallet som ses i både det friska klustret och patientklustret, med robusta statistiska mått som nedtonar inflytandet från brusiga avvikare. Om en gens uttryck klart ligger inom det ”sjuka” intervallet och utanför det friska intervallet flaggas den som en DEG*—en särskilt informativ gen för den individen. Dessa DEG*-gener får initiala token i Petri-nätet, vilket markerar var onormal aktivitet först uppträder i signaleringskretsen.
Låta nätverket spela ut till en diagnos
När token har placerats körs Petri-nätet stegvis. Vid varje steg ”avfyrar” varje interaktion vars inmatande gener har tillräckligt många token, vilket flyttar token till nedströms gener samtidigt som aktiverings- och inhibitionsregler respekteras. Detta fortgår tills inga fler rörelser är möjliga. Om åtminstone en token når nätverkets slutliga sjukdomsnod—som representerar processer som neurons död eller neurodegeneration—klassificeras provet som Alzheimers; annars etiketteras det som friskt. Eftersom varje avfyrningssteg registreras kan forskarna spåra en tydlig väg från en persons ovanliga genaktivitet hela vägen till ett friskt eller sjukt utfall, i stället för att förlita sig på en ogenomskinlig statistisk poäng.
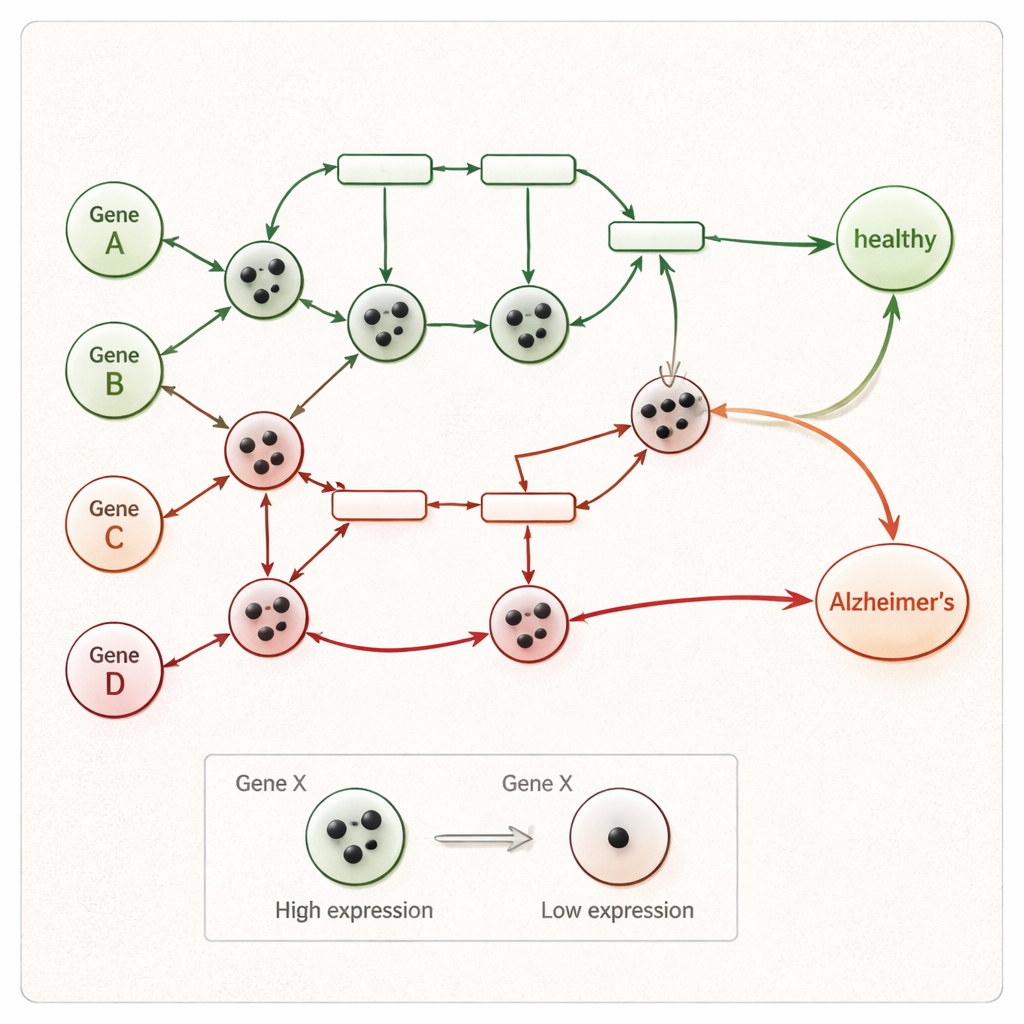
Hur exakt är detta tillvägagångssätt i praktiken?
Teamet testade sitt ramverk på flera stora, offentliga genuttrycksdatamängder från både blod och hjärnvävnad. På två brett använda bloddatamängder skilde deras metod korrekt Alzheimerspatienter från friska individer i cirka 98–99 % av fallen, långt över tidigare maskininlärningsmetoder som ofta nådde endast 65–81 % noggrannhet. De visade också god prestanda över ytterligare hjärn- och bloddatamängder, även när antalet prover var litet. Viktigt är att, till skillnad från många konkurrenter, deras metod inte slängde bort brusiga eller svårtolkade prover; i stället använder den sin interna design för att hantera variation samtidigt som all data behålls i analysen.
Vad detta betyder för framtida Alzheimers-tester
För en lekmannapublik är huvudbudskapet att studien omvandlar komplex genetik och vägdiagram till en klar, stegvis beslutsprocess som kan läsa tidiga tecken på Alzheimers sjukdom från ett enkelt prov, potentiellt bara blod. Genom att modellera hur avvikande gener fungerar tillsammans, inte bara hur de uppträder ensamma, ger Petri-nätsramverket både hög diagnostisk noggrannhet och en begriplig ”berättelse” om hur sjukdomen kan utvecklas hos varje person. Även om detta arbete fortfarande är forskning och ännu inte ett kliniskt test, pekar det mot framtida verktyg som skulle kunna upptäcka Alzheimers tidigare, vägleda behandlingsval och så småningom anpassas till andra hjärnsjukdomar och cancer med samma grundidé.
Citering: Ebrahimian, H., Asadzadeh, F., Rahgozar, M. et al. Diagnosis of Alzheimer’s disease with high accuracy via Petri net modeling of signaling pathways. Sci Rep 16, 6457 (2026). https://doi.org/10.1038/s41598-026-36585-0
Nyckelord: Diagnos av Alzheimers, genuttryck, signalvägar, Petri-nätsmodellering, blodbaserade biomarkörer