Clear Sky Science · sv
Tumörmikromiljön vid esofaguscancer och dess samband med kliniska egenskaper och svar på neoadjuvant behandling
Varför tumörens omgivning spelar roll
Esofaguscancer är en av de dödligaste cancerformerna globalt, och även med modern cytostatika och strålning svarar många patienter inte så bra som man hoppats. Denna studie ställer en förenklat utseende fråga med stora konsekvenser: vad händer i ”grannskapet” runt tumören—tumörmikromiljön—och kan dess sammansättning hjälpa till att förklara varför vissa patienter svarar på behandling medan andra inte gör det? Genom att noggrant studera immunceller och relaterade markörer före och efter behandling börjar forskarna kartlägga hur kroppen och tumören interagerar, och hur denna dolda dialog kan vägleda framtida, mer personligt anpassade behandlingar.
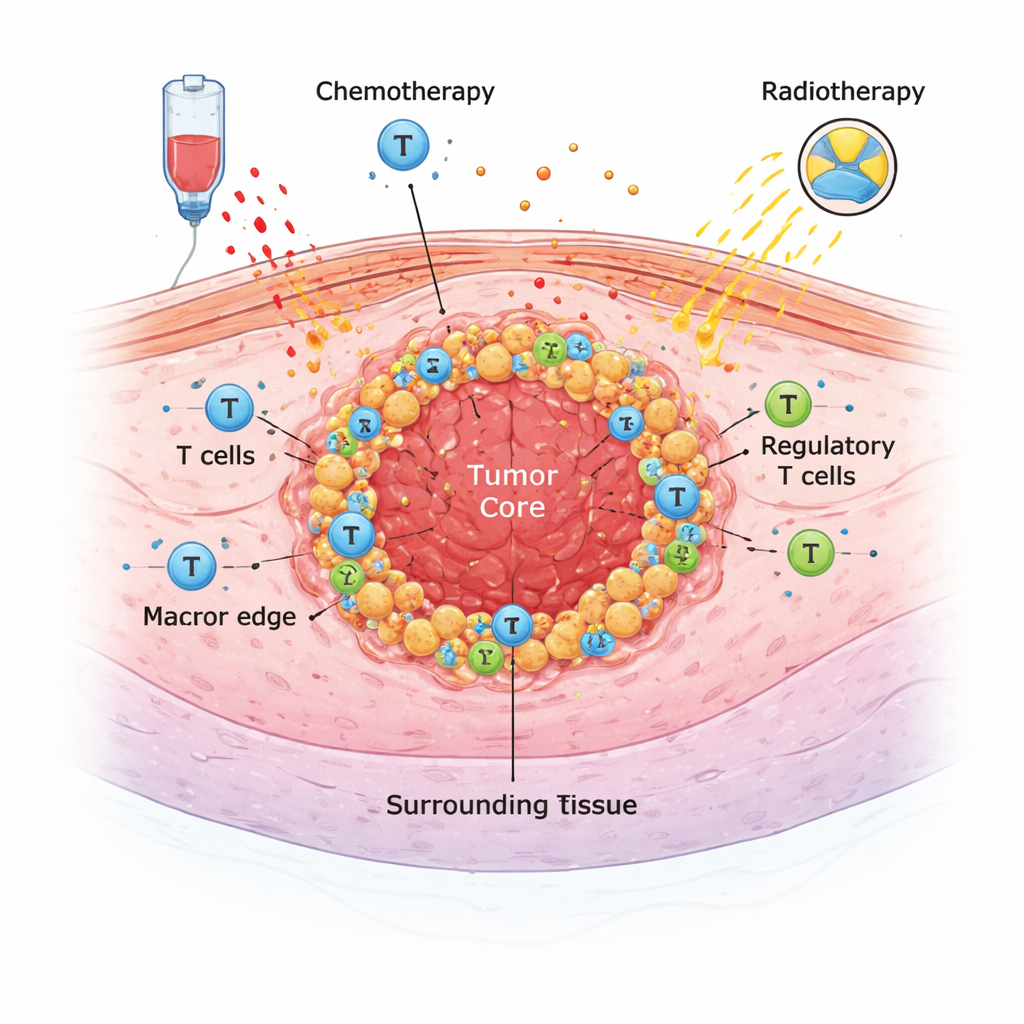
Den dolda ekosystemet kring en tumör
Solida tumörer växer inte isolerat. De finns i ett komplext ekosystem av immunceller, stödceller och signalmolekyler som kallas tumörmikromiljön. I denna studie granskade läkare och patologer i Lausanne tumörprover från 68 patienter som opererades för esofaguscancer mellan 2009 och 2021. De flesta hade fått kraftfull behandling före operation—antingen cytostatika, kemoradioterapi eller båda—för att krympa tumören. Med hjälp av särskilda färgningar på vävnadssnitt räknade teamet flera viktiga immuncellstyper (inklusive generella T‑celler, cytotoxiska T‑celler och olika typer av makrofager) och mätte markörer som kan förutsäga svar på immunterapi, såsom PD‑L1 och HER2.
Vilka patienterna var och vad som mättes
Patienterna i denna serie var främst män i tidig sextioårsålder, och majoriteten hade adenocarcinom, den typ av esofaguscancer som ofta kopplas till långvarig reflux och Barretts esofagus. En mindre grupp hade skivepitelcancer, en annan form som uppstår från de platta slemhinnecellerna i matstrupen. Forskarna kopplade noggrant mikroskopiska fynd till kliniska detaljer som sjukdomsstadium, rökvanor, viktnedgång och vilken typ av förbehandling som givits före operation. De följde också hur fullständigt varje tumör svarade på terapin, med ett graderingssystem som skiljer komplett försvinnande av cancerceller från litet eller inget svar.
Livsstil, tumörtyp och ett dämpat immunsvar
Flera vardags- och sjukdomsrelaterade faktorer visade sig vara förknippade med en svagare immunnärvaro runt tumören. Patienter som var aktiva rökare hade färre makrofager totalt och färre så kallade M2‑lika makrofager, som ofta kopplas till tumörstöd och immunsuppression. Personer med mer avancerade tumörer, större preoperativ viktnedgång eller skivepitelcancer tenderade att ha färre T‑celler och makrofager infiltrerande sina tumörer. I kontrast var tumörer med höga PD‑L1‑värden—en indikator som ofta används för att välja patienter för immunterapi—"hetare", med fler T‑celler och makrofager, men detta mönster har tidigare kopplats till sämre utfall, sannolikt eftersom tumören aktivt använder PD‑L1 för att slå av immunsvaret.
Hur behandling formar tumörens omgivning
Neoadjuvant (före operation) behandling omformade i hög grad tumörmikromiljön. Både cytostatika och kemoradioterapi ökade antalet makrofager, inklusive M2‑lika celler, samtidigt som de kraftigt reducerade de regulatoriska T‑cellerna, en grupp som normalt dämpar immunsvar. Totala antalet T‑celler och cytotoxiska T‑celler förändrades mindre konsekvent. Intressant nog tenderade kemoradioterapi att sänka PD‑L1‑nivåerna på tumörceller och omgivande celler, vilket minskade andelen patienter med höga PD‑L1‑värden efter behandling. Det tyder på att standardbehandling kan få tumörer att se mindre lämpliga ut för PD‑1/PD‑L1‑blockerande immunterapier om man endast bedömer ett enstaka prov efter kemoradioterapi.
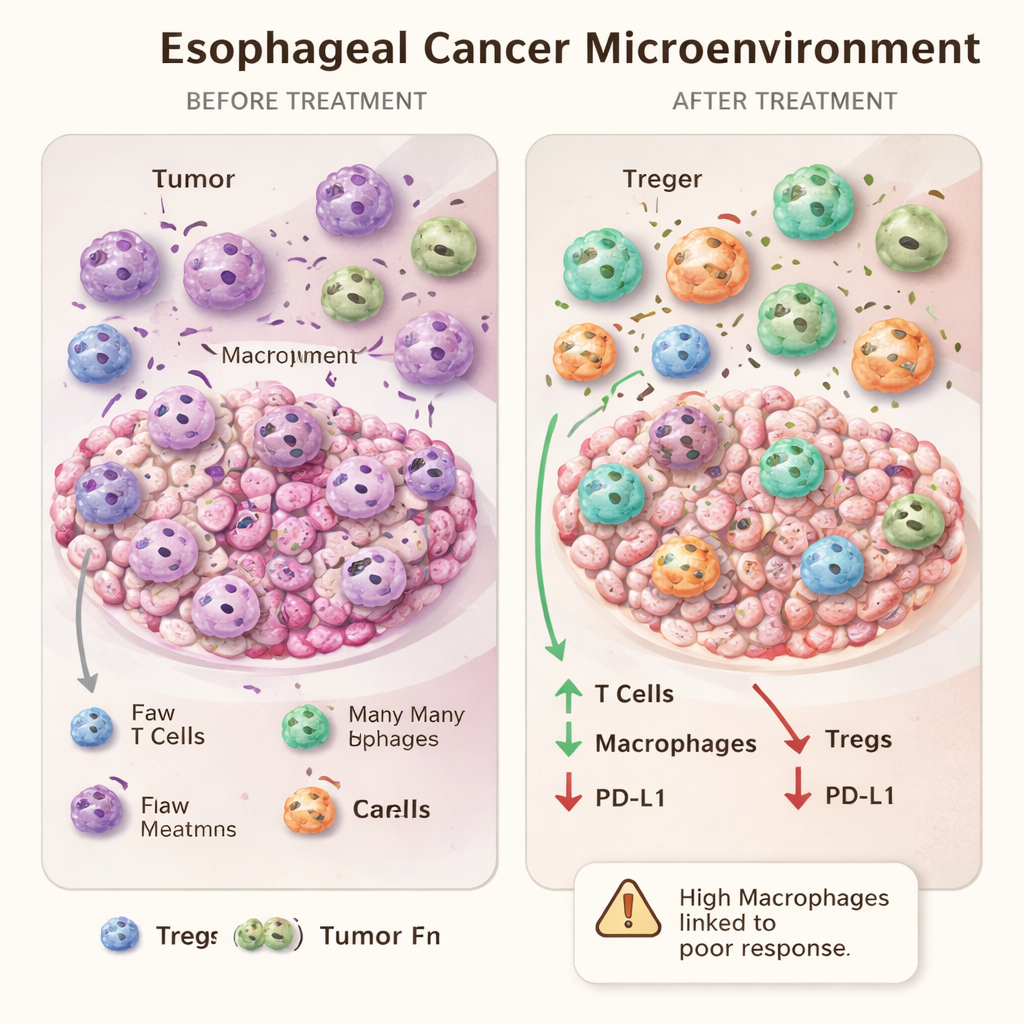
När fler immunceller kan signalera resistens
Ett av de mest intressanta fynden kom från jämförelser av behandlingens ytterligheter. Patienter vars tumörer helt försvann under mikroskopet skilde sig inte vid baslinjen från dåliga respondenter vad gäller immuncellernas närvaro runt cancern. Däremot hade de med dåliga svar efter behandling fler makrofager i tumörområdena än de som svarade fullständigt. Istället för att vara ett enkelt tecken på ett starkt immunsvar kan en överväxt av makrofager efter terapi snarare markera ett uttorkat eller snedvridet svar som tumören lärt sig utnyttja. Detta stärker idén att vissa makrofager, särskilt M2‑lika typer, faktiskt kan främja tumöröverlevnad och resistens.
Vad detta betyder för framtida vård
För patienter och kliniker är huvudbudskapet att biologin runt en esofagustumör—dess mikromiljö—formas av rökning, tumörtyp, sjukdomsgrad och av behandlingarna själva. Standard kemoterapi och kemoradioterapi krymper inte bara tumörer; de rekryterar och omformar också immunceller på sätt som kan hjälpa eller hämma långsiktig kontroll av sjukdomen. Studien antyder att räkna vissa immunceller, särskilt makrofager, före och efter behandling en dag skulle kunna hjälpa till att identifiera vem som sannolikt utvecklar resistens och vem som kan ha nytta av tilläggsbehandlingar som riktar sig mot dessa celler eller PD‑1/PD‑L1‑vägen. Även om fler, större studier behövs, för oss detta arbete närmare en anpassning av esofaguscancerbehandling inte bara efter tumörens genetik utan också efter det dynamiska ekosystem som omger den.
Citering: Fasquelle, F., Teixeira Farinha, H., Sempoux, C. et al. The tumor microenvironment in esophageal cancer and its association with clinical features and neoadjuvant treatment response. Sci Rep 16, 5664 (2026). https://doi.org/10.1038/s41598-026-36537-8
Nyckelord: esofaguscancer, tumörmikromiljö, immunceller, kemoradioterapi, immunterapi