Clear Sky Science · sv
Värd-m6A-modifikationer formar mikrobiotan som driver cellspecifik ferroptos som en kausal väg till kroniska lungsjukdomar
Varför dina mikrober spelar roll för dina lungor
Kroniska andningsproblem som astma och kroniskt obstruktiv lungsjukdom (KOL) brukar ofta skyllas på rökning, föroreningar eller allergier. Denna studie pekar på en annan, mindre uppenbar aktör: de biljoner mikrober som lever i vår tarm och på vår hud. Med storskaliga genetiska data visar författarna att vissa mikrober kanske inte bara följer med lungsjukdom, utan bidrar till att orsaka den — genom subtila kemiska förändringar i våra celler och en form av järnberoende celldöd. Att förstå detta dolda nätverk kan så småningom leda till nya sätt att förebygga eller behandla kroniska luftvägssjukdomar genom att styra våra mikrober och deras molekylära vägar i hälsosammare riktningar.
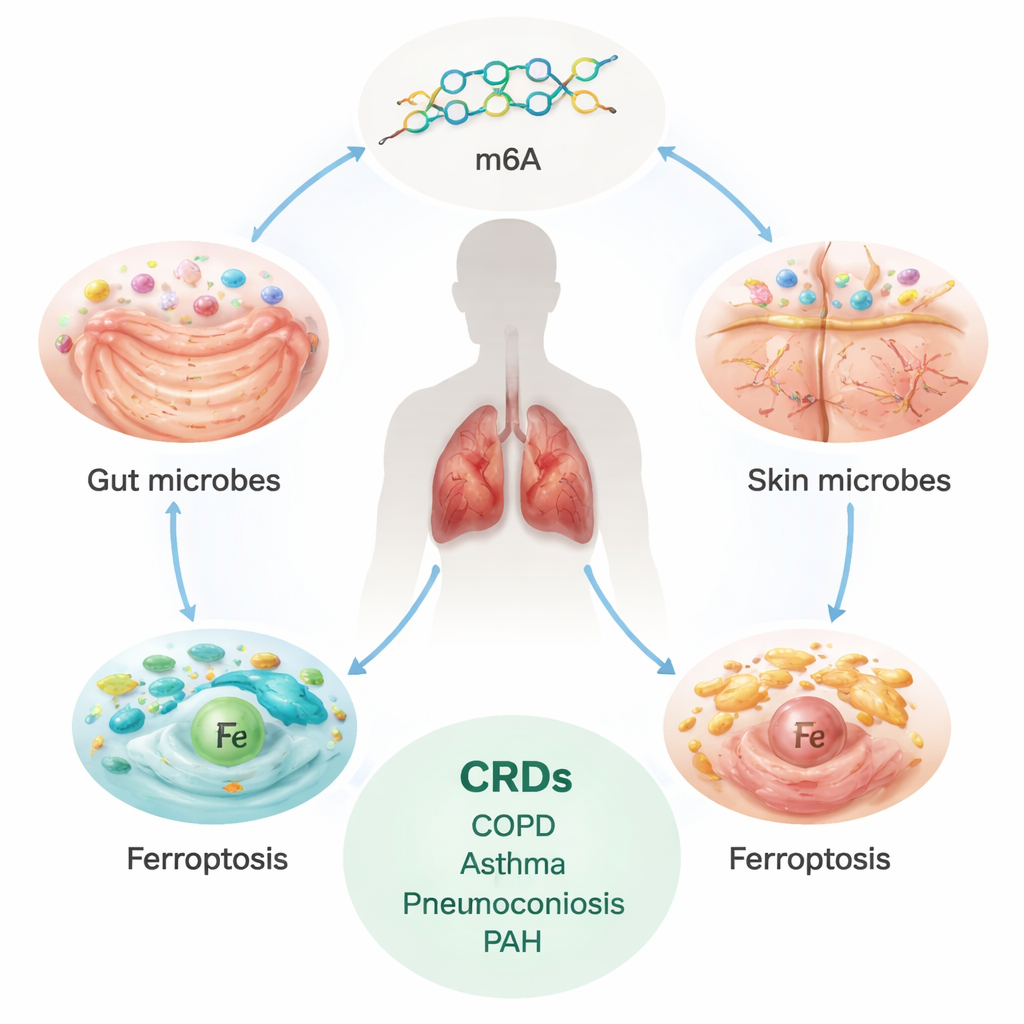
Den dolda bördan av kroniska lungsjukdomar
Kroniska luftvägssjukdomar, inklusive KOL, astma, interstitiell lungsjukdom (ILD), pneumokonios och pulmonell arteriell hypertension (PAH), drabbar hundratals miljoner människor världen över och orsakar miljontals dödsfall varje år. Dessa tillstånd utvecklas ofta långsamt men obevekligt, ärrbildar eller omstrukturerar lungor och blodkärl och leder till andfåddhet. Nuvarande behandlingar hanterar i huvudsak symtom; de stoppar inte fullt ut och vänder inte alltid den underliggande skadan. Det har fått forskare att söka efter djupare, grundläggande orsaker, särskilt sådana som kan modifieras innan svår sjukdom uppstår.
Mikrobiella grannar i tarm och hud
Vi vet nu att tarm och hud hyser komplexa mikrobgemenskaper som hjälper till att träna immunsystemet, forma ämnesomsättningen och upprätthålla barriärförsvar. Men driver dessa mikrober faktiskt lungsjukdom, eller förändras de bara när människor blir sjuka? För att reda ut orsak och verkan använde forskarna en metod som kallas Mendelsk randomisering, som utnyttjar naturliga genetiska skillnader mellan människor som ett slags livslångt ”experiment”. De kombinerade genetiska data om hundratals tarm- och hudmikrober med data om fem stora kroniska lungsjukdomar från stora europeiska studier och testade om ärftliga benägenheter för högre eller lägre nivåer av specifika mikrober är kopplade till risken för varje sjukdom.
Mikrober som hjälper eller skadar lungorna
Analysen identifierade dussintals tarmmikrober som antingen ökade eller minskade risken för respektive luftvägssjukdom, ofta i sjukdomsspecifika mönster. Till exempel verkade vissa tarmbakterier skydda mot KOL, astma eller PAH, medan andra ökade sannolikheten för ILD eller KOL. Hudmikrober visade mer blygsamma men ändå påtagliga samband, med vissa arter kopplade till högre risk och andra till lägre risk för olika tillstånd. Teamet vände också analysens riktning och fann att genetisk risk för KOL, astma och andra lungsjukdomar i sin tur förutsade förändringar i både tarm- och hudmikrobiota. Denna tvåvägs trafik tyder på en återkopplingsslinga: mikrober kan bidra till att forma lungsjukdom, och lungsjukdom kan omforma våra mikroböcosystem.
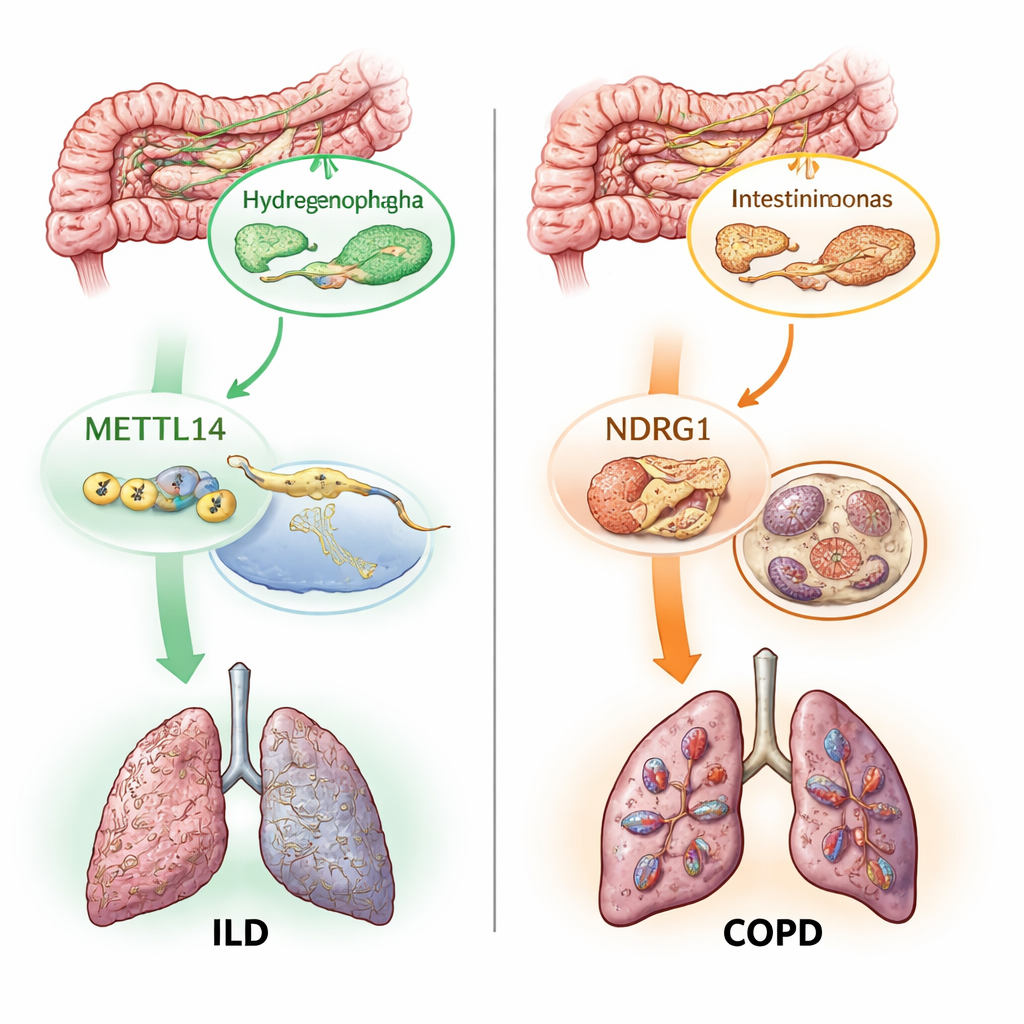
Två molekylära brytare: RNA-markeringar och järndriven celldöd
Utöver att kartlägga vilka mikrober som spelar roll undersökte författarna hur dessa mikroskopiska partner kan påverka lungvävnader. De fokuserade på två molekylära processer som redan misstänks vara inblandade i lungskada. Den första, kallad m6A-modifikation, är en liten kemisk märkning som läggs på RNA och som finjusterar hur gener slås på och av. Den andra, ferroptos, är en form av järnberoende celldöd driven av okontrollerad oxidation av fetter i cellmembran. Med genetiska proxyer för 19 m6A-relaterade gener och hundratals ferroptos-relaterade gener testade de om förändringar i dessa vägar orsakar lungsjukdom. De fann att ett m6A-skrivargene, METTL14, kopplades till lägre risk för ILD, och flera ferroptos-gener, inklusive NDRG1, kopplades till högre risk för KOL, ILD och astma.
Att koppla ihop prickarna: från mikrober till celler till sjukdom
Det mest nyskapande i arbetet var att spåra hur dessa delar passar in i orsaks- och verkningskedjor. Statistiska medlingsanalyser föreslog att en del av METTL14:s skyddande effekt mot ILD går via förändringar den framkallar i en särskild tarmmikrob kallad Hydrogenophaga. I en annan bana verkade en viss tarmbakterie, Intestinimonas massiliensis, påverka KOL-risk delvis genom att aktivera NDRG1 och ferroptos-programmet. Forskarna kontrollerade sedan data från mänsklig lungvävnad och bekräftade att både METTL14 och NDRG1 uttrycks annorlunda i sjuka jämfört med friska prover. Slutligen pekade de med hjälp av encellsgenetiska kartor över immunceller ut NDRG1:s skadliga effekt på KOL till en specifik immuncellsdelmängd, en sorts monocyt, vilket tyder på att framtida läkemedel som riktar sig mot detta gen kan behöva verka på cellnivå.
Vad detta betyder för framtida behandlingar
För icke-specialister är huvudbudskapet att lungornas hälsa inte bara handlar om vad vi andas in utan också om de mikrober som lever i och på oss och vilka molekylära brytare de aktiverar i våra celler. Denna studie kan inte experimentellt bevisa varje steg, och den är främst begränsad till personer av europeiskt ursprung, men den erbjuder starka genetiska ledtrådar om att tarmmikrober, RNA-markeringar som m6A och järndriven celldöd utgör en sammanhängande väg som leder till kronisk lungsjukdom. På lång sikt kan denna forskningslinje inspirera nya strategier som kombinerar mikrobiom-baserade terapier med läkemedel som riktar METTL14, NDRG1 eller ferroptos, med målet att inte bara lindra symtom utan att bryta de biologiska kretsar som driver kroniska luftvägssjukdomars progression.
Citering: Zhang, J., Liu, X., Liu, X. et al. Host m6A modifications shape microbiota that drives cell specific ferroptosis as a causal pathway to chronic respiratory diseases. Sci Rep 16, 5809 (2026). https://doi.org/10.1038/s41598-026-36513-2
Nyckelord: tarmmikrobiom, kronisk lungsjukdom, astma och KOL, RNA-epigenetik, cellers dödssätt