Clear Sky Science · sv
NEK7-fosforylering av cortactin påverkar migratorisk förmåga hos celler som uttrycker EML4-ALK V3
Varför cellrörelse är viktig vid lungcancer
Cancer blir livshotande när celler lär sig att förflytta sig. Vid icke-småcellig lungcancer sprider sig vissa tumörer genom kroppen snabbare än andra, och en bidragande orsak är ett felaktigt fusionsprotein kallat EML4-ALK. En särskild version, känd som variant 3 (V3), kopplas till särskilt aggressiv sjukdom och dåliga svar på riktade läkemedel. Denna studie ställer en enkel men viktig fråga: vad tillåter dessa V3-drivna cancerceller att ändra form och röra sig så effektivt, och kan vi identifiera de molekylära delarna som gör detta möjligt?
En hypermigratorisk lungcancervariant
Läkare har länge känt till att endast en minoritet av lungcancerfallen bär på EML4-ALK-fusionen, men patienter vars tumörer uttrycker V3-formen har ofta sämre prognos än de med andra varianter. Under mikroskop ser V3-uttryckande celler annorlunda ut: istället för att vara kompakta och kakelstenslika sträcker de ut sig i långa, tunna former med utdragna utskott, som celler i rörelse. Tidigare arbete visade att detta beteende beror på två enzymer, NEK9 och NEK7, som fungerar som molekylära strömbrytare i celler. De avgörande nedströmsmålen för dessa strömbrytare — de som direkt formar cellens inre skelett — var dock inte väl förstådda.
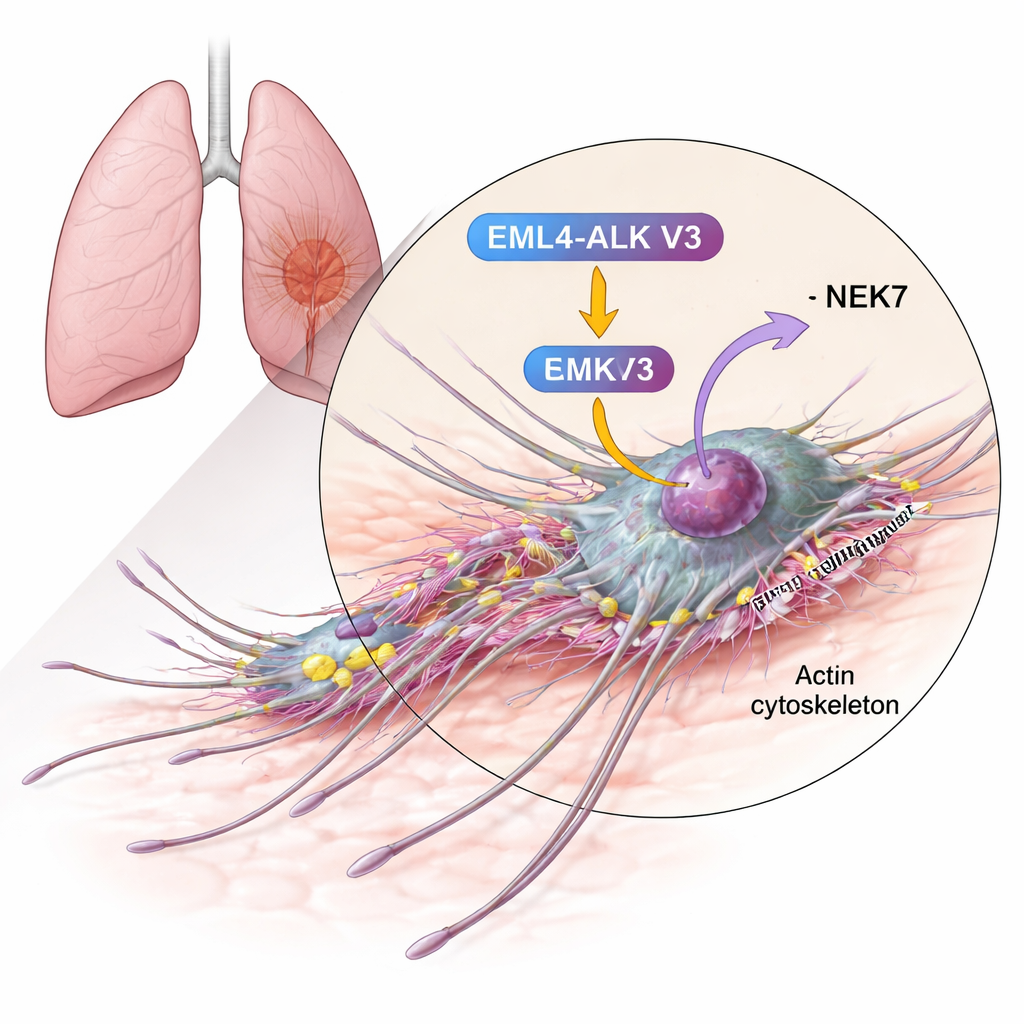
Kopplar ett rörelseprotein till en aggressiv fusion
Författarna fokuserade på cortactin, ett protein som redan är känt för att vara rikt förekommande i många invasiva cancerformer och som hjälper till att bygga de aktinnätverk som driver cellmembranet framåt. Med biokemiska tester visade de att cortactin kan modifieras kemiskt (fosforyleras) av NEK6 och, ännu mer uttalat, av NEK7. Enzymerna lägger fosfatgrupper på specifika serinrester inom cortactins aktinbindande region — just det segment som griper tag i aktinfibrer och stabiliserar grenade nätverk. När NEK7 var närvarande dekorerades cortactin med fler fosfatgrupper och på fler platser än med NEK6, vilket tyder på att NEK7 är huvudregulatorn i detta sammanhang.
Att stänga av cortactin bromsar cancercellmigration
För att se vad cortactin faktiskt gör i levande celler utarmade forskarna det med RNA-interferens i celler konstruerade för att aktivera NEK9 eller NEK7, eller för att uttrycka EML4-ALK V3 självt. I alla tre fallen kollapsade de utpräglade förlängda, mesenkymala formerna: cellerna blev plattare och rundare, förlorade sina långa utskott och bildade istället tjocka, raka aktin "stressfibrer" som korsade cellen. Flera migrationsanalyser — från att sluta artificiella "sår" i ett cellskikt till att spåra enskilda celler och mäta rörelse mot en kemisk signal — visade att utan cortactin saktade dessa högmotila celler ner dramatiskt. Liknande effekter sågs i etablerade lungcancercellinjer som naturligt bär EML4-ALK V3, vilket understryker banans kliniska relevans.
Fina filament och vassa spetsar i framkanten
Högupplöst avbildning i bronkiala epitelceller avslöjade en ännu mer detaljerad bild. Celler som uttryckte EML4-ALK V3 producerade många fina, ibland grenade, filopodia-liknande utskott som prydde deras framskjutningar. Vid spetsarna och vid förgreningspunkterna av dessa strukturer samlades cortactin, EML4-ALK V3, NEK7 och en fosforylerad form av cortactin tillsammans. Denna täta samexistens tyder på en fokuserad "byggarbetsplats" där NEK7 modifierar cortactin för att bygga och underhålla de känsliga, grenade aktinnäten som hjälper till att styra cellen. När cortactin togs bort försvann dessa invecklade utskott och invasiv tillväxt från 3D-tumörliknande sfäroider in i en omgivande gel minskade kraftigt.
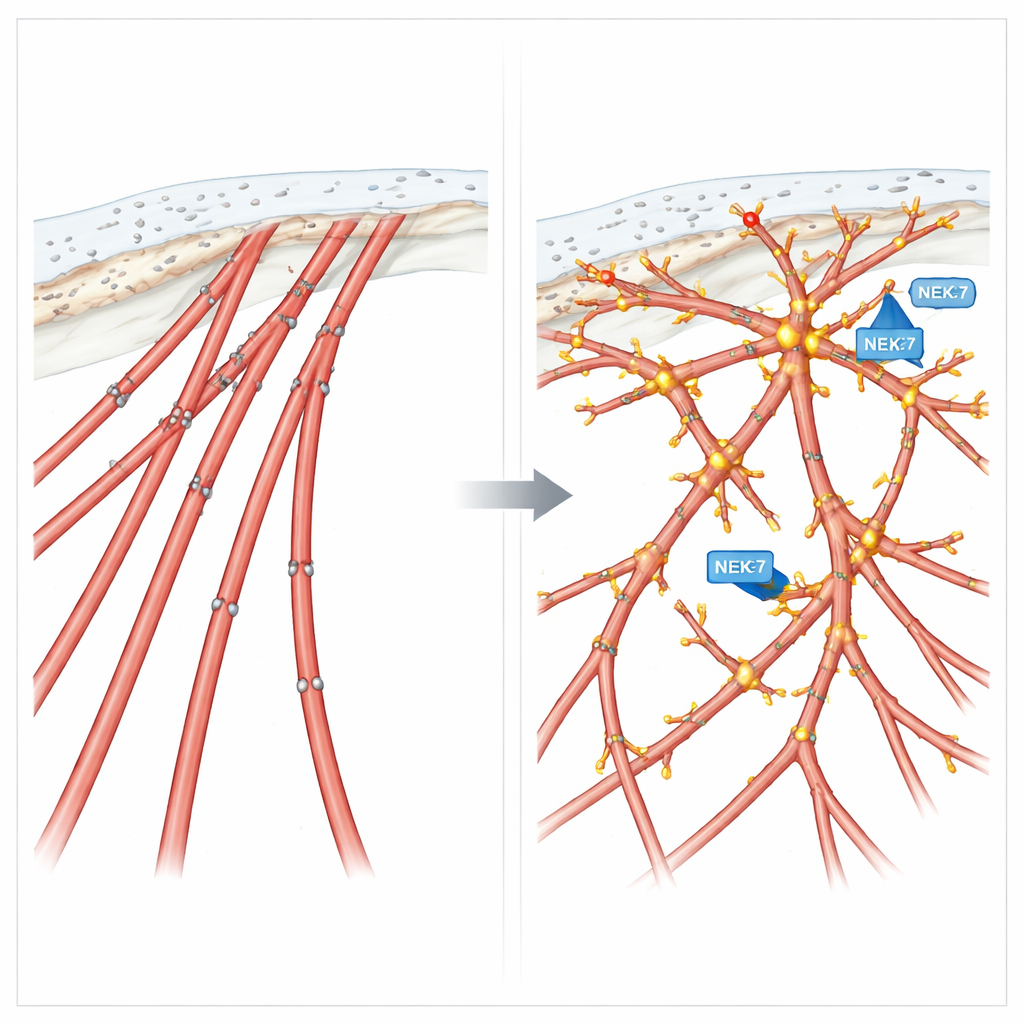
Fosforylering som en migrationsregulator
För att testa hur dessa kemiska märken på cortactin påverkar beteendet skapade teamet två designerformer av proteinet: en fosfo-mimetisk form som imiterar konstant fosforylering vid fyra nyckelplatser, och en fosfo-null form som inte kan fosforyleras där. Celler som uttryckte den mimetiska versionen utvecklade rikliga filopodia-liknande utskott och visade förbättrad riktad migration, liknande celler med aktiv NEK7 eller EML4-ALK V3. I kontrast bildade celler som uttryckte den icke-fosforylerbara versionen stela stressfibrer, förlorade dessa fina utskott och rörde sig snabbt men utan mål — bra på att vandra, dåliga på att följa en signal. I tredimensionella kulturer drev denna fosfo-null cortactin invasiva utväxter som var oorganiserade snarare än precist styrda.
Vad detta innebär för att förstå — och rikta in sig på — spridning
Enkelt uttryckt visar studien att den aggressiva EML4-ALK V3-lungcancervarianten kaprar ett normalt system för cellformning. Genom att aktivera NEK7 orsakar den att cortactin fosforyleras vid specifika platser inom dess aktinbindande region. Denna modifiering stämmer av cortactin så att det kan bygga fint grenade aktinstrukturer och filopodia-liknande utskott som stödjer snabb, riktad cellmigration och invasion. Att störa cortactin eller dess fosforylering vänder systemet: cellerna rör sig antingen knappt eller rör sig kaotiskt utan riktning. Dessa insikter blottlägger en konkret molekylär kedja — från en cancerdrivande fusion, via NEK7, till cortactin och aktin-cytoskelettet — som hjälper till att förklara varför vissa lungcancerformer metastaserar så effektivt, och pekar mot nya sätt att sakta ner eller vilseleda deras rörelse.
Citering: Richardson, E.L., Knebel, A., Straatman, K.R. et al. NEK7 phosphorylation of cortactin modulates the migratory capacity of cells expressing EML4-ALK V3. Sci Rep 16, 6407 (2026). https://doi.org/10.1038/s41598-026-36484-4
Nyckelord: icke-småcellig lungcancer, EML4-ALK V3, cellmigration, cortactin, aktin-cytoskelett