Clear Sky Science · sv
En integrativ metod för att identifiera nya miRNA–mRNA-interaktionsnätverk i LMNA-kardiomyopati
Varför små hjärtreulatorer spelar roll
Dilaterad kardiomyopati är ett allvarligt tillstånd där hjärtat blir förstorad och försvagad, vilket ofta leder till hjärtsvikt, farliga rytmstörningar och i vissa fall plötslig död. För många familjer är sjukdomen ärftlig, och förändringar i en gen som kallas LMNA är en vanlig orsak. Denna studie ställer en till synes enkel fråga med stora konsekvenser: i hjärtan skadade av LMNA-mutationer, vilka gener slås på eller av, och vilka små RNA-molekyler drar i de spakarna? Genom att kartlägga dessa molekylära samtal i detalj pekar arbetet mot nya sätt att förutsäga, övervaka och kanske en dag behandla denna aggressiva form av hjärtsjukdom.
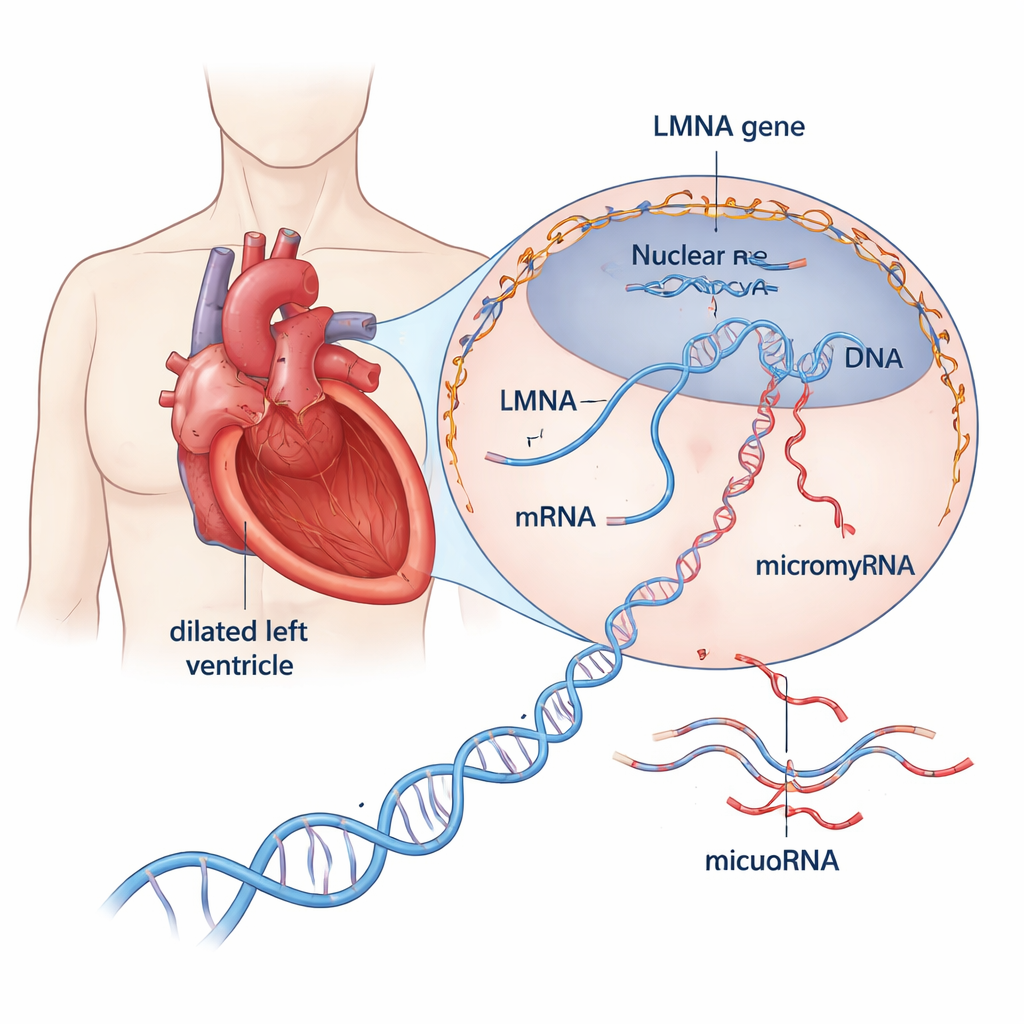
Närmare titt på en farlig hjärtsjukdom
Dilaterad kardiomyopati innebär att hjärtats huvudsakliga pumpkammare sträcks ut och blir tunnare, vilket försvagar dess förmåga att driva runt blodet. Ungefär en tredjedel till hälften av fallen som tidigare kallades ”idiopatiska” visar sig nu ha en genetisk grund. Bland mer än 30 involverade gener sticker LMNA ut: skadliga varianter i denna gen står för cirka 10 % av de ärftliga fallen och kopplas till snabb sjukdomsprogression, tidiga rytmrubbningar och hög risk för plötslig hjärtdöd. LMNA kodar för strukturella proteiner som bildar ett skelett runt cellens DNA, hjälper till att bevara kärnans form och påverkar vilka gener som är aktiva. Ändå har det varit dåligt förstått hur defekta LMNA-proteiner driver hjärtat mot svikt.
Följa budskapen i mössens hjärtan
För att undersöka detta använde forskarna en musmodell som bär på en välkänd LMNA-mutation (R249W) och som utvecklar en form av dilaterad kardiomyopati liknande den mänskliga sjukdomen. Vid 50 veckors ålder—när mössen visar förstorade kammare, nedsatt pumpfunktion och fibrotisk ärrbildning—extraherade teamet hjärtvävnad och undersökte två typer av RNA: budbärar-RNA (mRNA), som bär instruktioner för att skapa proteiner, och mikroRNA (miRNA), korta icke-kodande strängar som finjusterar genaktivitet genom att blockera eller nedbryta specifika mRNA. Med hjälp av högkapacitetssekvensering och strikta statistiska filter identifierade de 2 148 gener vars aktivitet förändrats i mutationsbärande hjärtan och 53 miRNA som antingen ökade eller minskade jämfört med friska möss.
Vad som förändras i sjuka hjärtceller
När forskarna grupperade de förändrade generna i biologiska signalvägar framträdde flera teman. Många av de påverkade generna kopplades till hur hjärtmuskelceller kontraherar, hur de fäster vid varandra och vid sin omgivande stödmatris, hur elektriska signaler färdas genom hjärtat och hur cellerna bearbetar fetter för att skapa energi. Dessa fynd stämmer väl med det kliniska förloppet vid LMNA-relaterad sjukdom: stel, fibrös vävnad; störd elektrisk ledning som gynnar arytmier; och försämrad energibalans. Väganalys med etablerade databaser bekräftade berikning i ombyggnad av extracellulär matrix, spänningsstyrda jonkanaler, synapsliknande kommunikation i hjärtat och fettsyremetabolism—vilket antyder att LMNA-mutationer stör flera sammanlänkade system snarare än ett enda felsteg.
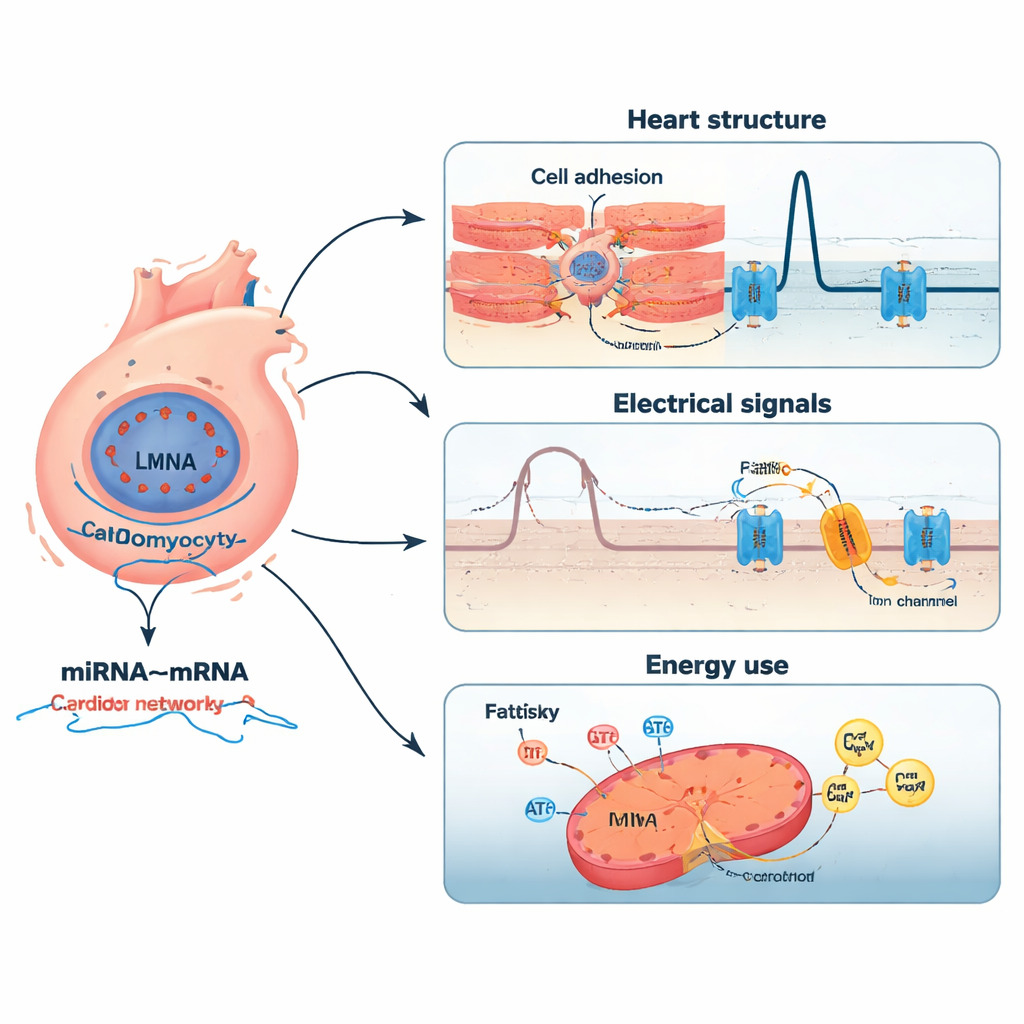
Nätverk av små reglage och deras mål
Studien gick vidare genom att koppla miRNA till deras sannolika mRNA-mål. Med korrelationsanalyser och jämförelser mot stora databaser med experimentellt validerade interaktioner byggde författarna ett nätverk med hög tillförlitlighet bestående av 2 197 miRNA–mRNA-par som involverade 12 nyckel-miRNA. Vissa miRNA var mer aktiva och verkade dämpa gener viktiga för hjärtutveckling, kalciumhantering och svar på oxidativ stress. Andra var mindre aktiva, vilket potentiellt släppte hämningarna på gener involverade i celladhesion, inflammation och omläggning av hjärtats strukturella skelett. Till exempel kopplades ett miRNA (miR-183-5p) till en receptor i Wnt-signalvägen, som påverkar cell-till-cell-kommunikation, medan ett annat (miR-3473a) kopplades till en kalciumfrisättningskanal central för hjärtrytmen. Tillsammans skisserar dessa nätverk hur subtila skift i små RNA-regulatorer kan förstärka effekten av en LMNA-mutation.
Från molekylära kartor till framtida terapier
För icke-specialister är slutsatsen att denna studie erbjuder en detaljerad karta över hur en LMNA-mutation omformar hjärtats interna kopplingar på genregleringsnivå. Istället för en enda ”skadlig gen” speglar sjukdomen ett kaskad av förändrade budskap—många orkestrerade av miRNA—som påverkar hjärtats struktur, elektriska stabilitet och energiutnyttjande. Även om arbetet utförts i möss och till stor del bygger på beräkningsanalys, framhäver det specifika miRNA–gen-par som lovande kandidater för framtida blodbaserade markörer eller riktade terapier. I längden kan finjustering av dessa små RNA-omkopplare hjälpa läkare att bättre förutsäga vem som löper störst risk, övervaka sjukdomsförloppet mer precist och utforma mer personliga behandlingar för familjer som drabbats av LMNA-relaterad kardiomyopati.
Citering: Córdoba-Caballero, J., Martínez, F.B., Campuzano, O. et al. An integrative approach to identify novel miRNA-mRNA interaction networks in LMNA-cardiomyopathy. Sci Rep 16, 6110 (2026). https://doi.org/10.1038/s41598-026-36439-9
Nyckelord: dilaterad kardiomyopati, LMNA-genen, mikroRNA, genreglering, hjärtsvikt