Clear Sky Science · sv
QAL333:s antitumorala aktivitet och prediktiv modellering: integrerad transkriptomisk-bioinformatisk analys avslöjar selektiv cytotoxicitet och bestämningsfaktorer för känslighet
Varför denna nya läkandekandidat är viktig
Cancerläkemedel hjälper ofta vissa patienter men misslyckas för andra, främst eftersom tumörer skiljer sig åt i sin inre koppling. Denna studie presenterar en nyligen utformad förening, QAL333, som verkar slå hårdare mot vissa kolorektala cancerformer än andra samtidigt som många normala celler skonas. Lika viktigt visar forskarna hur mönster av genaktivitet i tumörceller kan hjälpa till att förutsäga vem som sannolikt får nytta, vilket pekar mot mer precisa, personligt anpassade behandlingsstrategier.
En fokuserad attack mot specifika tumörtyper
Teamet inledde med att testa QAL333, en syntetisk molekyl relaterad till en familj föreningar som redan är kända för att skada cancerceller, på en bred panel av 15 humana cancercellinjer och tre icke‑cancerogena linjer. De fann att kolorektala cancerceller, särskilt en cellinje kallad SW620, var mycket känsliga, där läkemedlet dödade dem vid relativt låga doser. I kontrast var trippelnegativa bröstcancerceller betydligt mer resistenta och krävde doser mer än tio gånger högre som var svåra att uppnå säkert. Intressant nog reagerade inte alla icke‑cancerogena celler på samma sätt: vissa var känsliga, medan andra, såsom en allmänt använd njurcellinje, var förvånansvärt resistenta. Detta mönster visade att QAL333:s effekter beror mer på en cells inre biologi än på om den är märkt som ”cancer” eller ”normal”.
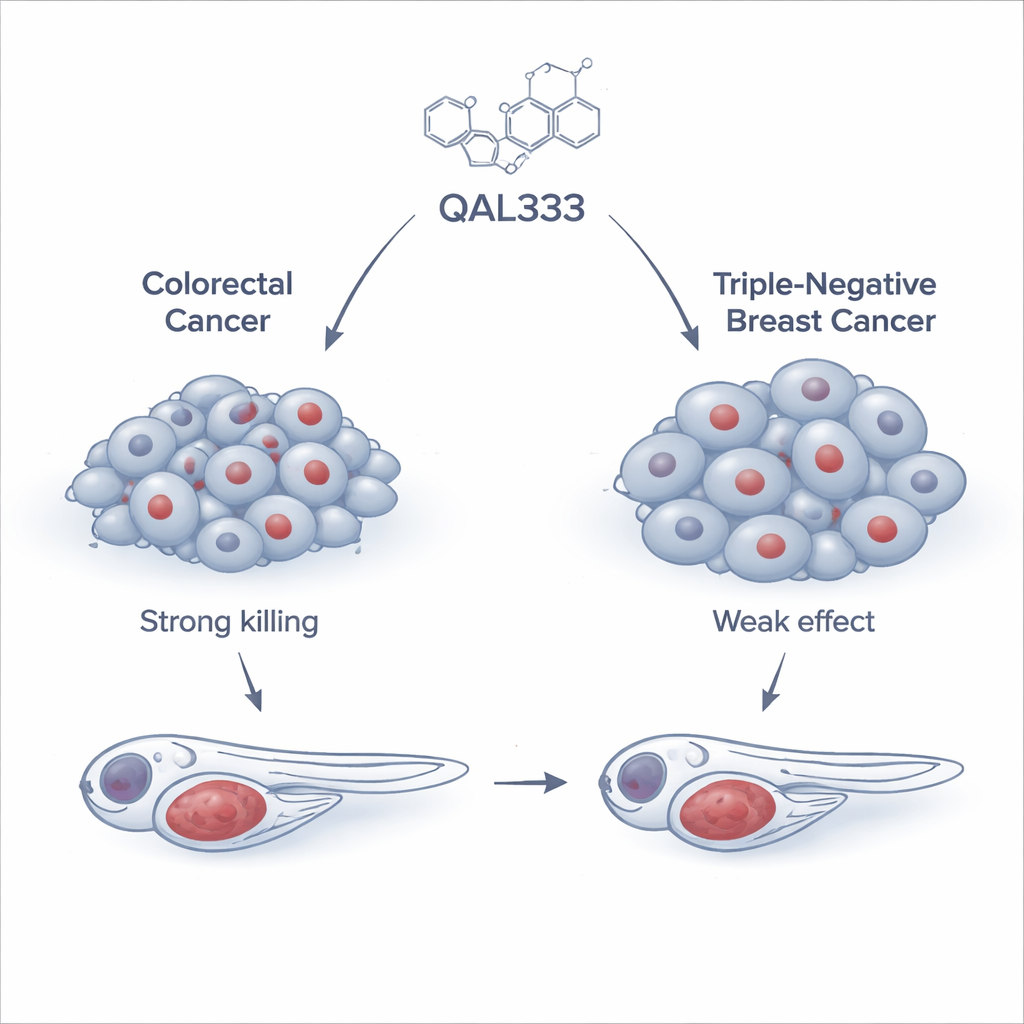
Test av läkemedlet i levande organismer
För att se om de lovande resultaten i cellodling skulle hålla i en levande kropp vände sig forskarna till zebrafisk, en liten genomskinlig fisk som ofta används för att modellera mänsklig sjukdom. De implanterade fluorescerande märkta humana cancerceller i zebrafisksembryon och behandlade dem med QAL333. Hos fisk som bar kolorektala cancerceller bromsade läkemedlet tydligt tumörtillväxten och närmade sig effekten av en standard kombinationskemoterapi som används kliniskt. I kontrast svarade tumörer från de trippelnegativa bröstcancercellerna knappt, även om ett vanligt bröstcancerläkemedel, paklitaxel, fungerade väl i samma modell. Dessa in vivo‑tester stärkte att QAL333:s styrka ligger i en undergrupp av tumörer snarare än i samtliga cancerformer.
Insikt i hur QAL333 verkar inne i cellerna
För att förstå varför vissa celler dör medan andra står emot mätte forskarna hur tusentals gener ändrade sina aktivitetsnivåer efter behandling med QAL333. I känsliga kolorektala cancerceller slog viktiga gener som driver cellens delningscykel och tillväxt ned, och stora överlevnads‑vägar dämpades. Signaler kopplade till oxidativ stress och en form av celldöd som skiljer sig från klassisk programmerad celldöd påverkades också, vilket tyder på att QAL333 överbelastar redan sköra system som hanterar skador i dessa celler. Resistent bröstcancer, däremot, slog på stress‑ och inflammationsprogram som kontrolleras av faktorer som NF‑κB, vilka är kända för att hjälpa celler att uthärda skadliga förhållanden. Denna jämförande bild gav en förståelse av att QAL333 överväldigar svaga försvar i vissa celler medan andra mobiliserar ett effektivt motstånd.
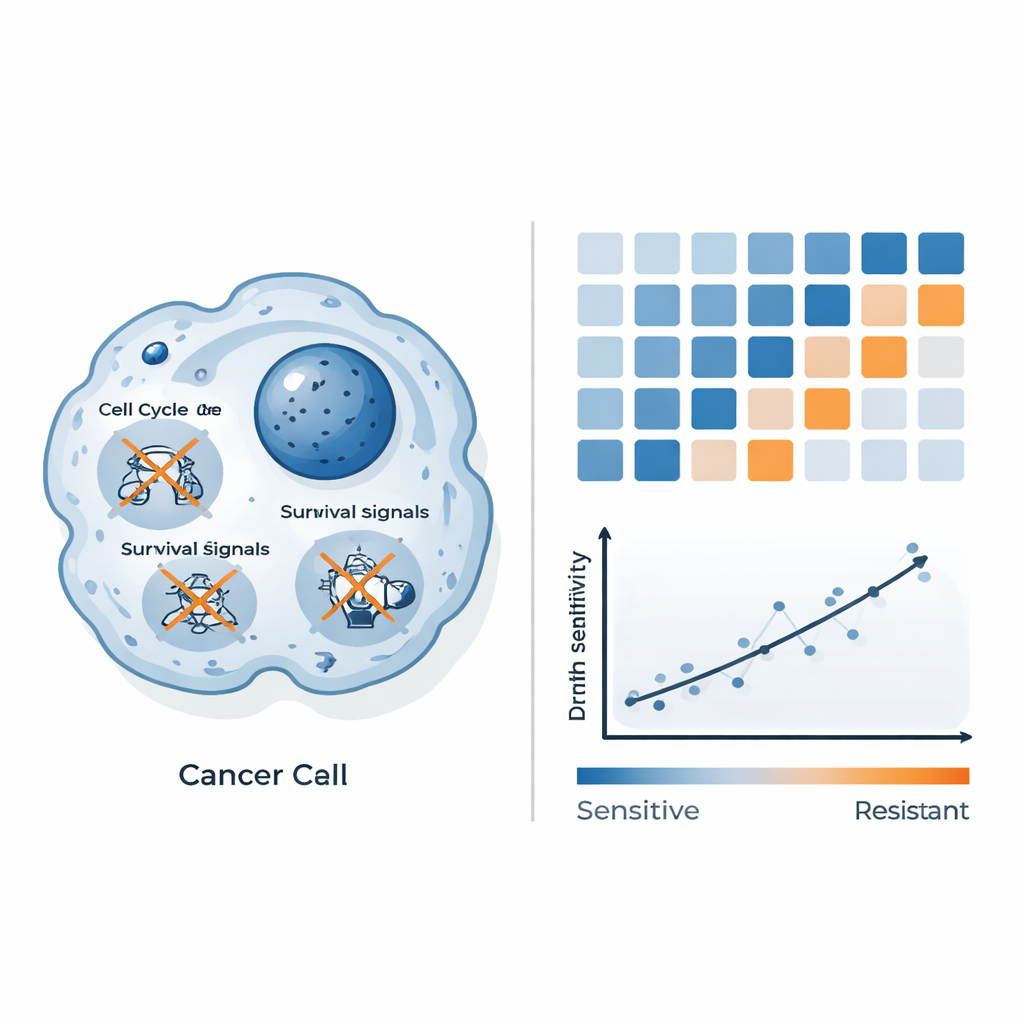
Använda genmönster för att förutsäga vem som svarar
Utöver att katalogisera genförändringar frågade forskarna om dessa mönster kunde omvandlas till ett praktiskt prognosverktyg. De kombinerade baslinje‑genaktivitetsdata från panelen av cellinjer med deras uppmätta läkemedelskänslighet och använde maskininlärning för att söka efter de mest informativa signalerna. Istället för att lita på enskilda gener grupperade de gener i biologiska vägar och skapade en samlad ”vägpoäng” byggd av tre system: hur celler bearbetar energi och kemikalier (metaboliska vägar), hur de organiserar sin omgivning (proteoglykaner och relaterade strukturer i cancer) och hur deras interna skelett är uppbyggt. Denna sammansatta poäng korrelerade starkt med hur mycket QAL333 som krävdes för att döda varje cellinje: lägre poäng förenades med högre känslighet och högre poäng med resistens. Med andra ord kan sättet dessa nätverk är inställda i en tumör förutsäga hur väl QAL333 kommer att fungera.
Oväntade antydningar om bredare biologiska effekter
Medan huvudfokus var cancer visade QAL333 också förmåga att störa ”quorum sensing”, ett kommunikationssystem som bakterier använder för att samordna beteenden som att bilda biofilmer. Vid mycket låga doser minskade föreningen biofilmsbildning av en bakterie kopplad till tandköttssjukdom och dämpade vissa inflammationssignaler i immunceller. Författarna ser detta som tidiga, explorativa fynd, men de antyder att QAL333 eller relaterade molekyler en dag kan ha användningsområden bortom cancerterapi, exempelvis vid infektioner där bakteriesamhällen är svåra att utrota.
Vad detta kan innebära för framtida patienter
Sammantaget positionerar studien QAL333 som en selektiv läkandekandidat som träffar sårbara kolorektala tumörer samtidigt som många andra celltyper skonas, och den kopplar detta till en vägkarta för att förutsäga vilka tumörer som mest sannolikt svarar. Om detta bekräftas i mer avancerade djurmodeller och slutligen hos patienter kan ett enkelt genuttryckstest hjälpa läkare avgöra när QAL333 är en bra match, i linje med det bredare målet att skräddarsy cancerbehandling efter varje tumörs interna koppling. Samtidigt understryker arbetet att även lovande läkemedel har begränsningar: bröstcancer och andra resistenta tumörer kan kräva smarta kombinationer eller helt andra strategier.
Citering: Kim, H.H., Im, S., Kim, J. et al. QAL333’s antitumor activity and predictive modeling: integrated transcriptomic-bioinformatic analysis reveals selective cytotoxicity and sensitivity determinants. Sci Rep 16, 5648 (2026). https://doi.org/10.1038/s41598-026-36430-4
Nyckelord: kolorektal cancer, målinriktad terapi, genuttryck, modellering av läkemedelskänslighet, zebrafisk-xenograft