Clear Sky Science · sv
Från in-silico QSAR‑modellering till in‑vitro MTT‑test: experimentell validering av nya uPAR‑ledare för trippelnegativ bröstcancer (TNBC) och hudcancer
Varför denna forskning är viktig
Cancerformer som trippelnegativ bröstcancer och vissa hudcancerformer är ökända för att vara svåra att behandla eftersom de sprider sig snabbt och ofta motstår standardbehandlingar. Denna studie undersöker ett lovande nytt mål på cancercellernas yta — kallat uPAR — och visar hur en kombination av datorbaserad läkemedelsdesign och laboratorieexperiment kan avslöja nya läkemedelskandidater som kan sakta ner eller stoppa spridningen av dessa aggressiva tumörer.
En dörr som hjälper cancern att sprida sig
För att en tumör ska bli dödlig måste dess celler bryta sig loss från ursprungsstället, sönderdela omgivande vävnad, ta sig in i blodomloppet och kolonisera avlägsna organ. uPAR är en nyckelspelare i denna process. Den sitter på cancercellens yta och samarbetar med partnerproteiner för att aktivera enzymer som löser upp den omgivande stödsstrukturen, vilket gör det lättare för celler att röra sig och invadera. uPAR återfinns i särskilt höga nivåer i trippelnegativa bröstcancerceller och i vissa hudcancerceller, och dess riklighet är kopplad till snabbare tillväxt, större invasivitet och sämre patientresultat. På grund av detta är uPAR ett attraktivt — men hittills underutnyttjat — mål för anticancerläkemedel.
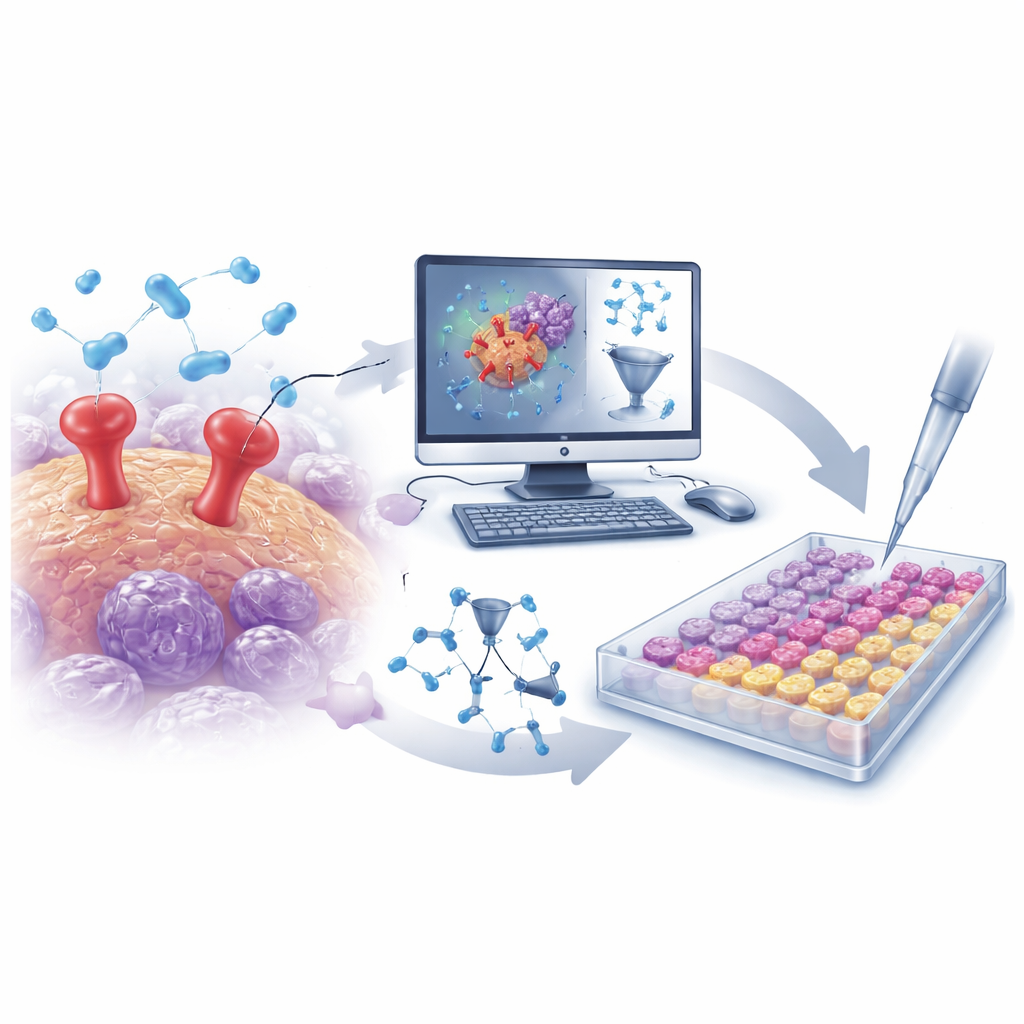
Att utvinna stora kemiska data med smarta algoritmer
Forskarna började med att sammanställa en stor samling på mer än 500 kända uPAR‑blockerande molekyler från en offentlig databas. Varje molekyls struktur översattes till tusentals numeriska deskriptorer som fångar egenskaper som storlek, form, laddningsfördelning och flexibilitet. Med dessa data byggde teamet en kvantitativ struktur‑aktivitet‑relationsmodell (QSAR) — ett slags matematiskt verktyg som lär sig vilka strukturella egenskaper som tenderar att göra en molekyl till en starkare uPAR‑hämmare. Efter noggrann validering för att undvika överanpassning visade modellen hög prediktiv förmåga på nya föreningar och framhävde flera nyckelattribut som antingen förstärkte eller försvagade uPAR‑blockering. Dessa insikter vägledde sökandet efter nya, bättre designade molekyler.
Från virtuella screens till riktiga provrör
Utrustade med den tränade QSAR‑modellen screenade teamet virtuellt ett fokuserat bibliotek på cirka 30 000 proteas‑inriktade molekyler. Modellen skar snabbt ner denna stora mängd till en liten uppsättning troliga uPAR‑hämmare. Parallellt användes datorbaserade dockningssimulationer för att se hur väl varje kandidat kunde passa in i uPAR:s bindningsställe, och molekylära dynamiksimuleringar testade om dessa dockade komplex skulle förbli stabila över tid. Från denna kombinerade in‑silico‑kampanj framträdde två framstående molekyler: D685‑0061, flaggad av QSAR‑modellen som mycket potent, och C878‑1660, markerad av dockning och simulering för att bilda särskilt stabila interaktioner med uPAR.
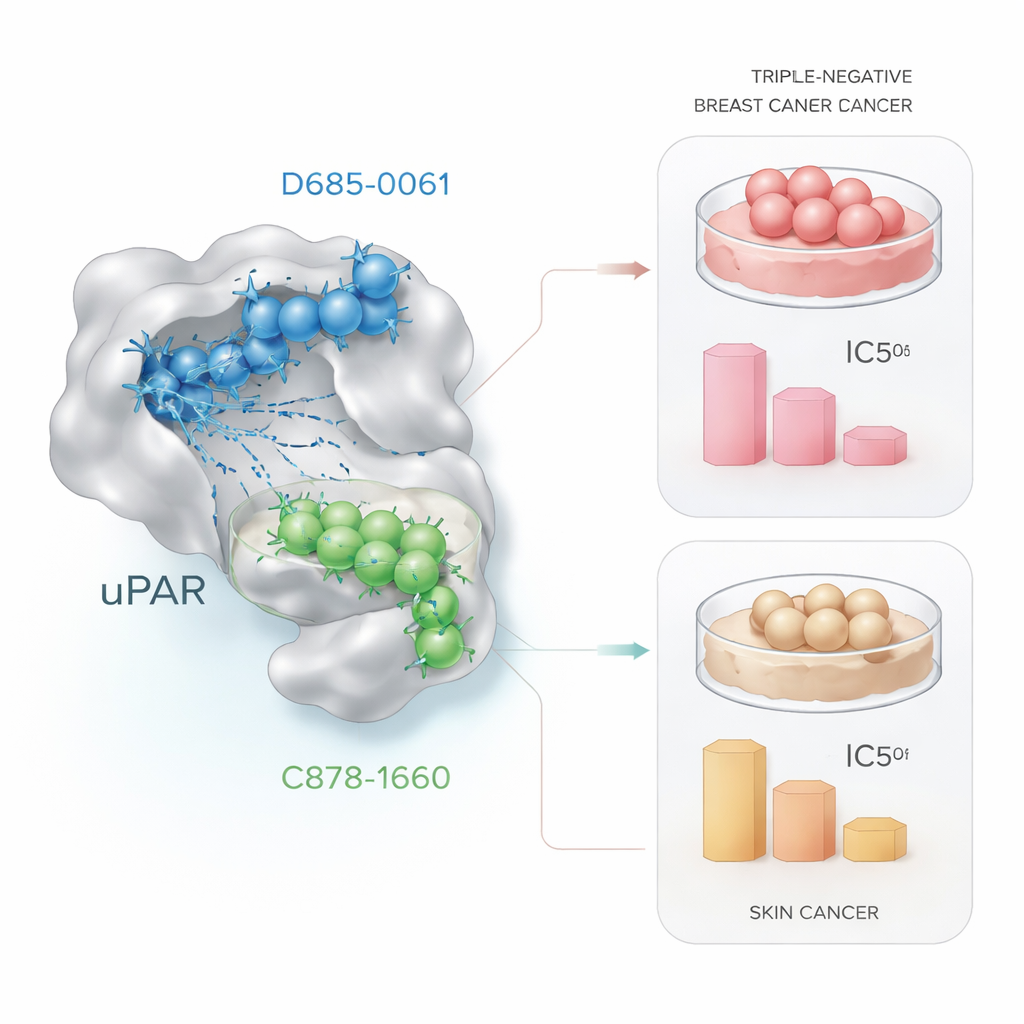
Att testa kandidaterna i cancerceller
Datorlöften är bara meningsfulla om de översätts till verkliga biologiska effekter. För att testa detta exponerade forskarna levande cancerceller för ökande doser av de två ledande molekylerna och mätte cellsurvival med en standardlaboratoriemetod kallad MTT‑analys. I trippelnegativa bröstceller (MDA‑MB‑231) dödade D685‑0061 celler mer effektivt och halverade viabiliteten vid omkring 21 mikromolar, medan C878‑1660 krävde ungefär fyra gånger så hög koncentration. Under mikroskopet visade celler behandlade med D685‑0061 tydliga tecken på programmerad celldöd, såsom rundning, avlossning från ytan och fragmentering. I kontrast var C878‑1660 den starkare mördaren i hudcancerceller (A431), och uppnådde 50 % celldöd vid cirka 19 mikromolar jämfört med ungefär 28 mikromolar för D685‑0061, återigen med synliga dosberoende skador.
Vad detta betyder för framtida cancerbehandlingar
Detta arbete levererar inte ett omedelbart nytt läkemedel, men det ger två lovande startpunkter och, lika viktigt, en kraftfull blåtryck för att hitta fler. Genom att länka stordata‑modellering, 3D‑simulationer och omsorgsfulla cellbaserade experiment visar studien att uPAR kan riktas selektivt med små molekyler som skadar aggressiva bröst‑ och hudcancerceller. D685‑0061 och C878‑1660 fungerar nu som ledföreningar som kemister kan förfina för att öka potens, förbättra säkerhet och optimera farmakokinetiska egenskaper. På längre sikt skulle läkemedel byggda på detta tillvägagångssätt kunna hjälpa till att blockera spridningen av uPAR‑drivna cancerformer och omvandla några av dagens farligaste tumörer till mer hanterbara sjukdomar.
Citering: Badukle, H., Jawarkar, R.D., Shah, U. et al. From in-silico QSAR modeling to in-vitro MTT assay: experimental validation of novel uPAR leads for triple-negative breast cancer (TNBC) and skin cancer. Sci Rep 16, 5786 (2026). https://doi.org/10.1038/s41598-026-36406-4
Nyckelord: uPAR‑hämmare, trippelnegativ bröstcancer, hudcancer, datorstödd läkemedelsdesign, MTT‑cellviabilitetsanalys