Clear Sky Science · sv
En täthetsfunktionalteoretisk studie av adsorption av cyklofosfamid och purinethol på ett kovalent triazinramverk (CTF-2) för läkemedelsleverans
Varför smartare kemoterapi spelar roll
Kemoterapidroger räddar liv, men de fungerar ofta mer som en strålkastare än som en laser—de angriper friska celler tillsammans med cancerösa. Det kan leda till allvarliga biverkningar, från trötthet och infektioner till organskada. Studien som beskrivs här undersöker ett ultratunt, mycket poröst material kallat ett kovalent triazinramverk (CTF-2) som en ”smart svamp” som kan bära två länge använda anticancermedel—cyklofosfamid och purinethol—på ett säkrare och mer effektivt sätt till där de behövs, för att sedan släppa dem under tumörliknande förhållanden.
En ny typ av molekylär svamp
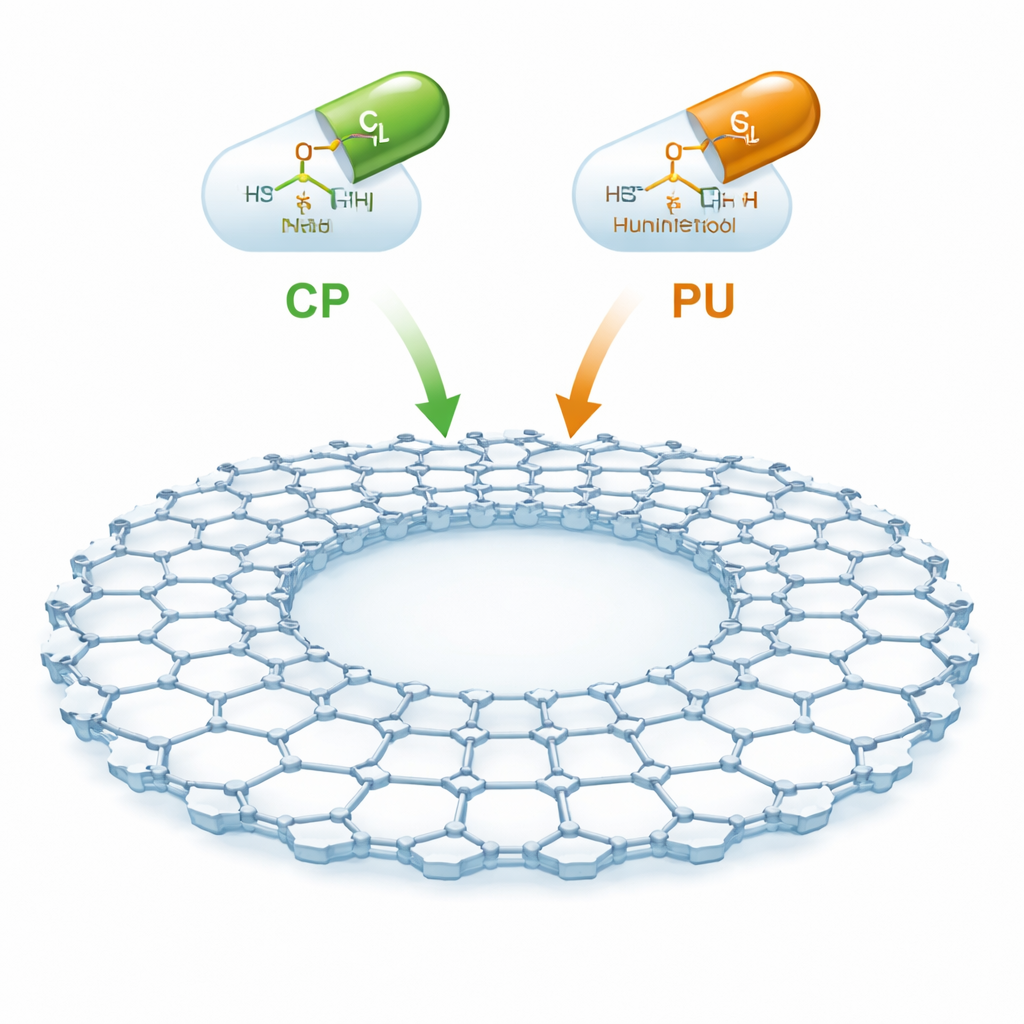
CTF-2 är ett människoskapad material uppbyggt av ringar av kol och kväve länkade till ett platt, skivliknande nätverk med en stor central kavitetsyta och gott om öppna utrymmen. Eftersom det är tunt, stabilt och fullt av porer erbjuder det en enorm intern yta för att fånga läkemedelsmolekyler. Författarna koncentrerade sig på två viktiga cancerläkemedel: cyklofosfamid, som används i stor utsträckning för blodcancer och solida tumörer, och purinethol (även kallat merkaptopurin), som används mot leukemier och vissa inflammatoriska tarmsjukdomar. Idén är att placera dessa läkemedel försiktigt på CTF-2:s yta så att de kan transporteras genom blodomloppet och frisättas mer selektivt, vilket minskar skadan för frisk vävnad.
Undersöka det osynliga med datorexperiment
I stället för att arbeta i ett våtlab använde teamet avancerade kvantnivåberäkningar (täthetsfunktionalteori och relaterade metoder) för att fråga hur starkt varje läkemedel skulle fästa vid CTF-2 och vad som håller komplexen samman. De optimerade formerna för CTF-2 tillsammans med varje läkemedel, mätte avstånden mellan atomer där de möts och beräknade hur mycket energi som frigörs när ett läkemedel adsorberas på ramverket. För cyklofosfamid var den beräknade adsorptionsenergin cirka −1,04 elektronvolt, något starkare än −0,82 elektronvolt som hittades för purinethol. Dessa värden, som förblir tydligt fördelaktiga även efter korrigering för tekniska artefakter och simulering av vatten som lösningsmedel, indikerar att båda läkemedlen binder tillräckligt stadigt för att kunna lastas men inte så starkt att de inte senare kan frigöras.
Mjuka krafter som gör viktigt arbete
Studien visar att ”limmet” mellan läkemedel och CTF-2 inte är en hård kemisk bindning utan ett nätverk av mjuka, icke-kovalenta krafter. Med specialiserade analyser av elektrontäthet—i praktiken kartor över var de delade elektronerna befinner sig—fann forskarna att van der Waals‑attraktioner (samma svaga krafter som låter gekon klättra på väggar) och milda elektrostatisk interaktioner dominerar. Dessa interaktioner sker på korta men icke-bindande avstånd mellan väte, kväve, syre, svavel och kolatomer på läkemedlen och på ramverket. Ytterligare beräkningar som delade upp den totala attraktionskraften i olika komponenter bekräftade att elektrostatiska och dispersions‑ (van der Waals) krafter ger det största bidraget till stabilisering, medan repulsiva krafter förhindrar att läkemedlet sjunker för djupt eller binder irreversibelt.
Tecken på stabil lastning och styrbar frisättning
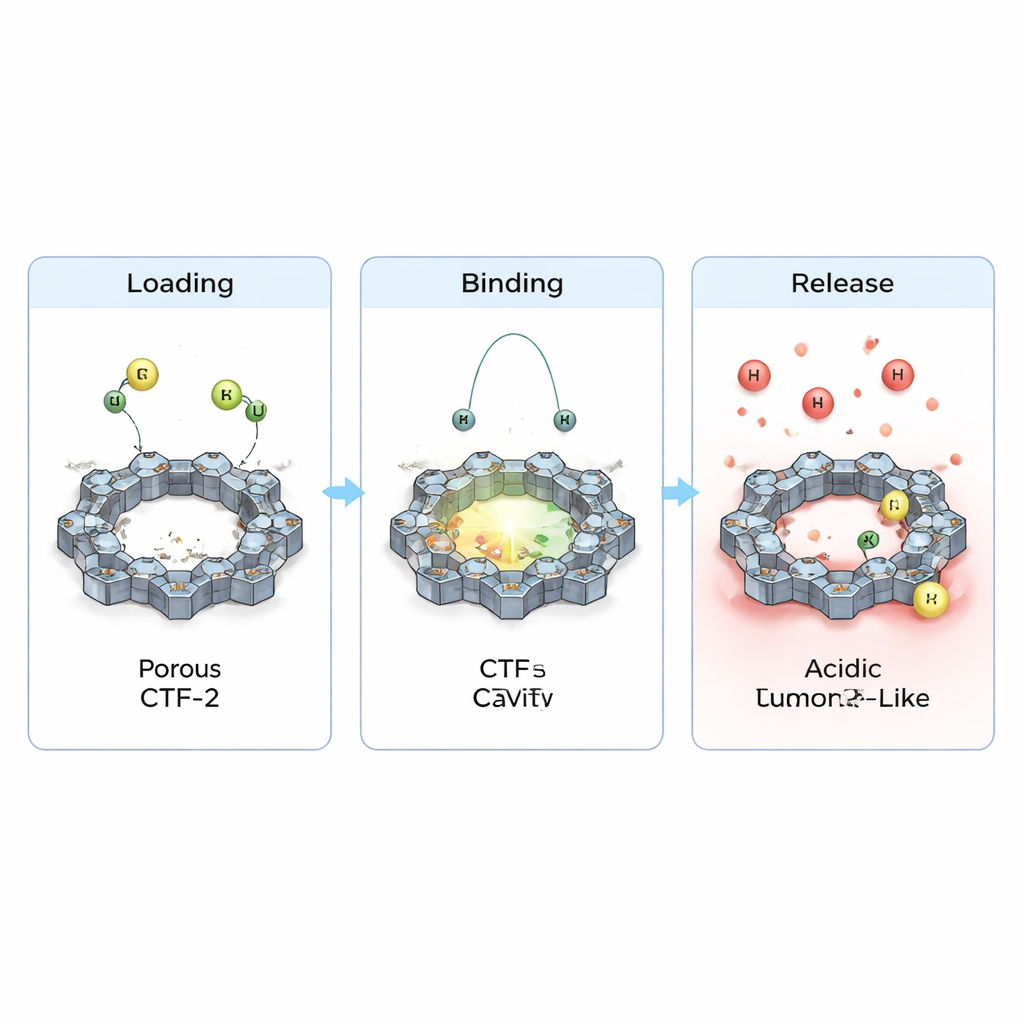
Teamet undersökte också hur elektroner förskjuts när läkemedlen sitter på CTF-2, och hur detta förändrar grundläggande elektriska egenskaper. De observerade små men tydliga överföringar av laddning mellan varje läkemedel och ramverket och en lätt förminskning av energigapet som skiljer fyllda från tomma elektroniska tillstånd. Detta tyder på att materialets reaktivitet och ledningsförmåga subtilt ändras vid lastning, en användbar egenskap för framtida sensorn eller theranostiska tillämpningar. Avgörande var att när de efterliknade den mer sura miljö som finns nära tumörer genom att tillföra extra protoner försvagades den beräknade bindningen och kontaktavstånden ökade. I enkla termer antyder simuleringarna att CTF-2 kan hålla kvar läkemedlen under normala blodliknande förhållanden, men tenderar att släppa dem lättare i tumörliknande, sura omgivningar—exakt det beteende som önskas för riktad leverans.
Vad detta betyder för framtida cancerbehandlingar
Sammantaget målar dessa beräkningar upp CTF-2 som en lovande bärare för cyklofosfamid och purinethol: det kan packa dem på sin porösa yta på ett stabilt sätt, skydda dem under cirkulationen och sedan frigöra dem när den lokala kemin förändras runt en tumör. Även om arbetet är teoretiskt och kräver experimentell bekräftelse, antyder det att fint designade, kväverika ramverk som CTF-2 skulle kunna hjälpa till att omvandla gamla men effektiva kemoterapidroger till smartare läkemedel—leverera potenta doser där de behövs mest samtidigt som de minskar de sidoverkningar som drabbar friska celler.
Citering: Tariq, T., Yar, M., Bayach, I. et al. A density functional theory study of cyclophosphamide and purinethol adsorption on a covalent triazine framework (CTF-2) for drug delivery applications. Sci Rep 16, 6125 (2026). https://doi.org/10.1038/s41598-026-36405-5
Nyckelord: nanobärare, läkemedelsleverans, cancerkemoeterapi, kovalent triazinramverk, beräkningsmodellering