Clear Sky Science · sv
En interaktiv kaskadiserad djupinlärningsram med expertförfining för noggrann segmentering av striatala subregioner
Varför kartläggning av små hjärnregioner spelar roll
Striatum, en liten struktur djupt inne i hjärnan, har en central roll för rörelse och motivation och påverkas i hög grad vid sjukdomar som Parkinsons. Läkare använder ofta PET‑ och MRI‑skanningar för att mäta kemiska förändringar i detta område, men striatum är uppdelat i många små subregioner som är svåra att urskilja och skissa ut exakt. Den här artikeln presenterar en ny datorstödd metod, kallad StriaSeg‑iARM, som hjälper specialister att rita dessa gränser mer exakt och effektivt, även hos personer vars hjärnor är förändrade av åldrande eller sjukdom.
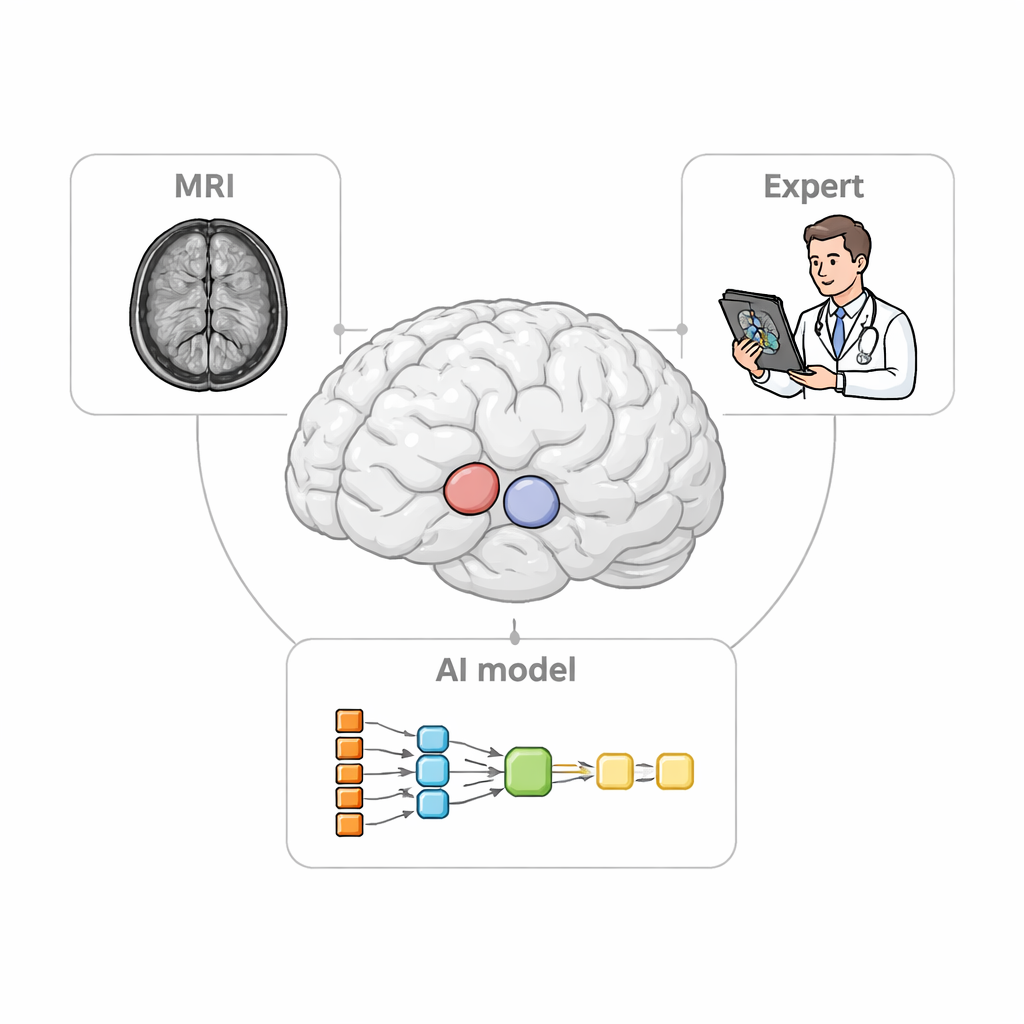
Det kliniska problemet rakt framför ögonen
När neurologer utvärderar tillstånd som Parkinsons sjukdom förlitar de sig på PET‑skanningar för att följa hur dopaminrelaterade signaler varierar över olika delar av striatum. För att göra detta korrekt måste de först definiera små tredimensionella ”intresseområden” på MRI, som fungerar som mätkoppar för PET‑data. Att manuellt rita dessa regioner är ett långsamt och mödosamt arbete och kan skilja sig från en expert till en annan. Befintlig programvara kan automatiskt lokalisera endast de större strukturerna och har ofta svårt att hantera patienter vars hjärnor är förminskade eller förvrängda—en vanlig situation vid avancerad neurodegenerativ sjukdom. Dessa brister kan sudda ut det verkliga skademönstret och minska bilddiagnostikens styrka som diagnostiskt verktyg.
En smartare tvåstegsassistent
Forskarna utformade StriaSeg‑iARM som ett tvåstegs djupinlärningssystem som arbetar direkt i varje persons eget hjärnrum i stället för att tvinga skanningen till en standardmall. I första steget hittar programmet hela striatum på en tredimensionell MRI. I det andra steget delar det upp denna struktur i 12 anatomiskt definierade subregioner på båda sidor av hjärnan. Mellan dessa två steg ligger den centrala nyheten: ett interaktivt steg där en expert snabbt kan kontrollera och, vid behov, korrigera den grova konturen från första steget innan den finare uppdelningen körs. Detta angreppssätt kombinerar automationens hastighet med en tränad observatörs omdöme.
Träning och testning i verkliga hjärnor
För att lära systemet vad det ska leta efter samlade teamet hundratals MRI‑skanningar från flera sjukhus och olika skannertyper och skapade noggranna manuella konturer av de 12 striatala subregionerna. De testade sedan modellen på två externa dataset som inkluderade både MRI och dopaminrelaterade PET‑skanningar: ett från relativt tidiga Parkinson‑patienter och friska frivilliga, och ett annat från en äldre, mer svårt påverkad klinisk grupp med påtaglig hjärnatrofi och blandade diagnoser. I dessa utmanande fall matchade StriaSeg‑iARM konsekvent de manuella expertkonturerna bättre än traditionella atlasbaserade metoder och en enklare ettstegs djupinlärningsmodell, med högre överlappning, mer exakta gränser och stabila volymmätningar.
Skarpare mätningar för hjärnkemi‑skanningar
Eftersom slutmålet är att kvantifiera PET‑signaler undersökte författarna också hur olika segmenteringsmetoder påverkade PET‑avläsningarna. Med en standardmått på spårämnesbindning i varje subregion jämförde de automatiska resultaten med dem baserade på manuella konturer. Atlasmetoden tenderade att underskatta bindningen, särskilt hos patienter med mer uttalade förändringar, medan den grundläggande djupinlärningsmodellen fortfarande visade märkbar bias i vissa regioner. I kontrast gav de kaskadiserade modellerna—särskilt när det interaktiva korrigeringssteget användes—PET‑värden som nära följde expertreferensen, med minimal bias och spridning. Teamet visade dessutom att en enkel osäkerhetspoäng från första steget kan flagga ungefär en fjärdedel av de svåraste fallen där expertförfining verkligen behövs, vilket håller resten fullt automatiska.
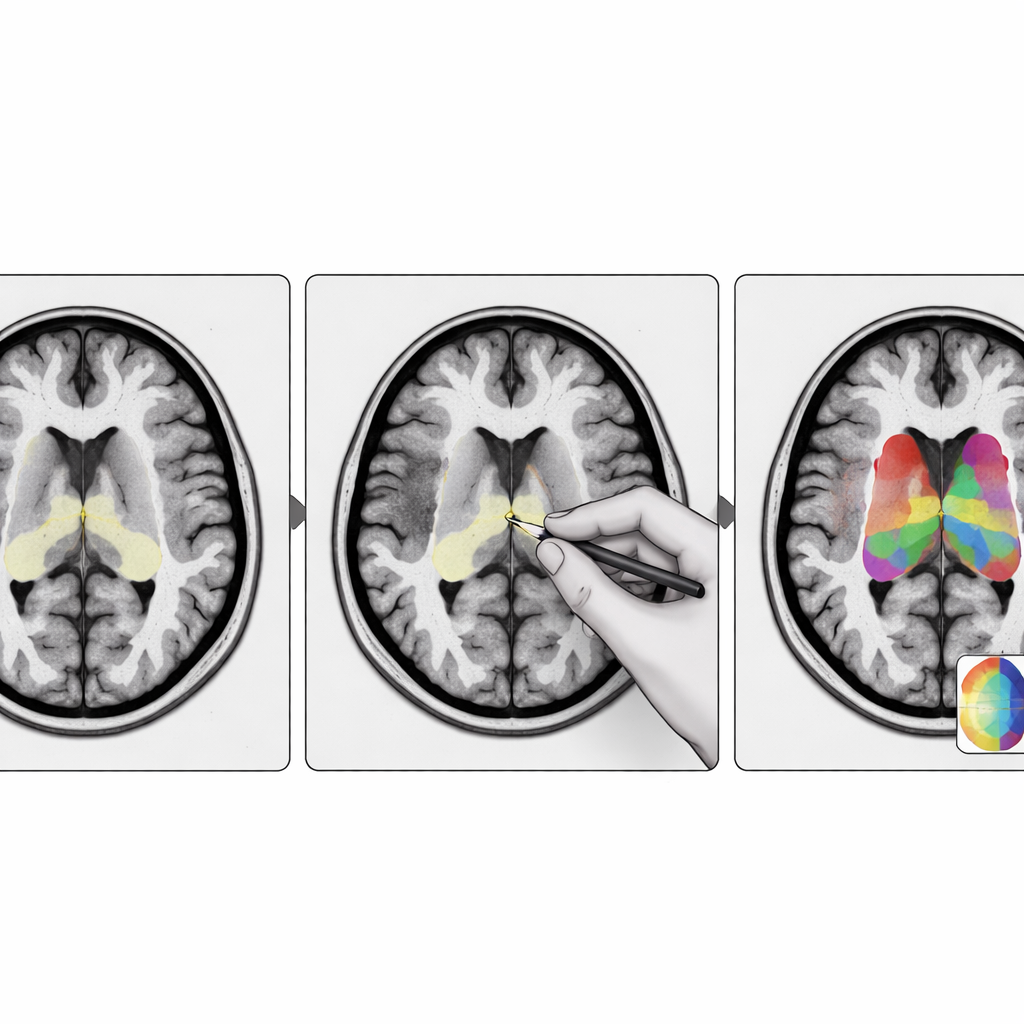
Vad detta betyder för patienter och kliniker
För icke‑specialister är huvudbudskapet att bättre digitala kartor över små hjärnregioner kan göra kemiska hjärnscanningar mer tillförlitliga. StriaSeg‑iARM erbjuder en flexibel ram där en djupinlärningsmodell utför majoriteten av arbetet, men specialister kan fortfarande kliva in för att korrigera knepiga fall utan att behöva träna om systemet. Denna kombination av automation och expertöversyn förbättrar precisionen i de mätningar som används för att diagnostisera och följa sjukdomar som Parkinsons, och den kan anpassas till andra organ och sjukdomar där små, svårupptäckta strukturer rymmer viktiga ledtrådar.
Citering: Kim, J., Kim, D., Kim, S. et al. An interactive cascaded deep learning framework with expert refinement for accurate striatal subregion segmentation. Sci Rep 16, 6550 (2026). https://doi.org/10.1038/s41598-026-36399-0
Nyckelord: Parkinsons sjukdomsbild, striatal segmentering, djupinlärning inom radiologi, hjärn‑PET MRI, neurodegenerativa biomarkörer