Clear Sky Science · sv
Implementering av high-throughput virtuell screening (HTVS) för identifiering av nya laktatdehydrogenas (LDH)-hämmare med antitumöregenskaper
Varför denna forskning är viktig för cancerbehandling
Cancerceller omprogrammerar ofta hur de tillverkar energi, och denna förändring kan utnyttjas för att designa smartare, mer selektiva läkemedel. Denna studie undersöker ett centralt metabolt enzym kallat laktatdehydrogenas (LDH), som hjälper tumörer att frodas i hårda miljöer och att stå emot behandling. Genom avancerad datorbaserad screening och laboratorietester identifierade forskarna två nya småmolekyler som blockerar LDH och visar lovande anticancereffekter i prostatacellinjer.
Cancercellernas ovanliga metabolism
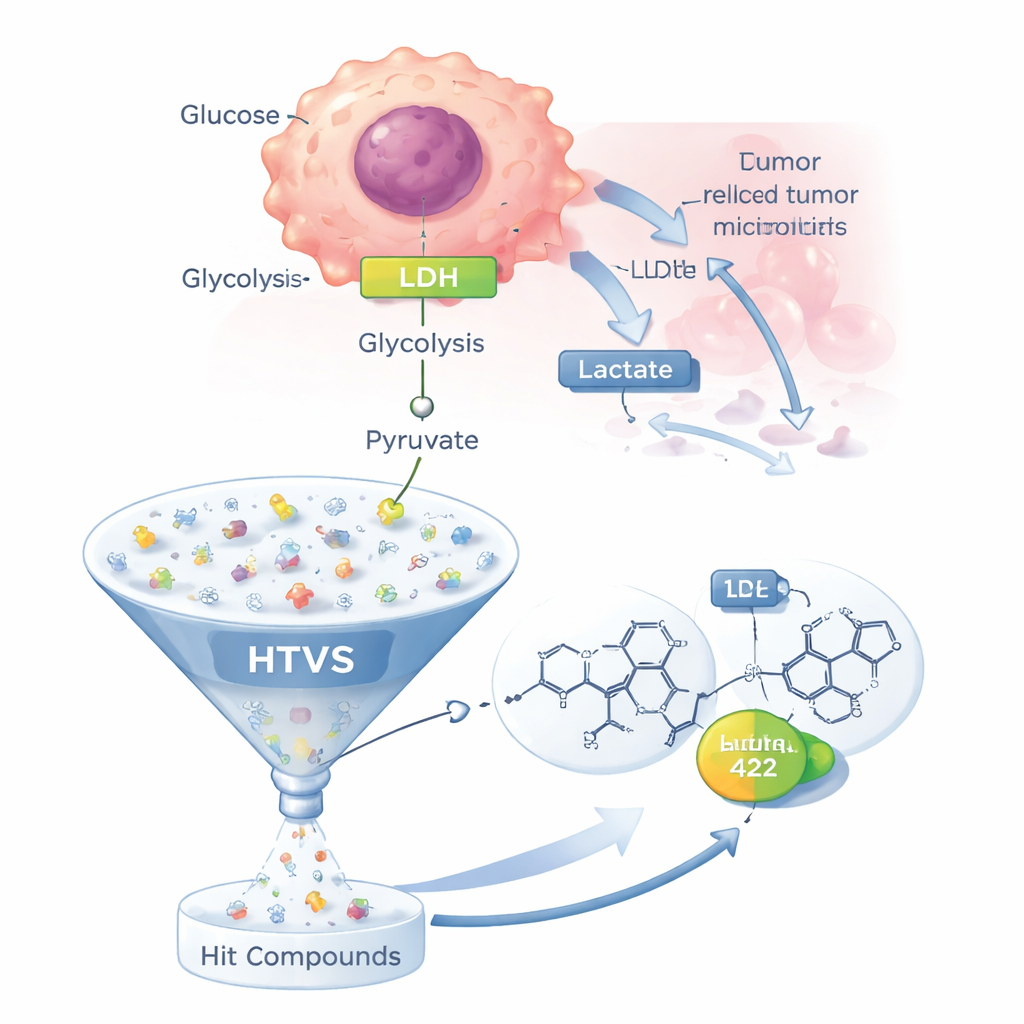
De flesta friska celler använder syre effektivt i sina mitokondrier för att generera energi. Många cancerceller förlitar sig däremot i hög grad på en mindre effektiv väg kallad glykolys, även när syre finns tillgängligt — ett fenomen känt som Warburg-effekten. I denna genväg bryts glukos ner till pyruvat, som sedan omvandlas till laktat av LDH istället för att gå in i mitokondrierna. Laktatet pumpas ut ur cellen och försurar tumörens omgivning, vilket hjälper cancerceller att undkomma celldöd, försvaga immunangrepp och till och med dämpa effekterna av många cytostatika. Eftersom LDH ligger i centrum för denna omställda metabolism och inget LDH-riktat läkemedel ännu godkänts, har det blivit ett högprioriterat mål för nya anticancermetoder.
Använder datorer för att sålla bland en halv miljon molekyler
I stället för att testa potentiella läkemedel en och en i laboratorium använde teamet en high-throughput virtuell screening (HTVS)-strategi. De började med 28 LDH-blockerande molekyler som redan rapporterats i vetenskaplig litteratur och extraherade därifrån en ”farmakofor” — ett abstrakt 3D-mönster av egenskaper som varje bra LDH-hämmare sannolikt delar. De tillämpade sedan denna modell på ett kommersiellt bibliotek med ungefär 500 000 läkemedelslika molekyler och frågade vilka kandidater som matchade de essentiella egenskaperna. Ungefär 110 000 molekyler klarade detta första filter, och vidare urval baserat på standardregler för ”drug-likeness” krympte listan till 2 337 mer realistiska kandidater för dockning mot LDH-enzymet.
Zooma in på de bästa bindarna
Nästa steg var att uppskatta hur tätt dessa kandidater kunde passa in i LDH:s aktiva säte. Genom flera nivåer av datorbaserad dockning beräknade forskarna hur varje molekyl skulle kunna interagera med specifika aminosyror inne i enzymets ficka. Denna mångstegprocess smalnade successivt av poolen från tusentals kandidater till bara 59 lovande molekyler, och sedan till fem tydliga »träffar« med särskilt stark förutsagd bindning. Två av dessa, betecknade föreningarna 15 och 422, stack ut eftersom molekyldynamiska simuleringar föreslog att de bildar ovanligt stabila komplex med LDH över tid, bevarar nyckelkontakter med kritiska rester i det aktiva sätet samtidigt som proteinets övergripande struktur förblir rimlig.
Från screen till verkliga cancerceller
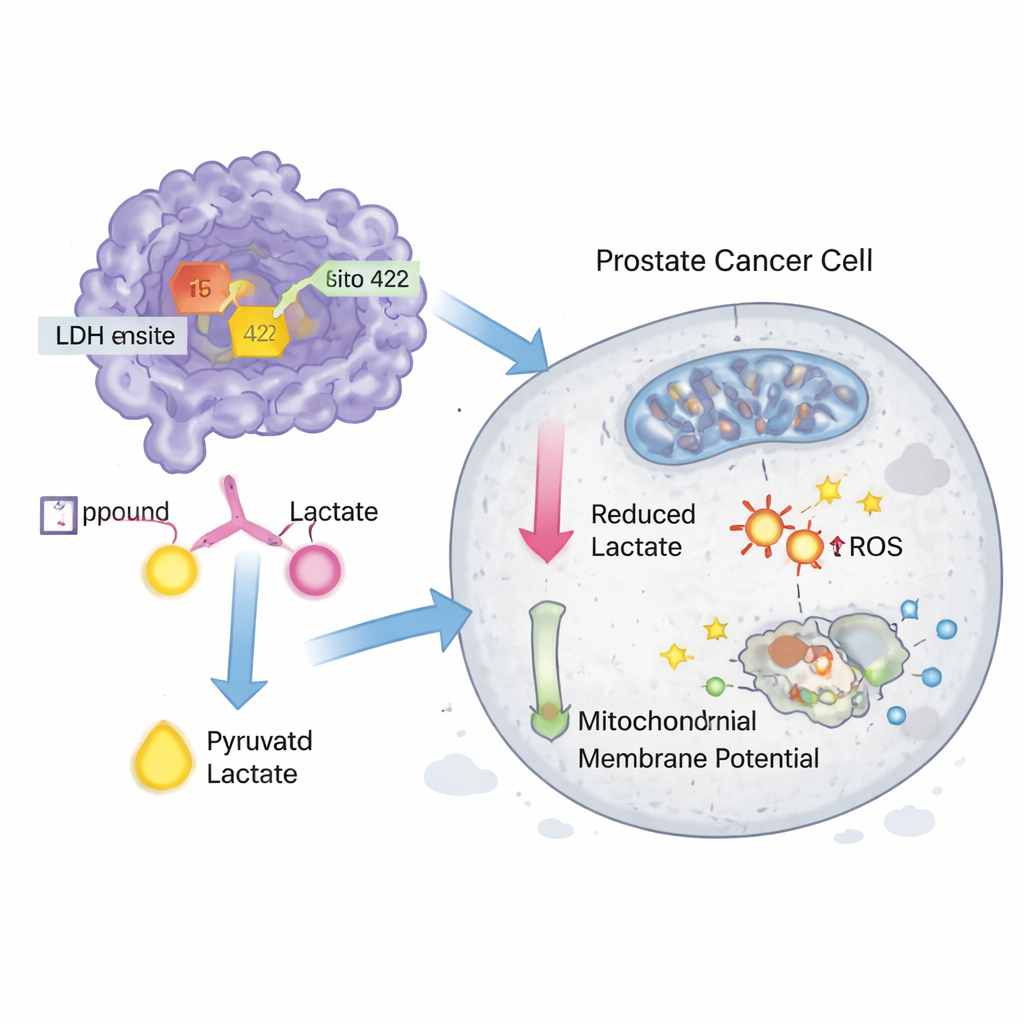
För att se om dessa träffar var relevanta i levande system köpte forskarna in föreningarna 15 och 422 och testade dem i prostatacellinjerna DU-145 och PC-3. Båda molekylerna hämmande LDH-aktivitet i celler vid nanomolarkoncentrationer och saktade också direkt aktiviteten hos ett renat LDH-enzym, även om de var något mindre potenta än en känd experimentell hämmare kallad GNE‑140. I tillväxtassayer minskade föreningarna cancercellernas överlevnad vid låga mikromolära doser, och närmade sig återigen prestationen hos GNE‑140. Ytterligare experiment visade att behandlingarna något ökade oxidativ stress, störde mitokondriens membranpotential — ett tecken på nedsatt energiproduktion — och utlöste programmerad celldöd (apoptos) i DU‑145-celler, där förening 15 var den mer aktiva av de två.
Vad detta kan betyda för framtida cancerläkemedel
Även om dessa molekyler inte är färdiga läkemedel ger de värdefulla utgångspunkter för läkemedelsdesign. Både föreningarna 15 och 422 har kemiska egenskaper som tyder på bättre löslighet, permeabilitet och övergripande »drug-likeness« än några befintliga LDH-hämmare, vilket gör dem till attraktiva leads för vidare optimering. Studien visar hur storskalig datorbaserad screening, styrd av kända strukturella egenskaper, kan upptäcka nya LDH-hämmare som försvagar cancerceller genom att svälta deras omställda energiförsörjning. Med framtida arbete för att förfina deras strukturer, testa direkt bindning mer noggrant och studera deras beteende i djurmodeller, skulle dessa föreningar kunna bidra till en ny klass anticancermedel som angriper tumörer via deras unika metabola sårbarheter.
Citering: Huang, Y., Benni, S., Yadav, U.P. et al. Deploying the high-throughput virtual screening (HTVS) approach for the identification of new lactate dehydrogenase (LDH) inhibitors with anticancer assets. Sci Rep 16, 5921 (2026). https://doi.org/10.1038/s41598-026-36385-6
Nyckelord: laktatdehydrogenas-hämmare, cancermetabolism, virtuell screening, prostatacancer, upptäckt av anticancermedel